
§14.3 酯的水解 相对分子质量较低的酯在没有催化剂存在时缓慢 水解。升高温度或在酸、碱存在下,水解速率加 快。 酯的水解反应是酯化反应的逆反应,在中性或酸 性条件下存在以下平衡关系: H RCOR H20 RCOH R OH 但在碱存在时,水解反应变为不可逆。酯的碱性 水解反应称为“皂化反应”,因为生成的羧酸与碱 生成了羧酸盐
• 相对分子质量较低的酯在没有催化剂存在时缓慢 水解。升高温度或在酸、碱存在下,水解速率加 快。 • 酯的水解反应是酯化反应的逆反应,在中性或酸 性条件下存在以下平衡关系: §14.3 酯的水解 RCOR ' O + H2O H + O + R ' RCOH OH 但在碱存在时,水解反应变为不可逆。酯的碱性 水解反应称为“皂化反应”,因为生成的羧酸与碱 生成了羧酸盐

§14.3 酯的水解 14.3.1 碱性水解 在酯的碱性水解反应中,碱逐渐消耗,实际上它 不是催化剂而是参加反应的试剂。因此反应过程中 碱用量>化学计量,反应可进行完全。 皂化速率=kCHL3 COOEt[OH] 在水解反应中酯分子可能在两个地方发生碱的断裂: 一R -R 酰氧断裂(Ac) 烷氧断裂(AI)
§14.3 酯的水解 14.3.1 碱性水解 在酯的碱性水解反应中,碱逐渐消耗,实际上它 不是催化剂而是参加反应的试剂。因此反应过程中 碱用量 > 化学计量,反应可进行完全。 皂化速率 = k2 [CH3COOEt][OH- ] 在水解反应中酯分子可能在两个地方发生碱的断裂: R C O O R ' R C O O R ' 酰氧断裂(Ac) 烷氧断裂(Al)

§14.3 酯的水解 14.3.1碱性水解 请看下列反应事实: 酯的碱性水解: 9 0 CH3CH2C15OCH2CH3 NaOH-CH3CH2CONa CH3CH215OH 水中加碱水解: 0 0 CH3COCSH2CHu-n 180H CH3C-180+n-CsHuOH 事实表明酯的碱性水解一般为酰氧断裂:
§14.3 酯的水解 14.3.1 碱性水解 请看下列反应事实: 事实表明酯的碱性水解一般为酰氧断裂: CH3CH2C 18 OCH2CH3 + NaOH O CH3CH2CONa + CH3CH2 18 OH O CH3COC5H2CH11 -n + 18 OH O CH3C- 18 O - + n-C5H11OH O 酯的碱性水解 : 水中加碱水解:
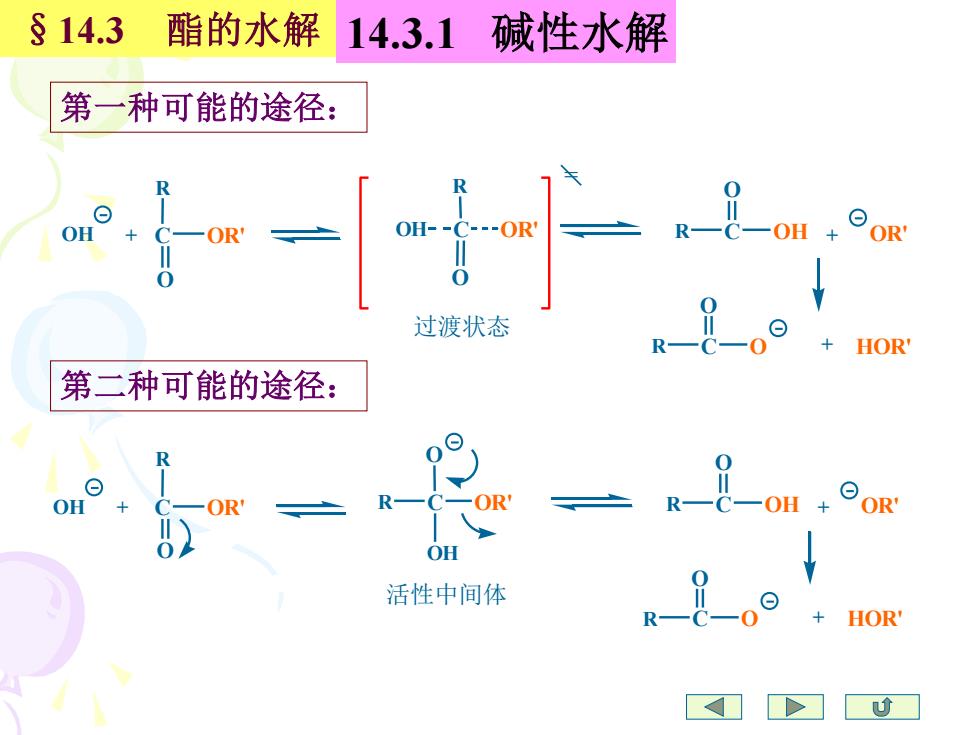
§14.3 酯的水解 14.3.1碱性水解 第一种可能的途径: OH - OR' -OH 过渡状态 HOR' 第二种可能的途径: OH R OR -OH OR OH 活性中间体 HOR
§14.3 酯的水解 14.3.1 碱性水解 R C O OH R C O OR' R C O OR' OH R C HOR' O O OH OR' + + 活性中间体 + R C O OH R C O OR' R C O OH OR' R C HOR' O O OH OR' + + 过渡状态 + = 第一种可能的途径: 第二种可能的途径:

§14.3 酯的水解 14.3.1碱性水解 羰基氧原子用8O标记后部分水解,然后回收未水解的 酯,测定18O的丰度,发现18O比原来的酯低,这说明反应过 程中发生质子交换。 OH 交换 -OR' 活性中间体
§14.3 酯的水解 14.3.1 碱性水解 羰基氧原子用18 O标记后部分水解,然后回收未水解的 酯,测定18 O的丰度,发现18 O比原来的酯低,这说明反应过 程中发生质子交换。 R C O 18 OH R C O OR' R O C OR' 18 OH OR' 18 OH + 活性中间体 + R C O 18 OH R C 18 O OR' R C 18 O OH + OH OR' + OR' 交换