
中华人民共和国国家标准 GB4789.10-2010 食品安全国家标准 食品微生物学检验金黄色葡萄球菌检验 National food safety standard Food microbiological examination:Staphylococcus aureu 2010-03-26发布 2010-06-01实施 中华人民共和国卫生部发布
中华人民共和国国家标准 GB 4789.10—2010 食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验 National food safety standard Food microbiological examination: Staphylococcus aureus 中华人民共和国卫生部 发布 2010-03-26 发布 2010-06-01 实施

GB4789.10-2010 前言 本标准代替GB/T4789.10-2008《食品卫生微生物学检验金黄色葡萄球菌检验》和 GB/T4789.37-2008《食品卫生微生物学检验金黄色葡萄球菌计数). 本标准与GB/T4789.10-2008和GB/T4789.37-2008相比,主要修改如下: 一修改了标准的中英文名称: 一修改了范围: 一规范了样品制备过程 一增加了计算公式中系数1.1的解释: -修改了附录A中胰酪胨大豆肉汤的名称,规范为10%氯化钠胰酪胨大豆肉汤: 一增加了第二法金黄色荷萄球菌Baird--Parker平板计数和第三法金黄色简萄球菌MPN计数。 本标准的附录A、附录B、附录C是规范性附录。 本标准所代替标准的历次版本发布情况为: GB4789.10-84、GB4789.10-1994、GB/T4789.10-2003、GB/T4789.10-2008。 GB/T4789.37-2008
GB 4789.10—2010 I 前 言 本标准代替 GB/T 4789.10-2008《食品卫生微生物学检验 金黄色葡萄球菌检验》和 GB/T 4789.37-2008《食品卫生微生物学检验 金黄色葡萄球菌计数》。 本标准与 GB/T 4789.10-2008 和 GB/T 4789.37-2008 相比,主要修改如下: ——修改了标准的中英文名称; ——修改了范围; ——规范了样品制备过程; ——增加了计算公式中系数 1.1 的解释; ——修改了附录 A 中胰酪胨大豆肉汤的名称,规范为 10%氯化钠胰酪胨大豆肉汤; ——增加了第二法金黄色葡萄球菌 Baird-Parker 平板计数和第三法金黄色葡萄球菌 MPN 计数。 本标准的附录 A、附录 B、附录 C 是规范性附录。 本标准所代替标准的历次版本发布情况为: ——GB 4789.10-84、GB 4789.10-1994、GB/T 4789.10-2003、GB/T 4789.10-2008。 ——GB/T 4789.37-2008

GB4789.10-2010 食品安全国家标准 食品微生物学检验金黄色葡萄球菌检验 1范围 本标准规定了食品中金黄色葡萄球菌(Sap咖lococcus aureus)的检验方法。 本标准第一法适用于食品中金黄色葡萄球菌的定性检验:第二法适用于金黄色葡萄球菌含量较高的 食品中金黄色葡萄球菌的计数:第三法适用于金黄色葡萄球菌含量较低而杂菌含量较高的食品中金黄色 葡萄球菌的计数。 2设备和材料 除微生物实验室常规灭南及培养设备外,其他设备和材料如下: 2.1恒温培养箱:36℃±1℃ 2.2冰箱:2℃一5℃。 2.3恒温水浴箱:37℃~65℃。 2.4天平:感量0.1g 2.5均质器。 2.6振荡器。 2.7无菌吸管:1mL(具0.01mL刻度)、10ml(具0.1mL刻度)或微量移液器及吸头。 2.8无菌锥形瓶:容量100mL、500mL。 2.9无菌培养皿:直径90mm。 2.10注射器:0.5mL。 2.11pH计或pH比色管或精密pH试纸 3培养基和试剂 3.110%氯化钠胰酪陈大豆肉汤:见附录A中A1。 3.27.5%氯化钠肉汤:见附录A中A2。 3.3血琼脂平板:见附录A中A3。 3.4 Baird-Parker琼脂平板:见附录A中A.4
GB 4789.10—2010 1 食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验 1 范围 本标准规定了食品中金黄色葡萄球菌(Staphylococcus aureus)的检验方法。 本标准第一法适用于食品中金黄色葡萄球菌的定性检验;第二法适用于金黄色葡萄球菌含量较高的 食品中金黄色葡萄球菌的计数;第三法适用于金黄色葡萄球菌含量较低而杂菌含量较高的食品中金黄色 葡萄球菌的计数。 2 设备和材料 除微生物实验室常规灭菌及培养设备外,其他设备和材料如下: 2.1 恒温培养箱:36 ℃±1 ℃。 2.2 冰箱:2 ℃~5 ℃。 2.3 恒温水浴箱:37 ℃~65 ℃。 2.4 天平:感量 0.1 g。 2.5 均质器。 2.6 振荡器。 2.7 无菌吸管:1 mL(具 0.01 mL 刻度)、10 mL(具 0.1 mL 刻度)或微量移液器及吸头。 2.8 无菌锥形瓶:容量 100 mL、500 mL。 2.9 无菌培养皿:直径 90 mm。 2.10 注射器:0.5 mL。 2.11 pH 计或 pH 比色管或精密 pH 试纸。 3 培养基和试剂 3.1 10 %氯化钠胰酪胨大豆肉汤:见附录 A 中 A.1。 3.2 7.5 %氯化钠肉汤:见附录 A 中 A.2。 3.3 血琼脂平板:见附录 A 中 A.3。 3.4 Baird-Parker 琼脂平板:见附录 A 中 A.4

GB4789.10-2010 3.5脑心浸出液肉汤(BH山:见附录A中A5。 3.6兔血浆:见附录A中A.6。 3.7稀释液:磷酸盐缓冲液:见附录A中A7。 3.8营养琼脂小斜面:见附录A中A8。 3.9革兰氏染色液:见附录A中A.9。 3.10无菌生理盐水:见附录A中A.10
GB 4789.10—2010 2 3.5 脑心浸出液肉汤(BHI) :见附录 A 中 A.5。 3.6 兔血浆:见附录 A 中 A.6。 3.7 稀释液:磷酸盐缓冲液:见附录 A 中 A.7。 3.8 营养琼脂小斜面:见附录 A 中 A.8。 3.9 革兰氏染色液:见附录 A 中 A.9。 3.10 无菌生理盐水:见附录 A 中 A.10
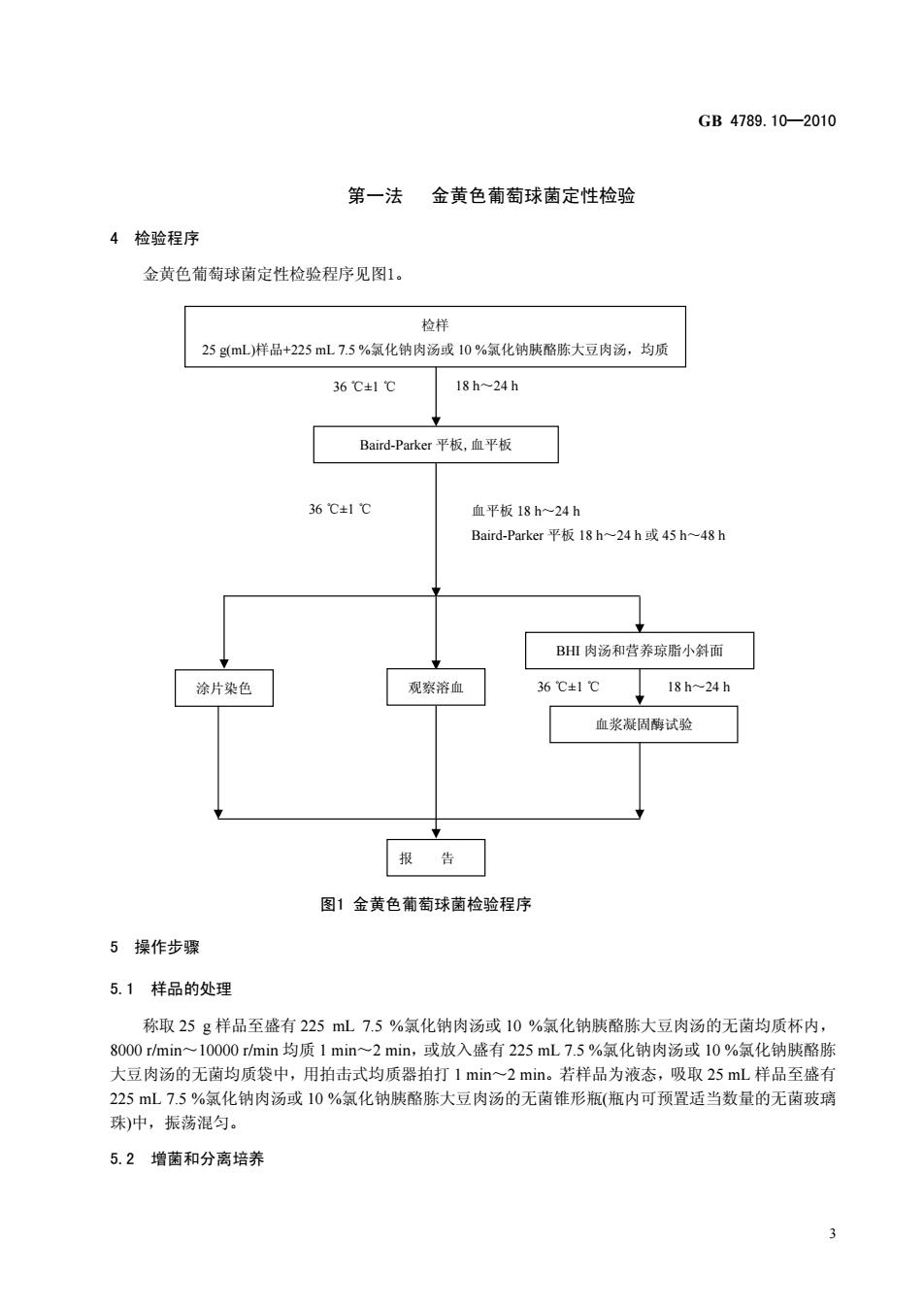
GB4789.10-2010 第一法金黄色葡萄球菌定性检验 4检验程序 金黄色葡萄球菌定性检验程序见图1 检样 25gmL)样品+225mL75%氧化钠肉汤或10%氧化钠胰酪陈大豆肉汤,均质 36℃±1℃ 18h-24h Band-Pate平板.直平板 36℃±1℃ 血平板18h~24h Baird--Parker平板18h-24h或45h~48h BH肉汤和营养琼脂小斜面 涂片染色 观察溶血 36±1℃ 18h-24h 血浆凝固悔试验 报告 图1金黄色葡萄球菌检验程序 5操作步骤 5.1样品的处理 称取25g样品至盛有225mL7.5%氯化钠肉汤或10%氯化钠胰酪胨大豆肉汤的无菌均质杯内 8000min一10000min均质1min一2min,或放入盛有225mL75%氯化钠肉汤域10%氯化钠胰酪 大豆肉汤的无菌均质袋中,用拍击式均质器拍打1min~2min。若样品为液态,吸取25mL样品至盛有 225mL7.5%氯化钠肉汤或10%氯化钠胰酪陈大豆肉汤的无菌锥形瓶(瓶内可预置适当数量的无茵玻璃 珠)中,振荡混匀。 5.2增菌和分离培养
GB 4789.10—2010 3 36 ±1 ℃ ℃ 18 h~24 h 36 ±1 ℃ ℃ 18 h~24 h 第一法 金黄色葡萄球菌定性检验 4 检验程序 金黄色葡萄球菌定性检验程序见图1。 图1 金黄色葡萄球菌检验程序 5 操作步骤 5.1 样品的处理 称取 25 g 样品至盛有 225 mL 7.5 %氯化钠肉汤或 10 %氯化钠胰酪胨大豆肉汤的无菌均质杯内, 8000 r/min~10000 r/min 均质 1 min~2 min,或放入盛有 225 mL 7.5 %氯化钠肉汤或 10 %氯化钠胰酪胨 大豆肉汤的无菌均质袋中,用拍击式均质器拍打 1 min~2 min。若样品为液态,吸取 25 mL 样品至盛有 225 mL 7.5 %氯化钠肉汤或 10 %氯化钠胰酪胨大豆肉汤的无菌锥形瓶(瓶内可预置适当数量的无菌玻璃 珠)中,振荡混匀。 5.2 增菌和分离培养 36 ±1 ℃ ℃ 血平板 18 h~24 h Baird-Parker 平板 18 h~24 h 或 45 h~48 h Baird-Parker 平板,血平板 检样 25 g(mL)样品+225 mL 7.5 %氯化钠肉汤或 10 %氯化钠胰酪胨大豆肉汤,均质 血浆凝固酶试验 BHI 肉汤和营养琼脂小斜面 涂片染色 观察溶血 报 告