
GAU 讲品果程 (2)同系列 直链b.p>支链 例如:正丁醇(118℃)和异丁醇(108.1℃); 直链:羟基在链端b.p>羟基不在链端 例如:」 正丁醇(118℃)和仲丁醇(99.5℃)。 (3)一0H数目↑→b.p↑ 例如:丙醇(97.4℃)和丙三醇(290℃) 2.在水中的溶解度 一OH数目↑,碳原子数目↓→S↑ 3.与无机盐生成结晶配合物 低级醇能与CaCl2、MgCl2、CuSO,等无机盐生成结晶配 合物,称为结晶醇。例如:CaCl2·4C2H0H Gansu Agricultural University PDF文件使用"pdfFactory”试用版本创建ww,fineprint.cn
精品课程 Gansu Agricultural University (2)同系列 直链 b.p > 支链 例如:正丁醇(118℃)和异丁醇(108.1℃); 直链:羟基在链端 b.p > 羟基不在链端 例如:正丁醇(118℃)和仲丁醇(99. 5℃)。 (3)—OH数目↑→ b.p↑ 例如:丙醇(97.4℃)和丙三醇(290℃) 2.在水中的溶解度 —OH数目↑,碳原子数目↓→ S↑ 3.与无机盐生成结晶配合物 低级醇能与CaCl2、MgCl2、CuSO4等无机盐生成结晶配 合物,称为结晶醇。例如:CaCl2 · 4C2H5OH
GAU 济品爆程 三、化学性质 醇分子相当于H,0分子中的一个一H被一R取代, 0:不等性sp3杂化 氧原子的电子构型 0g:1S22S22P4 SP3杂化 E ↑↓↑↑ ↑↓↑↓↑↑ 2P轨道 SP3杂化轨道 2S轨道 Gansu Agricultural University PDF文件使用"pdfFactory”试用版本创建ww.fineprint.cn
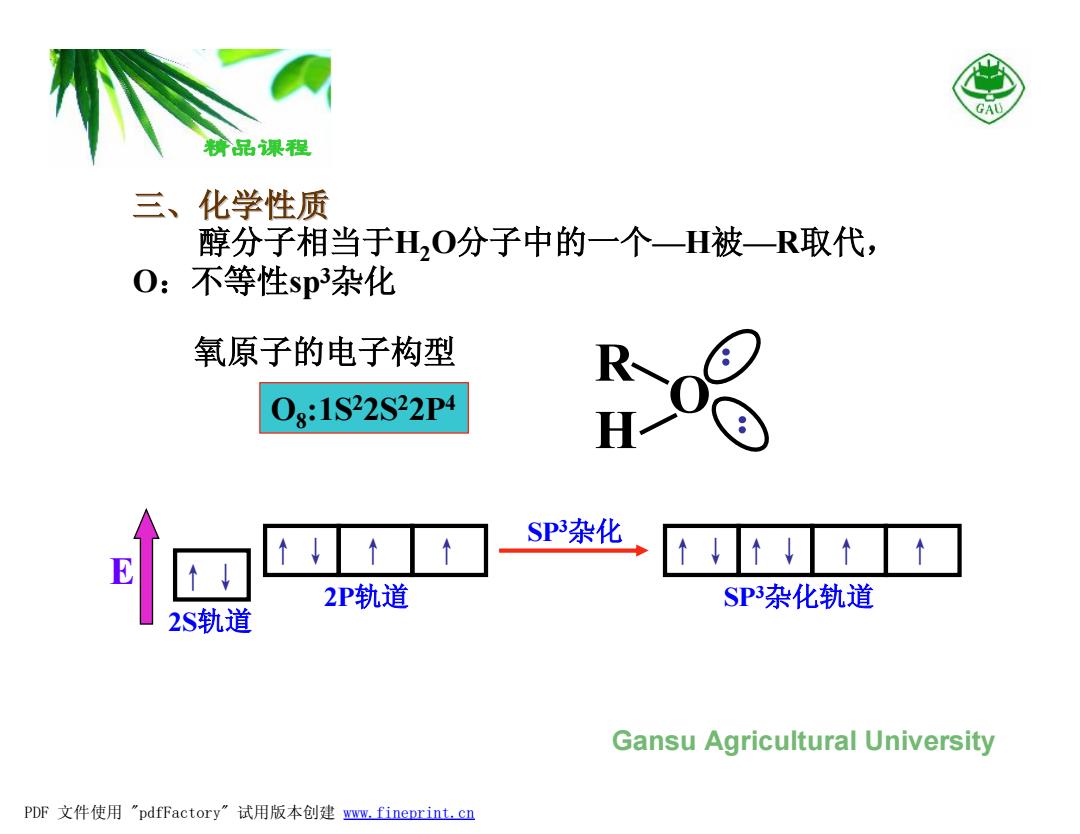
精品课程 Gansu Agricultural University 三、化学性质 醇分子相当于H2O分子中的一个—H被—R取代, O:不等性sp3杂化 氧原子的电子构型 O8 :1S22S22P4 ↑↓ ↑↓ ↑ ↑ SP3杂化 SP3杂化轨道 2S轨道 ↑↓ ↑↓ ↑ ↑ 2P轨道 E O R H : :

GAU 新品课程 醇反应性的总分析 氧化反应 形成氢键形芋 成盐 酸性(被金属取代) H H 脱水反应 取代反应 Gansu Agricultural University PDF文件使用"pdfFactory”试用版本创建w.fineprint.cn
精品课程 Gansu Agricultural University 醇反应性的总分析 C C O H H H 氧化反应 取 代 反 应 脱 水 反 应 酸性(被金属取代) 形成氢键形 成盐 金羊

GAU 精品爆程 1.与活泼金属的反应(p152)一0十H HOH Na >NaOH H2 反应剧烈 ROH Na >RONa H2 反应温和 讨论:( ①反应本质 弱酸的电离平衡:H20+H20。一H30++OH ROH H20H30+OR- 任何能使负离子稳定的因素,都有利于弱酸的电离, 达平衡时HO]↑→酸性↑。 Gansu Agricultural University PDF文件使用"pdfFactory”试用版本创建ww.fineprint.cn
精品课程 Gansu Agricultural University 1.与活泼金属的反应(p152) O H HOH + Na NaOH + H2 ROH + Na RONa + H2 反应剧烈 反应温和 讨论: ① 反应本质 弱酸的电离平衡: ROH + H 2O H 3O+ + OR - H2O + H 2O H 3O+ + OH - 任何能使负离子稳定的因素,都有利于弱酸的电离, 达平衡时[H3O+ ]↑→ 酸性↑

GAU 新品课程 一O1上所连的斥电子基↑+R0的稳定性+}一 醇的电离↓→ 一OH周围空间位阻↑ →溶剂化作用↓ 达到平衡时,H01↓→酸性↓ ②醇的酸性次序: H20>CH,OH>1°>2°>3°ROH ③OH(Lewis碱)→结合质子质子化醇(金羊盐): ROH+HC1÷[ROH2]+C1 Gansu Agricultural University PDF文件使用"pdfFactory”试用版本创建ww.fineprint.cn
精品课程 Gansu Agricultural University —OH上所连的斥电子基↑→RO-的稳定性↓ —OH周围空间位阻↑ → 溶剂化作用↓ 醇的电离↓→ 达到平衡时,[H3O+ ]↓→酸性↓ ② 醇的酸性次序: H2O > CH3OH > 1°> 2°> 3°ROH ③ —OH (Lewis 碱) 结合质子 质子化 醇(金羊盐 ): ROH+HCl [ROH2]+Cl