§13.2 一元羧酸的物理性质 13.2.1熔点,沸点 分子中有两个部位可形成H-键,常以二聚体存在。 H-O R- C-R (1)沸点(b.p)很高(比M相近的醇高) 例: M甲酸= Mz醇' b.p 100.7℃ 78.5℃ (2)与水形成H-键=>易溶于水 C1一C4的酸与水混溶,R增大,水溶性!
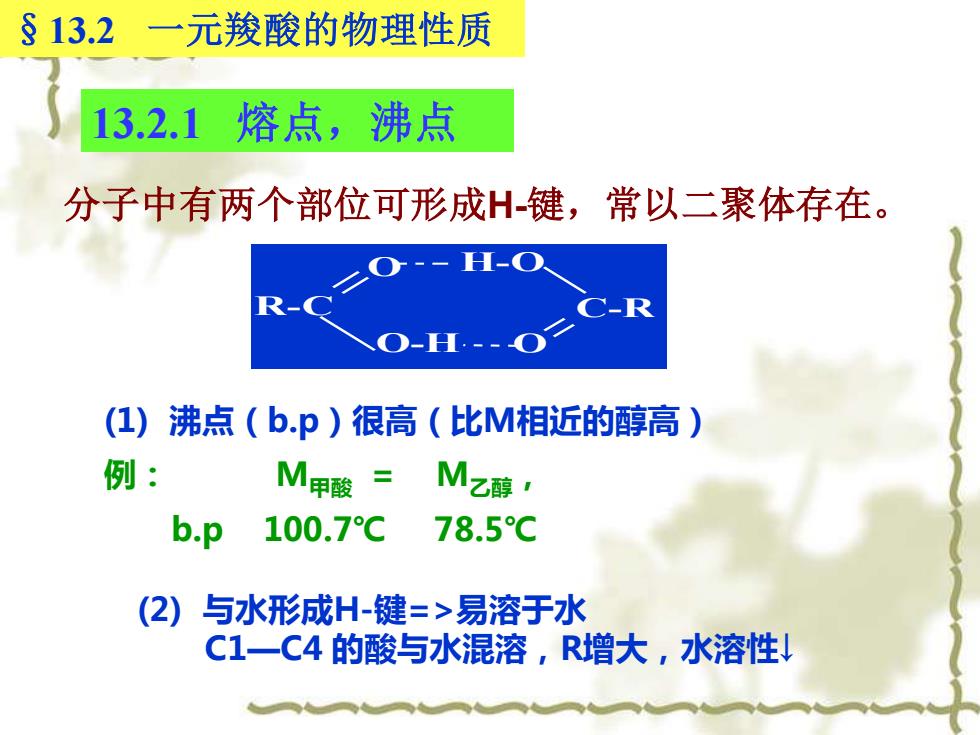
(1) 沸点(b.p)很高(比M相近的醇高) 例: M甲酸 = M乙醇, b.p 100.7℃ 78.5℃ R-C O H-O O O-H C-R 13.2.1 熔点,沸点 分子中有两个部位可形成H-键,常以二聚体存在。 (2) 与水形成H-键=>易溶于水 C1—C4 的酸与水混溶,R增大,水溶性↓ §13.2 一元羧酸的物理性质
§13.2一元羧酸的物理性质 13.2.2 红外光谱 羧酸中的C=O: 单体 二缔合体 RCOOH 1770~1750cm1 ~1710cm-1 CH,=CHCOOH ~1720cm-1 ~1690cm1 ArCOOH 1700-1690cm 羧酸中的OH: ~3550cm1 3000~2500cm 羧酸中的C-0 ~1250cm-1
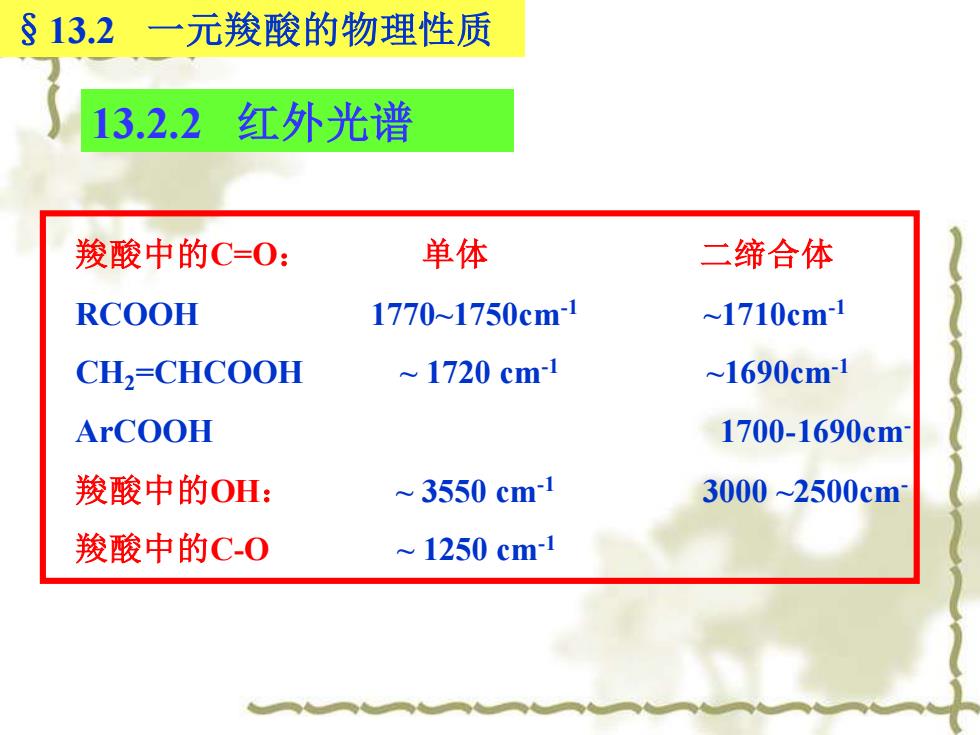
13.2.2 红外光谱 §13.2 一元羧酸的物理性质 羧酸中的C=O: 单体 二缔合体 RCOOH 1770~1750cm-1 ~1710cm-1 CH2=CHCOOH ~ 1720 cm-1 ~1690cm-1 ArCOOH 1700-1690cm- 羧酸中的OH: ~ 3550 cm-1 3000 ~2500cm- 羧酸中的C-O ~ 1250 cm-1

§13.2一元羧酸的物理性质 13.2.3 核磁共振谱 HNMR R,CHCOOH δ 1012 HCR,COOH δu 2≈2.6
1HNMR R2CHCOOH H: 10~12 HCR2COOH H: 2~2.6 13.2.3 核磁共振谱 §13.2 一元羧酸的物理性质

§13.3 一元羧酸的酸性 1.羧酸根比较稳定,所以羧酸的氢能解离而 表现出酸性。 2.多数的羧酸是弱酸,pKa约为4-5 (大部分的羧酸是以未解离的分子形式存在) 3.羧酸可以和碳酸氢钠反应,生成羧酸盐。 RCOOH NaHCO3- →RCOO-Na+CO2+H2O
1. 羧酸根比较稳定,所以羧酸的氢能解离而 表现出酸性。 2. 多数的羧酸是弱酸,pKa约为4-5 (大部分的羧酸是以未解离的分子形式存在) §13.3 一元羧酸的酸性 3. 羧酸可以和碳酸氢钠反应,生成羧酸盐。 RCOOH + NaHCO3 RCOO-Na + CO2 +H2O

§13.3 一元羧酸的酸性 13.3.1羧酸的电离 羧酸最重要的性质之一是具有酸性,在水中可离解出 质子,能使石蕊试纸变红。 R-COOH-K2 R-COO+HT Ka HJRCOO] =1.75×10-5 RCOOHI 羧酸的酸性强度,一般用解离常数Ka值或pKa值表示: pKa=-lgKa pKa 则酸性
13.3.1 羧酸的电离 §13.3 一元羧酸的酸性 羧酸最重要的性质之一是具有酸性,在水中可离解出 质子,能使石蕊试纸变红。 R-COOH R-COO- + H+ Ka Ka = [H + ][RCOO - ] [RCOOH] = 1.75×10 -5 羧酸的酸性强度,一般用解离常数Ka值或pKa值表示: pKa = -lgKa pKa 则酸性