
2.熵的定义 对微小变化 -9. 熵是系统混乱度的量度,只能通过可逆过程计算熵变 物理化学(B)I
物理化学(B)I 2. 熵的定义 ( )R i i i Q S T = R d ( ) Q S T 对微小变化 = 熵是系统混乱度的量度,只能通过可逆过程计算熵变

3.判据 (1)克劳修斯不等式(封闭系统可逆性判据) >不可逆过程 dS≥ δ2 T =可逆过程 dS(绝热)≥0 (2)自发变化的判据 ">"表示不可逆,自发 (dS)u.m≥0 "="表示可逆,平衡 物理化学(B)I
物理化学(B)I 3. 判据 (1)克劳修斯不等式(封闭系统可逆性判据) d Q S T > 不可逆过程 = 可逆过程 d 0 S(绝热) (2)自发变化的判据 , (d ) 0 S U V " " = 表示可逆,平衡 " " 表示不可逆,自发

(2)自发变化的判据 "<"表示不可逆,自发 (d0≤0"-”表示可逆,平衡 "<"表示不可逆,自发 (dG)r.pm=o≤0 "="表示可逆,平衡 最大功(有效功)原理 (△4)r=WR (AA)Iv=(WPR (AG)Ip=(WPR 物理化学(B)I
物理化学(B)I (2)自发变化的判据 f , , 0 (d ) 0 A T V W = " " 表示不可逆,自发 " " = 表示可逆,平衡 f , , 0 (d ) 0 G T p W = " " 表示不可逆,自发 " " = 表示可逆,平衡 最大功(有效功)原理 (A)T = WR (A)T,V =(Wf )R (G)T,p =(Wf )R
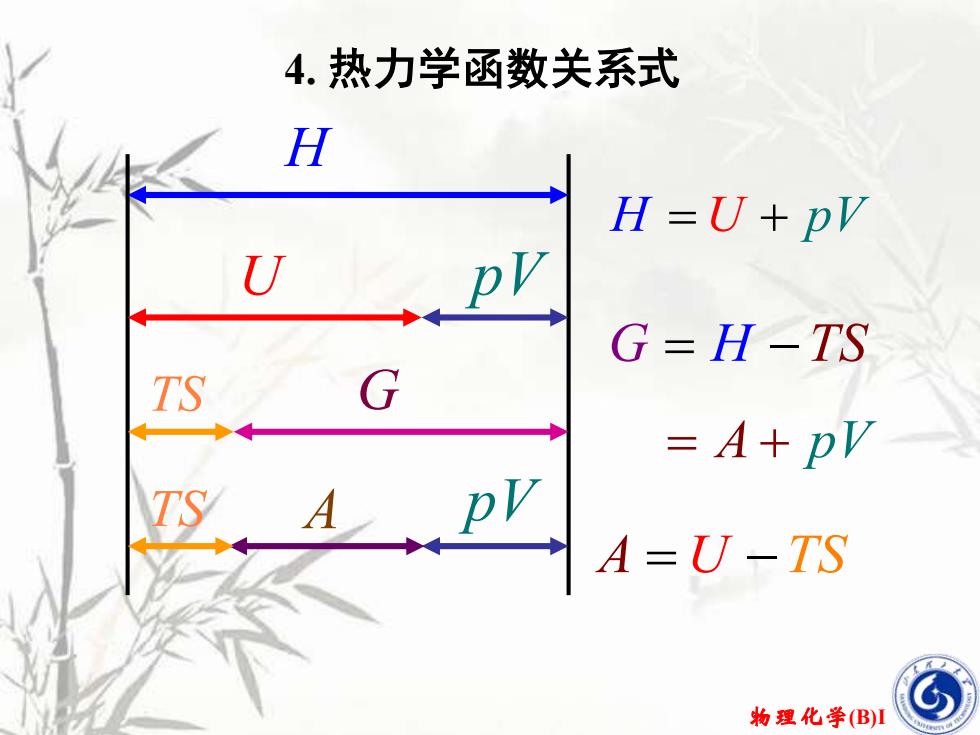
4.热力学函数关系式 H H=U+pV U G-H-TS TS G =A+pV TS A A=U-TS 物理化学(B)1
物理化学(B)I 4. 热力学函数关系式 G = − H TS H pV H = + U pV U A TS G TS A = − U TS pV = + A pV

5.热力学基本方程 (1) dU TdS-pdv (2) dH TdS +Vdp (3)d4=-SdT-pdv (4) dG=-SdT+Vdp 从公式(1),(2)导出 从公式(1),3)导出 7=( 从公式(2),(4)导出 从公式3),(4)导出 v- S=-( 适用于组成不变的封闭系统且只有体积功时的基本公式 物理化学(B)I
物理化学(B)I 5. 热力学基本方程 d d d U T S p V = − (1) (2) d d d H T S V p = + (3) d d d A S T p V = − − (4) d d d G S T V p = − + 适用于组成不变的封闭系统且只有体积功时的基本公式 ( )V U T S = 从公式(1), (2)导出 ( )S U V p = − 从公式(1), (3)导出 ( )S H V p = 从公式(2), (4)导出 ( )V A T S = − 从公式(3), (4)导出 ( ) p H S = ( )T A V = − ( )T G p = ( ) p G T = −