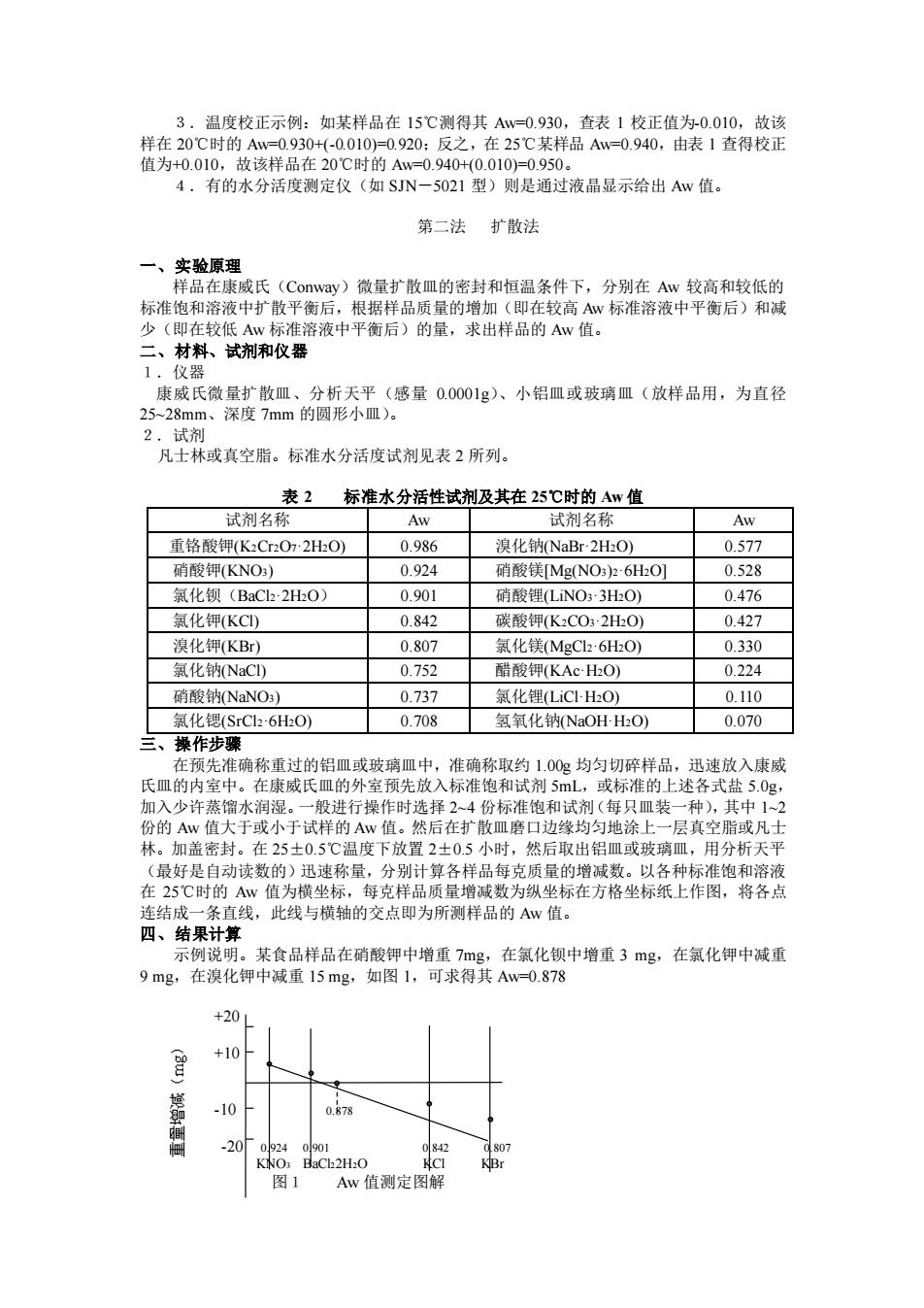
3.温度校正示例:如某样品在 15℃测得其 Aw=0.930,查表 1 校正值为-0.010,故该 样在 20℃时的 Aw=0.930+(-0.010)=0.920;反之,在 25℃某样品 Aw=0.940,由表 1 查得校正 值为+0.010,故该样品在 20℃时的 Aw=0.940+(0.010)=0.950。 4.有的水分活度测定仪(如 SJN-5021 型)则是通过液晶显示给出 Aw 值。 第二法 扩散法 一、实验原理 样品在康威氏(Conway)微量扩散皿的密封和恒温条件下,分别在 Aw 较高和较低的 标准饱和溶液中扩散平衡后,根据样品质量的增加(即在较高 Aw 标准溶液中平衡后)和减 少(即在较低 Aw 标准溶液中平衡后)的量,求出样品的 Aw 值。 二、材料、试剂和仪器 1.仪器 康威氏微量扩散皿、分析天平(感量 0.0001g)、小铝皿或玻璃皿(放样品用,为直径 25~28mm、深度 7mm 的圆形小皿)。 2.试剂 凡士林或真空脂。标准水分活度试剂见表 2 所列。 表 2 标准水分活性试剂及其在 25℃时的 Aw 值 试剂名称 Aw 试剂名称 Aw 重铬酸钾(K2Cr2O7·2H2O) 0.986 溴化钠(NaBr·2H2O) 0.577 硝酸钾(KNO3) 0.924 硝酸镁[Mg(NO3)2·6H2O] 0.528 氯化钡(BaCl2·2H2O) 0.901 硝酸锂(LiNO3·3H2O) 0.476 氯化钾(KCl) 0.842 碳酸钾(K2CO3·2H2O) 0.427 溴化钾(KBr) 0.807 氯化镁(MgCl2·6H2O) 0.330 氯化钠(NaCl) 0.752 醋酸钾(KAc·H2O) 0.224 硝酸钠(NaNO3) 0.737 氯化锂(LiCl·H2O) 0.110 氯化锶(SrCl2·6H2O) 0.708 氢氧化钠(NaOH·H2O) 0.070 三、操作步骤 在预先准确称重过的铝皿或玻璃皿中,准确称取约 1.00g 均匀切碎样品,迅速放入康威 氏皿的内室中。在康威氏皿的外室预先放入标准饱和试剂 5mL,或标准的上述各式盐 5.0g, 加入少许蒸馏水润湿。一般进行操作时选择 2~4 份标准饱和试剂(每只皿装一种),其中 1~2 份的 Aw 值大于或小于试样的 Aw 值。然后在扩散皿磨口边缘均匀地涂上一层真空脂或凡士 林。加盖密封。在 25±0.5℃温度下放置 2±0.5 小时,然后取出铝皿或玻璃皿,用分析天平 (最好是自动读数的)迅速称量,分别计算各样品每克质量的增减数。以各种标准饱和溶液 在 25℃时的 Aw 值为横坐标,每克样品质量增减数为纵坐标在方格坐标纸上作图,将各点 连结成一条直线,此线与横轴的交点即为所测样品的 Aw 值。 四、结果计算 示例说明。某食品样品在硝酸钾中增重 7mg,在氯化钡中增重 3 mg,在氯化钾中减重 9 mg,在溴化钾中减重 15 mg,如图 1,可求得其 Aw=0.878 +20 +10 -10 0.878 -20 0.924 0.901 0.842 0.807 KNO3 BaCl22H2O KCl KBr 图1 Aw 值测定图解
3.温度校正示例:如某样品在 15℃测得其 Aw=0.930,查表 1 校正值为-0.010,故该 样在 20℃时的 Aw=0.930+(-0.010)=0.920;反之,在 25℃某样品 Aw=0.940,由表 1 查得校正 值为+0.010,故该样品在 20℃时的 Aw=0.940+(0.010)=0.950。 4.有的水分活度测定仪(如 SJN-5021 型)则是通过液晶显示给出 Aw 值。 第二法 扩散法 一、实验原理 样品在康威氏(Conway)微量扩散皿的密封和恒温条件下,分别在 Aw 较高和较低的 标准饱和溶液中扩散平衡后,根据样品质量的增加(即在较高 Aw 标准溶液中平衡后)和减 少(即在较低 Aw 标准溶液中平衡后)的量,求出样品的 Aw 值。 二、材料、试剂和仪器 1.仪器 康威氏微量扩散皿、分析天平(感量 0.0001g)、小铝皿或玻璃皿(放样品用,为直径 25~28mm、深度 7mm 的圆形小皿)。 2.试剂 凡士林或真空脂。标准水分活度试剂见表 2 所列。 表 2 标准水分活性试剂及其在 25℃时的 Aw 值 试剂名称 Aw 试剂名称 Aw 重铬酸钾(K2Cr2O7·2H2O) 0.986 溴化钠(NaBr·2H2O) 0.577 硝酸钾(KNO3) 0.924 硝酸镁[Mg(NO3)2·6H2O] 0.528 氯化钡(BaCl2·2H2O) 0.901 硝酸锂(LiNO3·3H2O) 0.476 氯化钾(KCl) 0.842 碳酸钾(K2CO3·2H2O) 0.427 溴化钾(KBr) 0.807 氯化镁(MgCl2·6H2O) 0.330 氯化钠(NaCl) 0.752 醋酸钾(KAc·H2O) 0.224 硝酸钠(NaNO3) 0.737 氯化锂(LiCl·H2O) 0.110 氯化锶(SrCl2·6H2O) 0.708 氢氧化钠(NaOH·H2O) 0.070 三、操作步骤 在预先准确称重过的铝皿或玻璃皿中,准确称取约 1.00g 均匀切碎样品,迅速放入康威 氏皿的内室中。在康威氏皿的外室预先放入标准饱和试剂 5mL,或标准的上述各式盐 5.0g, 加入少许蒸馏水润湿。一般进行操作时选择 2~4 份标准饱和试剂(每只皿装一种),其中 1~2 份的 Aw 值大于或小于试样的 Aw 值。然后在扩散皿磨口边缘均匀地涂上一层真空脂或凡士 林。加盖密封。在 25±0.5℃温度下放置 2±0.5 小时,然后取出铝皿或玻璃皿,用分析天平 (最好是自动读数的)迅速称量,分别计算各样品每克质量的增减数。以各种标准饱和溶液 在 25℃时的 Aw 值为横坐标,每克样品质量增减数为纵坐标在方格坐标纸上作图,将各点 连结成一条直线,此线与横轴的交点即为所测样品的 Aw 值。 四、结果计算 示例说明。某食品样品在硝酸钾中增重 7mg,在氯化钡中增重 3 mg,在氯化钾中减重 9 mg,在溴化钾中减重 15 mg,如图 1,可求得其 Aw=0.878 +20 +10 -10 0.878 -20 0.924 0.901 0.842 0.807 KNO3 BaCl22H2O KCl KBr 图1 Aw 值测定图解

五、注意事项 1.每个样品测定时应作平行试验。其测定值的平行误差不得超过 0.02。 2.取样要在同一条件下进行,操作要迅速。 3.试样的大小和形状对测定结果影响不大。 4.康威氏微量扩散皿密封性要好。 5.取食品的固体或液体部分,样品平衡后其结果没有差异。 6.绝大多数样品可在 2 小时后测得 Aw 值,但米饭类、油脂类、油浸烟熏鱼类则需 4 天左右时间才能测定。因此,需加入样品量 0.2%的山梨酸防腐,并以山梨酸的水溶液作 空白。 实验三 食品中还原糖的测定 一、实验原理 样品经除去蛋白质后,在加热条件下,直接滴定标定过的碱性酒石酸铜液,以次甲基蓝 作指示剂,根据样品液消耗体积,计算还原糖量。 二、材料、试剂与仪器 ⒈ 碱性酒石酸铜甲液:称取 15g 硫酸铜(CuSO4·5H2O)及 0.05g 次甲基蓝,溶于水中 并稀释至 1000mL。 ⒉ 碱性酒石酸铜乙液:称取 50g 酒石酸钾钠及 75g 氢氧化钠,溶于水中,再加入 4g 亚铁氰化钾,完全溶解后,用水稀释至 1000mL,贮存于橡胶塞玻璃瓶内。 ⒊ 乙酸锌溶液:称取 21.9g 乙酸锌,加 3mL 冰乙酸,加水溶解并稀释至 100mL。 ⒋ 10.6%亚铁氰化钾溶液。 ⒌ 盐酸。 ⒍ 葡萄糖标准溶液:精密称取 1.00g 经过 98—100°C 干燥至恒量的纯葡萄糖,加水 溶解后加入 5mL 盐酸,并以水稀释至 1000mL。此溶液每毫升相当于 1mg 葡萄糖。 三、操作步骤 ⒈ 样品处理: (1) 乳类、乳制品及含蛋白质的冷食类:称取约 2.5-5g 固体样品(吸取 25-50mL 液体 样品),置于 250mL 容量瓶中,加 50mL 水,摇匀后慢慢加入 5mL 乙酸锌溶液及 5mL10.6%亚 铁氰化钾溶液,加水至刻度,混匀。静置 30min,用干燥滤纸过滤,弃去初滤液,滤液备用。 (2) 酒精性饮料:吸取 100mL 样品,置于蒸发皿中,用 1N 氢氧化钠溶液中和至中性, 在水浴上蒸发至原体积的 1/4 后,移入 250mL 容量瓶中。加 50mL 水,混匀。以下按⑴自“慢 慢加入 5mL 乙酸锌溶液及 5mL10.6%亚铁氰化钾溶液”起依法操作。 (3) 含多量淀粉的食品:称取 10-20g 样品,置于 250mL 容量瓶中,加 200mL 水,在 45℃ 水浴中加热 1h,并不时振摇。冷后加水至刻度,混匀,静置。吸取 200mL 上清液于另一 250mL 容量瓶中,以下按⑴自“慢慢加入 5mL 乙酸锌溶液及 5mL10.6%亚铁氰化钾溶液”起依法操 作。 (4) 汽水等含有二氧化碳的饮料:吸取 100mL 样品置于蒸发皿中,在水浴上除去二氧 化碳后,移入 250mL 容量瓶中,-并用水洗涤蒸发皿,洗液并入容量瓶中,再加水至刻度, 混匀后,备用。 ⒉ 标定碱性酒石酸铜溶液:吸取 5.0mL 碱性酒石酸铜甲液及 5.0mL 乙液,置于 150mL 锥形瓶中,加水 10mL,加入玻璃珠 2 粒,从滴定管滴加约 9mL 葡萄糖标准溶液,控制在 2min 内加热至沸,趁沸以每两秒 1 滴的速度继续滴加葡萄糖标准溶液,直至溶液蓝色刚好褪去为 终点,记录消耗葡萄糖标准溶的总体积,同时平行操作三份,取其平均值,计算每 10mL(甲、 乙液各 5mL)碱性酒石酸铜溶液相当于葡萄糖的质量(mg)。 ⒊ 样品溶液预测:吸取 5.0mL 碱性酒石酸铜甲液及 5.0 mL 乙液,置于 150 mL 锥形瓶
五、注意事项 1.每个样品测定时应作平行试验。其测定值的平行误差不得超过 0.02。 2.取样要在同一条件下进行,操作要迅速。 3.试样的大小和形状对测定结果影响不大。 4.康威氏微量扩散皿密封性要好。 5.取食品的固体或液体部分,样品平衡后其结果没有差异。 6.绝大多数样品可在 2 小时后测得 Aw 值,但米饭类、油脂类、油浸烟熏鱼类则需 4 天左右时间才能测定。因此,需加入样品量 0.2%的山梨酸防腐,并以山梨酸的水溶液作 空白。 实验三 食品中还原糖的测定 一、实验原理 样品经除去蛋白质后,在加热条件下,直接滴定标定过的碱性酒石酸铜液,以次甲基蓝 作指示剂,根据样品液消耗体积,计算还原糖量。 二、材料、试剂与仪器 ⒈ 碱性酒石酸铜甲液:称取 15g 硫酸铜(CuSO4·5H2O)及 0.05g 次甲基蓝,溶于水中 并稀释至 1000mL。 ⒉ 碱性酒石酸铜乙液:称取 50g 酒石酸钾钠及 75g 氢氧化钠,溶于水中,再加入 4g 亚铁氰化钾,完全溶解后,用水稀释至 1000mL,贮存于橡胶塞玻璃瓶内。 ⒊ 乙酸锌溶液:称取 21.9g 乙酸锌,加 3mL 冰乙酸,加水溶解并稀释至 100mL。 ⒋ 10.6%亚铁氰化钾溶液。 ⒌ 盐酸。 ⒍ 葡萄糖标准溶液:精密称取 1.00g 经过 98—100°C 干燥至恒量的纯葡萄糖,加水 溶解后加入 5mL 盐酸,并以水稀释至 1000mL。此溶液每毫升相当于 1mg 葡萄糖。 三、操作步骤 ⒈ 样品处理: (1) 乳类、乳制品及含蛋白质的冷食类:称取约 2.5-5g 固体样品(吸取 25-50mL 液体 样品),置于 250mL 容量瓶中,加 50mL 水,摇匀后慢慢加入 5mL 乙酸锌溶液及 5mL10.6%亚 铁氰化钾溶液,加水至刻度,混匀。静置 30min,用干燥滤纸过滤,弃去初滤液,滤液备用。 (2) 酒精性饮料:吸取 100mL 样品,置于蒸发皿中,用 1N 氢氧化钠溶液中和至中性, 在水浴上蒸发至原体积的 1/4 后,移入 250mL 容量瓶中。加 50mL 水,混匀。以下按⑴自“慢 慢加入 5mL 乙酸锌溶液及 5mL10.6%亚铁氰化钾溶液”起依法操作。 (3) 含多量淀粉的食品:称取 10-20g 样品,置于 250mL 容量瓶中,加 200mL 水,在 45℃ 水浴中加热 1h,并不时振摇。冷后加水至刻度,混匀,静置。吸取 200mL 上清液于另一 250mL 容量瓶中,以下按⑴自“慢慢加入 5mL 乙酸锌溶液及 5mL10.6%亚铁氰化钾溶液”起依法操 作。 (4) 汽水等含有二氧化碳的饮料:吸取 100mL 样品置于蒸发皿中,在水浴上除去二氧 化碳后,移入 250mL 容量瓶中,-并用水洗涤蒸发皿,洗液并入容量瓶中,再加水至刻度, 混匀后,备用。 ⒉ 标定碱性酒石酸铜溶液:吸取 5.0mL 碱性酒石酸铜甲液及 5.0mL 乙液,置于 150mL 锥形瓶中,加水 10mL,加入玻璃珠 2 粒,从滴定管滴加约 9mL 葡萄糖标准溶液,控制在 2min 内加热至沸,趁沸以每两秒 1 滴的速度继续滴加葡萄糖标准溶液,直至溶液蓝色刚好褪去为 终点,记录消耗葡萄糖标准溶的总体积,同时平行操作三份,取其平均值,计算每 10mL(甲、 乙液各 5mL)碱性酒石酸铜溶液相当于葡萄糖的质量(mg)。 ⒊ 样品溶液预测:吸取 5.0mL 碱性酒石酸铜甲液及 5.0 mL 乙液,置于 150 mL 锥形瓶

中,加水 10 mL,加入玻璃珠 2 粒,控制在 2min 内加热及沸,趁沸以先快后慢的速度,从 滴定管中滴加样品溶液,并保持溶液沸腾状态,待溶液颜色变浅时,以每两秒 1 滴的速度滴 定,直至溶液蓝色刚好褪去为终点,记录样液消耗体积。 ⒋ 样品溶液测定:吸取 5.0 mL 碱性酒石酸铜甲液及 5.0 mL 乙液,置于 150 mL 锥形瓶 中,加水 10 mL,加入玻璃珠 2 粒,从滴定管滴加比预测体积少 1 mL 的样品溶液,使在 2min 内加热至沸,趁沸继续以每两秒 1 滴的速度滴定,直至蓝色刚好褪去为终点,记录样液消耗 体积,同法平行操作三份,得出平均消耗体积。 四、结果计算 m3 X3= ×100 V2 m4× ×1000 250 式中:X3——样品中还原糖的含量(以葡萄糖计),%; m3——10mL 碱性酒石酸铜溶液(甲、乙液各 5 mL)相当于还原糖(以葡萄计)的质 量,mg; m4-样品质量或体积,g 或 mL; V2——测定时平均消耗样品溶液体积,mL; 250 为样品溶液总体积, mL。 五﹑注意事项 1.此法有称快速法,适合于各类食品中还原糖的测定,是国家标准分析法。 2.此实验应严格遵守操作步骤及条件的准确一致性(如加热时间,滴定时的条件与速度 等),以减少操作中产生的误差。 实验四 食品中蔗糖的测定 一、实验原理 样品经除去蛋白质后,其中蔗糖经盐酸水解转化为还原糖,再按还原糖测定。水解前后 还原糖的差值为蔗糖含量。 二、材料、试剂与仪器 ⒈ 试剂 (1)6mol/L 盐酸: 量取 50 mL 盐酸加水稀释至 100 mL; (2)甲基红指标液: 0.1%乙醇溶液; (3)20%氢氧化钠溶液; 其余试剂同前面食品中还原糖的测定中的试剂。 2. 仪器 同食品中还原糖的测定中的仪器 三、操作步骤 吸取 2 份 50 mL 按测定还原糖方法中制备样品处理液,置于 100 mL 容量瓶中,一份加 5mL6mol/L 盐酸,在 68—70℃水浴中加热 15min,冷后加 2 滴甲基红指标液,用 20%氢氧化 钠溶液中和至中性,加水至刻度,混匀。另一份直接加水稀释至 100 mL,按测定还原糖的 方法分别测定还原糖。 四、结果计算 X=(R2—R1)×0.95 式中:X——样品中蔗糖含量,%; R2——水解处理后还原糖含量,%; R1——不经水解处理还原糖含量,%;
中,加水 10 mL,加入玻璃珠 2 粒,控制在 2min 内加热及沸,趁沸以先快后慢的速度,从 滴定管中滴加样品溶液,并保持溶液沸腾状态,待溶液颜色变浅时,以每两秒 1 滴的速度滴 定,直至溶液蓝色刚好褪去为终点,记录样液消耗体积。 ⒋ 样品溶液测定:吸取 5.0 mL 碱性酒石酸铜甲液及 5.0 mL 乙液,置于 150 mL 锥形瓶 中,加水 10 mL,加入玻璃珠 2 粒,从滴定管滴加比预测体积少 1 mL 的样品溶液,使在 2min 内加热至沸,趁沸继续以每两秒 1 滴的速度滴定,直至蓝色刚好褪去为终点,记录样液消耗 体积,同法平行操作三份,得出平均消耗体积。 四、结果计算 m3 X3= ×100 V2 m4× ×1000 250 式中:X3——样品中还原糖的含量(以葡萄糖计),%; m3——10mL 碱性酒石酸铜溶液(甲、乙液各 5 mL)相当于还原糖(以葡萄计)的质 量,mg; m4-样品质量或体积,g 或 mL; V2——测定时平均消耗样品溶液体积,mL; 250 为样品溶液总体积, mL。 五﹑注意事项 1.此法有称快速法,适合于各类食品中还原糖的测定,是国家标准分析法。 2.此实验应严格遵守操作步骤及条件的准确一致性(如加热时间,滴定时的条件与速度 等),以减少操作中产生的误差。 实验四 食品中蔗糖的测定 一、实验原理 样品经除去蛋白质后,其中蔗糖经盐酸水解转化为还原糖,再按还原糖测定。水解前后 还原糖的差值为蔗糖含量。 二、材料、试剂与仪器 ⒈ 试剂 (1)6mol/L 盐酸: 量取 50 mL 盐酸加水稀释至 100 mL; (2)甲基红指标液: 0.1%乙醇溶液; (3)20%氢氧化钠溶液; 其余试剂同前面食品中还原糖的测定中的试剂。 2. 仪器 同食品中还原糖的测定中的仪器 三、操作步骤 吸取 2 份 50 mL 按测定还原糖方法中制备样品处理液,置于 100 mL 容量瓶中,一份加 5mL6mol/L 盐酸,在 68—70℃水浴中加热 15min,冷后加 2 滴甲基红指标液,用 20%氢氧化 钠溶液中和至中性,加水至刻度,混匀。另一份直接加水稀释至 100 mL,按测定还原糖的 方法分别测定还原糖。 四、结果计算 X=(R2—R1)×0.95 式中:X——样品中蔗糖含量,%; R2——水解处理后还原糖含量,%; R1——不经水解处理还原糖含量,%;

0.95——还原糖(以葡萄糖计)换算为蔗糖的系数。 第一法 酶水解法 一、实验原理 样品经除去脂肪及可溶性糖类后,其中淀粉用淀粉酶水解成双糖,再用盐酸将双糖水解 成单糖,最后按还原糖测定,并折算成淀粉。 二、材料 试剂与仪器 ⒈ 0.5%淀粉酶溶液:称取淀粉酶 0.5g,加 100mL 水溶解,加入数滴甲苯或三氯甲烷, 防止长霉,贮于冰箱中。 ⒉ 碘溶液:称取 3.6g 碘化钾溶于 20 mL 水中,加入 1.3g 碘,溶解后加水稀释至 100mL。 ⒊ 乙醚 ⒋ 85%乙醇。 其余试剂同食品中蔗糖的测定中试剂。 三、操作步骤 ⒈ 样品处理 称取 2~5 样品,置于放有折叠滤纸的漏斗内,先用 50 mL 乙醚分别次洗除脂肪,再用 约 100mL85%乙醇洗去可溶性糖类,将残留物移入 250mL 烧杯内,并用 50mL 水洗滤纸及漏斗, 洗液并入烧杯内,将烧杯置沸水浴上加热 15min,使淀粉糊化,放冷至 60℃以下,加 20 mL 淀粉酶溶液,在 55~60℃保温 1h,并时时搅拌。然后取 1 滴此液加 1 滴碘溶液,应不显现 蓝色,若显蓝色,再加热糊化并加 20mL 淀粉酶溶液,继续保温,直至加碘不显蓝色为止。 加热至沸,冷后移入 250mL 容量瓶中,并加水至刻度,温匀,过滤,弃去初滤液。取 50 mL 滤液,置于 250 mL 锥形瓶中,加 5 mL6N 盐酸,装上回流冷凝器,在沸水浴中回流 1h,冷 后加 2 滴甲基红指示液,用 20%氢氧化钠溶液中和至中性,溶液转入 100 mL 容量瓶中,洗 剂锥形瓶,洗液并入 100 mL 容量瓶中,加水至刻度,混匀备用。 ⒉ 测定 按食品中还原糖的测定方法操作。同时量取 50 mL 水及与样品处理时相同量的淀粉酶溶 液,按同一方法做试剂空白试验。 四、结果计算 (A1-A2)×0.9 X1= ×100 50 V1 m1× × × 1000 250 100 式中:X1——样品中淀粉的含量,%; A1——测定用样品中还原糖的含量,mg; A2——试剂空白中还原糖的含量,mg; 0.9——还原糖(以葡萄糖计)换算成淀粉的换算系数; m1——称取样品质量,g; V1——测定用样品处理液的体积,mL。 第二法 酸水解法 一、实验原理 样品经除去脂肪及可溶性糖类后,其中淀粉用酸水解成具有还原性的单糖,然后按还原 糖测定,并折算成淀粉。 二、材料、试剂与仪器 ⒈ 试剂 ⑴乙醚 ⑵85%乙醇溶液。 ⑶6mol/L 盐酸溶液。 ⑷40%氢氧化钠溶液
0.95——还原糖(以葡萄糖计)换算为蔗糖的系数。 第一法 酶水解法 一、实验原理 样品经除去脂肪及可溶性糖类后,其中淀粉用淀粉酶水解成双糖,再用盐酸将双糖水解 成单糖,最后按还原糖测定,并折算成淀粉。 二、材料 试剂与仪器 ⒈ 0.5%淀粉酶溶液:称取淀粉酶 0.5g,加 100mL 水溶解,加入数滴甲苯或三氯甲烷, 防止长霉,贮于冰箱中。 ⒉ 碘溶液:称取 3.6g 碘化钾溶于 20 mL 水中,加入 1.3g 碘,溶解后加水稀释至 100mL。 ⒊ 乙醚 ⒋ 85%乙醇。 其余试剂同食品中蔗糖的测定中试剂。 三、操作步骤 ⒈ 样品处理 称取 2~5 样品,置于放有折叠滤纸的漏斗内,先用 50 mL 乙醚分别次洗除脂肪,再用 约 100mL85%乙醇洗去可溶性糖类,将残留物移入 250mL 烧杯内,并用 50mL 水洗滤纸及漏斗, 洗液并入烧杯内,将烧杯置沸水浴上加热 15min,使淀粉糊化,放冷至 60℃以下,加 20 mL 淀粉酶溶液,在 55~60℃保温 1h,并时时搅拌。然后取 1 滴此液加 1 滴碘溶液,应不显现 蓝色,若显蓝色,再加热糊化并加 20mL 淀粉酶溶液,继续保温,直至加碘不显蓝色为止。 加热至沸,冷后移入 250mL 容量瓶中,并加水至刻度,温匀,过滤,弃去初滤液。取 50 mL 滤液,置于 250 mL 锥形瓶中,加 5 mL6N 盐酸,装上回流冷凝器,在沸水浴中回流 1h,冷 后加 2 滴甲基红指示液,用 20%氢氧化钠溶液中和至中性,溶液转入 100 mL 容量瓶中,洗 剂锥形瓶,洗液并入 100 mL 容量瓶中,加水至刻度,混匀备用。 ⒉ 测定 按食品中还原糖的测定方法操作。同时量取 50 mL 水及与样品处理时相同量的淀粉酶溶 液,按同一方法做试剂空白试验。 四、结果计算 (A1-A2)×0.9 X1= ×100 50 V1 m1× × × 1000 250 100 式中:X1——样品中淀粉的含量,%; A1——测定用样品中还原糖的含量,mg; A2——试剂空白中还原糖的含量,mg; 0.9——还原糖(以葡萄糖计)换算成淀粉的换算系数; m1——称取样品质量,g; V1——测定用样品处理液的体积,mL。 第二法 酸水解法 一、实验原理 样品经除去脂肪及可溶性糖类后,其中淀粉用酸水解成具有还原性的单糖,然后按还原 糖测定,并折算成淀粉。 二、材料、试剂与仪器 ⒈ 试剂 ⑴乙醚 ⑵85%乙醇溶液。 ⑶6mol/L 盐酸溶液。 ⑷40%氢氧化钠溶液

⑸10%氢氧化钠溶液。 ⑹甲基红指示液:0.2%乙醇溶液。 ⑺精密 PH 试纸。 ⑻20%乙酸铅溶液。 ⑼10%硫酸钠溶液。 其余试剂同还原糖测定试剂。 ⒉ 仪器 水浴锅;1200r/min 高速组织捣碎机;皂化装置并附 250 mL 锥形瓶。 三、操作步骤 1 样品处理 (1) 粮食、豆类、糕点、饼干等较干燥的样品:称取 2.0—5.0g 磨碎过 40 目筛的样品, 置于放有慢速滤纸的漏斗中,用 30 mL 乙醚分三次洗去样品中脂肪,弃去乙醚。再用 150 mL85% 乙醇溶液分数次洗涤残渣,除去可溶性糖类物质。并滤干乙醇溶液,以 100 mL 水洗涤漏斗 中残渣并转移至 250 mL 锥形瓶中,加入 30 mL6mol/L 盐酸,接好冷凝管,置沸水浴中回流 2h。回流完毕后,立即置流水中冷却。待样品水解液冷却后,加入 2 滴甲基红指示液,先以 40%氢氧化钠溶液调至黄色,再以 6mol/L 盐酸校正至水解液刚变成红色为宜。若水解液颜色 较深,可用精密 PH 试纸测试,使样品水解液的 PH 约为 7。然后加 20 mL20%乙酸铅溶液,摇 匀,放置 10min。再加 20 mL10%硫酸钠溶液,以除去过多的铅。摇匀后将全部溶液及残渣转 入 500 mL 容量瓶中,用水洗涤锥形瓶,洗液合并于容量瓶中,加水稀释至刻度。过滤,弃 去初滤液 20 mL,滤液供测定用。 (2) 蔬菜、水果、各种粮豆含水熟食制品:按 1:1 加水在组织捣碎机中捣成匀浆(蔬 菜、水果需先洗净、晾干,取可食部分)。称取 5~10g 匀浆(液体样品可直接量取),于 250 mL 锥形瓶中,加 30 mL 乙醚振摇提取(除去样品中脂肪),用滤纸过滤除去乙醚,再用 30 mL 乙醚淋洗两次,弃去乙醚。以下按⑴自“再用 15 0mL85%乙醇溶液”起依法操作。 2 测定 按测定还原糖的方法操作。 四、结果计算 (A3-A4) × 0.9 X2= × 100 V2 m2× × 1000 500 式中:X2——样品中淀粉含量,%; A3——测定用样品中水解液中还原糖含量,mg; A4——试剂空白中还原糖的含量,mg; m2——样品质量,g; V2——测定用样品水解液体积,mL; 500——样品液总体积; 0.9——还原糖折算成淀粉的换算系数。 实验五 食品淀粉的测定 酶比色法 一、原理 淀粉在淀粉葡萄糖苷酶(AGS)催化下,最终水解为葡萄糖。葡萄糖氧化酶(GOD)在有
⑸10%氢氧化钠溶液。 ⑹甲基红指示液:0.2%乙醇溶液。 ⑺精密 PH 试纸。 ⑻20%乙酸铅溶液。 ⑼10%硫酸钠溶液。 其余试剂同还原糖测定试剂。 ⒉ 仪器 水浴锅;1200r/min 高速组织捣碎机;皂化装置并附 250 mL 锥形瓶。 三、操作步骤 1 样品处理 (1) 粮食、豆类、糕点、饼干等较干燥的样品:称取 2.0—5.0g 磨碎过 40 目筛的样品, 置于放有慢速滤纸的漏斗中,用 30 mL 乙醚分三次洗去样品中脂肪,弃去乙醚。再用 150 mL85% 乙醇溶液分数次洗涤残渣,除去可溶性糖类物质。并滤干乙醇溶液,以 100 mL 水洗涤漏斗 中残渣并转移至 250 mL 锥形瓶中,加入 30 mL6mol/L 盐酸,接好冷凝管,置沸水浴中回流 2h。回流完毕后,立即置流水中冷却。待样品水解液冷却后,加入 2 滴甲基红指示液,先以 40%氢氧化钠溶液调至黄色,再以 6mol/L 盐酸校正至水解液刚变成红色为宜。若水解液颜色 较深,可用精密 PH 试纸测试,使样品水解液的 PH 约为 7。然后加 20 mL20%乙酸铅溶液,摇 匀,放置 10min。再加 20 mL10%硫酸钠溶液,以除去过多的铅。摇匀后将全部溶液及残渣转 入 500 mL 容量瓶中,用水洗涤锥形瓶,洗液合并于容量瓶中,加水稀释至刻度。过滤,弃 去初滤液 20 mL,滤液供测定用。 (2) 蔬菜、水果、各种粮豆含水熟食制品:按 1:1 加水在组织捣碎机中捣成匀浆(蔬 菜、水果需先洗净、晾干,取可食部分)。称取 5~10g 匀浆(液体样品可直接量取),于 250 mL 锥形瓶中,加 30 mL 乙醚振摇提取(除去样品中脂肪),用滤纸过滤除去乙醚,再用 30 mL 乙醚淋洗两次,弃去乙醚。以下按⑴自“再用 15 0mL85%乙醇溶液”起依法操作。 2 测定 按测定还原糖的方法操作。 四、结果计算 (A3-A4) × 0.9 X2= × 100 V2 m2× × 1000 500 式中:X2——样品中淀粉含量,%; A3——测定用样品中水解液中还原糖含量,mg; A4——试剂空白中还原糖的含量,mg; m2——样品质量,g; V2——测定用样品水解液体积,mL; 500——样品液总体积; 0.9——还原糖折算成淀粉的换算系数。 实验五 食品淀粉的测定 酶比色法 一、原理 淀粉在淀粉葡萄糖苷酶(AGS)催化下,最终水解为葡萄糖。葡萄糖氧化酶(GOD)在有