
第10章膜分离667 1.3.3非对称性膜 其特点是膜的断面不对称。它是由起膜分离作用的表面活性层(0.2~0.5 m)和起支撑强化作用的多孔支撑层(5001000m)构成。多孔支撑层孔径 很大,对透过流体无阻力。由于非对称性膜起分离作用的表面活性层很薄,孔径 微细,因此透过量大,膜孔不易堵塞,容易清洗。目前的超滤和反渗透膜多为非 对称性膜。 图[10-1(a)]所示的非对称性膜为指状结构,多用于超滤,而反渗透膜的 结构多为海绵状,如图[10-1(b)]所示。 表面活性层 惰性层 (a)指状结构 b)海绵状结构 图10-1非对称性膜面结构示意图 1.3.4离子交换膜 是一种带电基团的聚合膜,分阳离子交换膜和阴离子交换膜两种。阳离子交 换膜带有阳离子交换基团,带负电荷,能选择性地吸附阳离子并使其通过,对阴 离子则产生排斥作用。与之相反,阴离子交换膜带有阴离子交换基团,带正电 荷,能选择性地吸附阴离子,并使之通过。离子交换膜主要用于电渗析。常用的 有聚乙烯膜或聚氯乙烯膜。阳离子交换基团有磺酸型和磷酸型,阴离子交换基团 有季胺、叔胺和仲胺等。 1.4膜性能 膜性能包括膜的分离透过性和物化稳定性。 膜的物化稳定性是指膜的强度,适用的压力、温度、pH值以及对有机溶剂

668食品工程原理 和各种化学药品的耐受性,这是决定膜使用寿命的主要因素。 膜的分离透过性包括分离效率、渗透通量和通量衰减系数3个方面。 1.4.1分离效率 对于不同的膜分离过程和分离对象可以用不同的表示方法。对于溶液脱盐或 除去混合液中的微粒和高分子物质等可以用表观截留率R和实际截留率R表示。 R=1-Cp (10-1) Ch R=1- (10-2) 式中:cb、cp、cw分别为料液、透过液、膜表面上溶质的质量浓度。 1.4.2渗透通量 用单位时间内通过单位膜面积的透过物量表示。 1.4.3通量衰减系数 由于浓差极化、膜压实及膜污染等原因,膜的渗透通量将随时间的延长而减 小。渗透通量与时间的关系可以用下式来表示: Je=Jo0m (10-3) 式中:J。为初始时刻的渗透通量;J。为时间0时的渗透通量;m为衰减系数。 本章将重点介绍反渗透、超滤和电渗析这3种目前在食品工业中已得到广泛 应用的膜分离过程。 2 反渗透 2.1 反渗透的基本原理 渗透是由于化学位梯度的存在而弓引起的自发扩散现象,如图10-2(a)所示

第10幸膜分离669 我们将纯水与盐水用一张能透过水的半透膜隔开,在一定温度和压强下,纯水的 化学位大于溶液中水的化学位,在化学位梯度的作用下,纯水透过膜向盐水侧渗 透,使盐水侧液位升高。 当水位提高到h时[如图10-2(b)示],盐水侧的压力与纯水侧压力之差 等于渗透压π。此时渗透过程达到平衡,水的渗透通量为零。 如果在盐水侧加压[如图10-2(c)所示],使盐水侧与纯水侧的压差大于 渗透压π,则水将反向从盐水侧透过半透膜流向纯水侧,这一过程就称为反渗 透。 外加压强尸 纯水 纯水 纯水 半透 半透膜 半透膜 a (b) (c) 图10-2渗透与反渗透现象 根据化学热力学的基本理论可以推导出理想稀溶液的渗透压公式: (10-4) 式中ct为溶液中溶质i的浓度,mol/m3。 10-4式称为理想溶液渗透压的Van't Hoff公式。 由Van'tHof渗透压公式可知,溶液的浓度越高,π值越大。因此,在 反渗透过程中所施加的实际操作压力,应在系统和膜强度允许的范围内, 远大于按Van't Hoff渗透压公式算出的溶液的π值,一般为π值的几倍到近十 倍。 Van't Hoff渗透压公式只适用于理想溶液。对实际溶液需引入一校正因数 中:
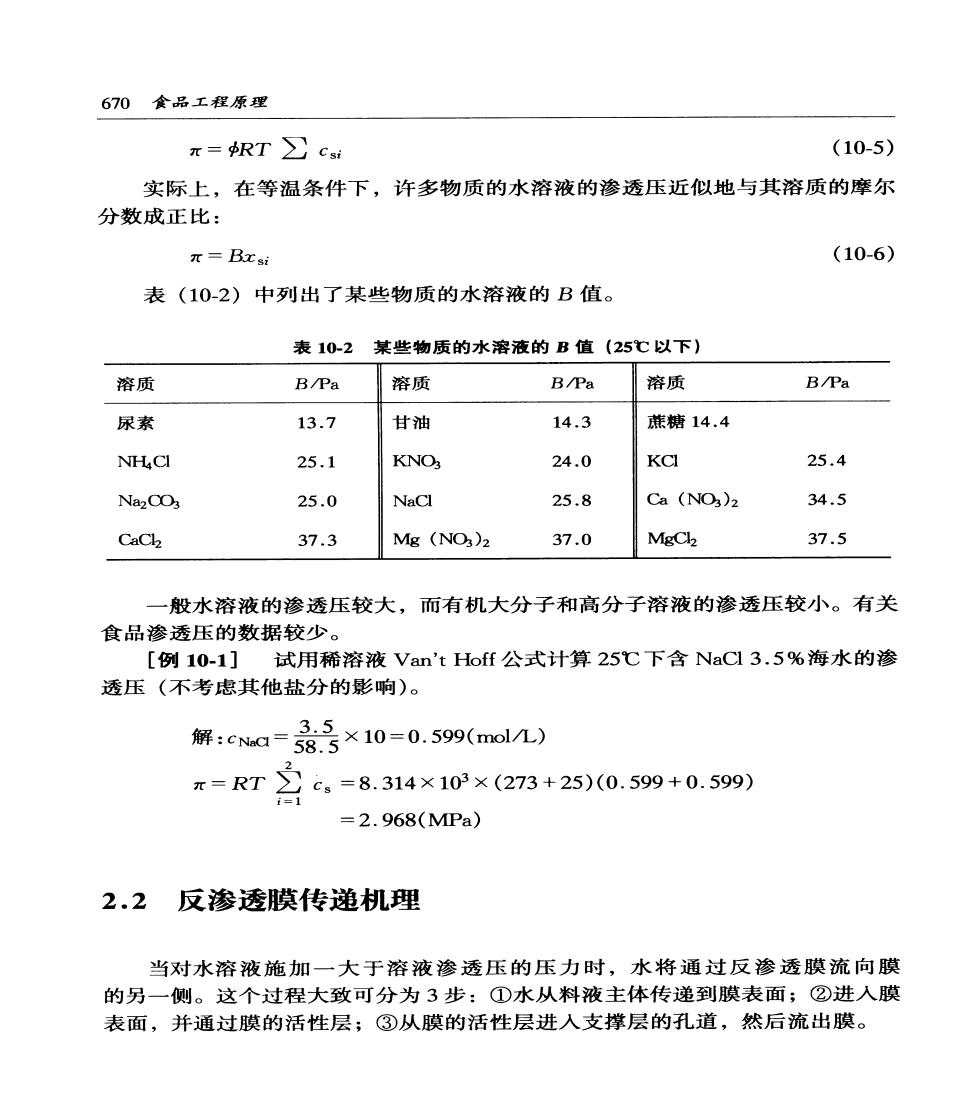
670食品工程原理 r=RT∑ct (10-5) 实际上,在等温条件下,许多物质的水溶液的渗透压近似地与其溶质的摩尔 分数成正比: x=Bxsi (10-6) 表(10-2)中列出了某些物质的水溶液的B值。 表10-2某些物质的水溶液的B值(25℃以下) 溶质 B/Pa 溶质 B/Pa 溶质 B/Pa 尿素 13.7 甘油 14.3 蔗糖14.4 NHCI 25.1 KNO3 24.0 KCl 25.4 Na2CO3 25.0 NaCl 25.8 Ca (NO3)2 34.5 CaCk2 37.3 Mg (NO3)2 37.0 MgCk 37.5 一般水溶液的渗透压较大,而有机大分子和高分子溶液的渗透压较小。有关 食品渗透压的数据较少。 [例10-1]试用稀溶液Van't Hoff公式计算25℃下含NaCl3.5%海水的渗 透压(不考虑其他盐分的影响)。 3.5 解:cNa=58.号3×10=0.599(molM) T=RT2c,=8.314×103×(273+25)(0.599+0.59) =1 =2.968(MPa) 2.2反渗透膜传递机理 当对水溶液施加一大于溶液渗透压的压力时,水将通过反渗透膜流向膜 的另一侧。这个过程大致可分为3步:①水从料液主体传递到膜表面;②进入膜 表面,并通过膜的活性层;③从膜的活性层进人支撑层的孔道,然后流出膜
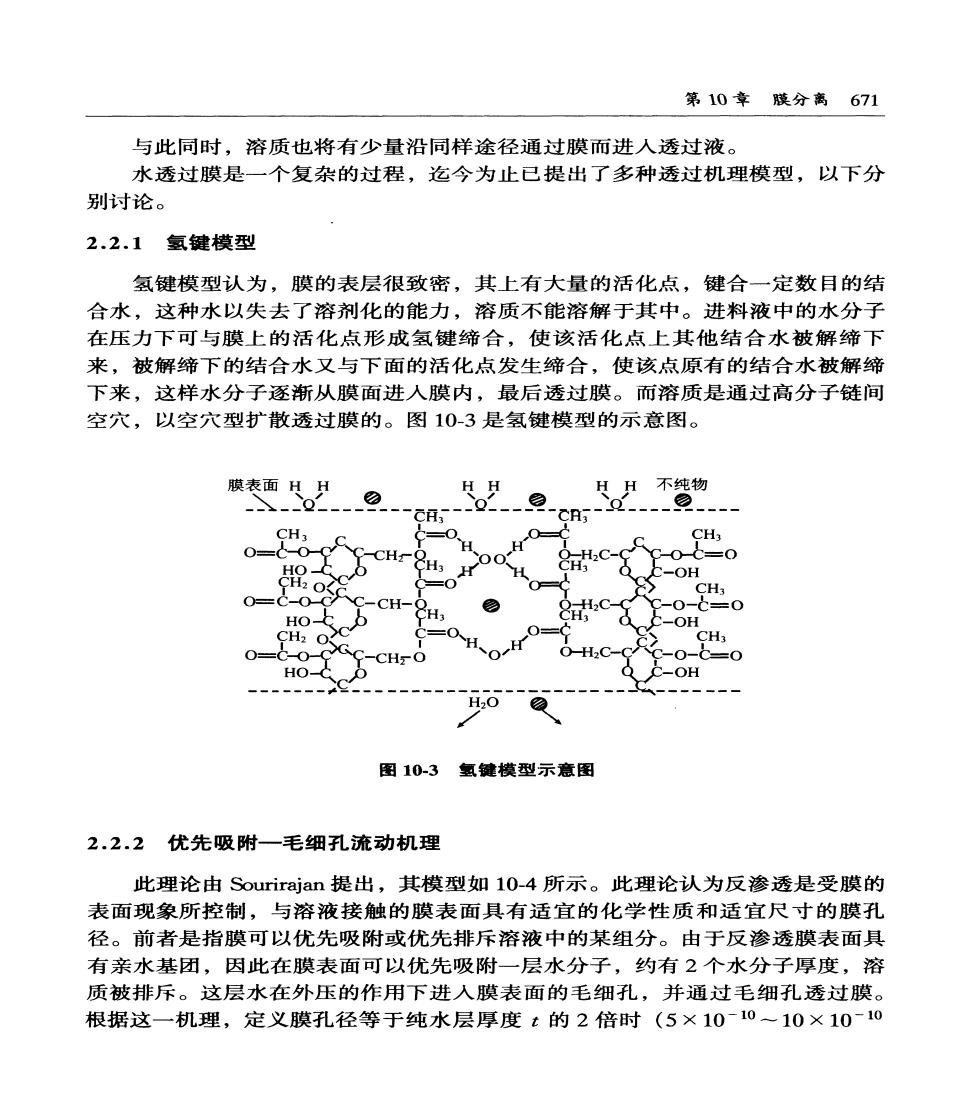
第10章膜分离671 与此同时,溶质也将有少量沿同样途径通过膜而进入透过液。 水透过膜是一个复杂的过程,迄今为止已提出了多种透过机理模型,以下分 别讨论。 2.2.1氢键模型 氢键模型认为,膜的表层很致密,其上有大量的活化点,键合一定数目的结 合水,这种水以失去了溶剂化的能力,溶质不能溶解于其中。进料液中的水分子 在压力下可与膜上的活化点形成氢键缔合,使该活化点上其他结合水被解缔下 来,被解缔下的结合水又与下面的活化点发生缔合,使该点原有的结合水被解缔 下来,这样水分子逐渐从膜面进人膜内,最后透过膜。而溶质是通过高分子链间 空穴,以空穴型扩散透过膜的。图10-3是氢键模型的示意图。 膜表面HH HH不纯物 c,- CH3 0=( CH3 -CH 0 =0 H C-OH CH3 CH- 12 H30 H 12 O HO -OH H202 图10-3氢键模型示意图 2.2.2优先吸附一毛细孔流动机理 此理论由Sourirajan提出,其模型如l0-4所示。此理论认为反渗透是受膜的 表面现象所控制,与溶液接触的膜表面具有适宜的化学性质和适宜尺寸的膜孔 径。前者是指膜可以优先吸附或优先排斥溶液中的某组分。由于反渗透膜表面具 有亲水基团,因此在膜表面可以优先吸附一层水分子,约有2个水分子厚度,溶 质被排斥。这层水在外压的作用下进入膜表面的毛细孔,并通过毛细孔透过膜。 根据这一机理,定义膜孔径等于纯水层厚度t的2倍时(5×1010~10×10~10