
第9章新型无机材料工艺与技术 内容提要 随着时代的发展,工业生产各部门对材料的种类和性能不断提出新的要求。而科学技 术的进步,使得材料制备新工艺不断出现,对材料科学的某些现象的认识不断加深。在此 基础上,人们又利用新技术和新知识去合成新的材料。新材料通常是其结构和性能在制造 过程中得到精确控制的材料,能满足某些尖端技术领域的特殊要求。因此,新材料和材料 合成新技术在科学技术领域和国民经济的发展中占有重要地位。 近几十年来,无机材料合成新技术不断出现,如溶胶-凝胶合成技术、水热与溶剂热合 成技术、物理气相沉积技术、化学气相沉积技术、微波等离子体合成技术、自蔓延高温合成 技术、仿生合成技术等。这些技术大致分为材料合成新技术和材料表面处理新技术,其中有 些技术既是合成新技术,又是表面处理新技术,如溶胶-凝胶技术、化学气相沉积技术等。 无机材料合成新技术中,溶胶-凝胶合成技术、物理气相沉积技术、化学气相沉积技术 发展较快,也比较成熟,应用较广,本章扼要介绍了溶胶-凝胶法的工艺原理及影响因素、 溶胶-凝胶技术在材料合成方面的应用,物理气相沉积技术制备材料的主要工艺方法,化学 气相沉积工艺及其在无机材料制备中的应用等。另外,许多新材料是多物相的、其性能是 经过材料中的不同的物相协同优化的复合材料。材料复合技术涉及到的内容非常广泛,包 括材料体系、复合方法及其应用等,本章有选择地介绍了有关陶瓷基复合材料、金属陶瓷、 水泥基复合材料、碳纤维增强碳复合材料和纳米复合材料等材料复合新技术及新型复合材 料方面的内容。 9.1溶胶-凝胶技术 溶胶是由粒径在1~100nm之间的固体颗粒分散于液体介质中所形成的多相体系。其中 的固体颗粒一般由10~10个原子组成,称为胶体。当溶胶受到温度变化、扰动、化学反 应或电化学平衡等因素的作用,其黏度增大到一定程度时,溶胶将转变为一种介于液态和 固态之间的物质,即凝胶。在凝胶中,胶粒聚集成为三维网络,并网络了部分或全部介质。 所谓溶胶-凝胶技术,是指以无机化合物或金属有机化合物为前驱物,经溶液、溶胶、凝胶 而固化,在溶胶或凝胶状态下成型,再经干燥、热处理转化为氧化物或其他固体材料的方 法,是基于胶体化学原理制备材料的湿化学方法。 在20世纪30年代,Geffcken等利用金属醇盐水解和凝胶化制备了氧化物薄膜。1971 年Dislich利用该法制备了SiO2-B2O3-Al2O3-Na2O-K2O系玻璃,自此以后该法受到材料学界 的重视。20世纪80年代以来,溶胶-凝胶法应用于超微粉体、纤维、薄膜、块体材料的合成 以及光学、电学、装饰等功能材料的研究,成为一种受到普遍重视的无机材料制备新技术。 9.1.1溶胶-凝胶法分类 按形成溶胶-凝胶的物理化学过程来分,溶胶-凝胶法可分为传统胶体法、水解-聚合法 和配合物法三种,如表9-1所示。传统胶体法常用于制备粉体、薄膜,但也能制备块体材 料,如重达几千克、长1m以上的光纤预制棒;水解-聚合法以金属盐,特别是可溶于醇的 金属醇盐为前驱物,其溶胶-凝胶过程易于控制,能从溶胶、凝胶出发制成不同形态的材料。 由于具有较多的优点,溶胶-凝胶法的研究和应用一直以该法为主。不过许多低价(<4价) l
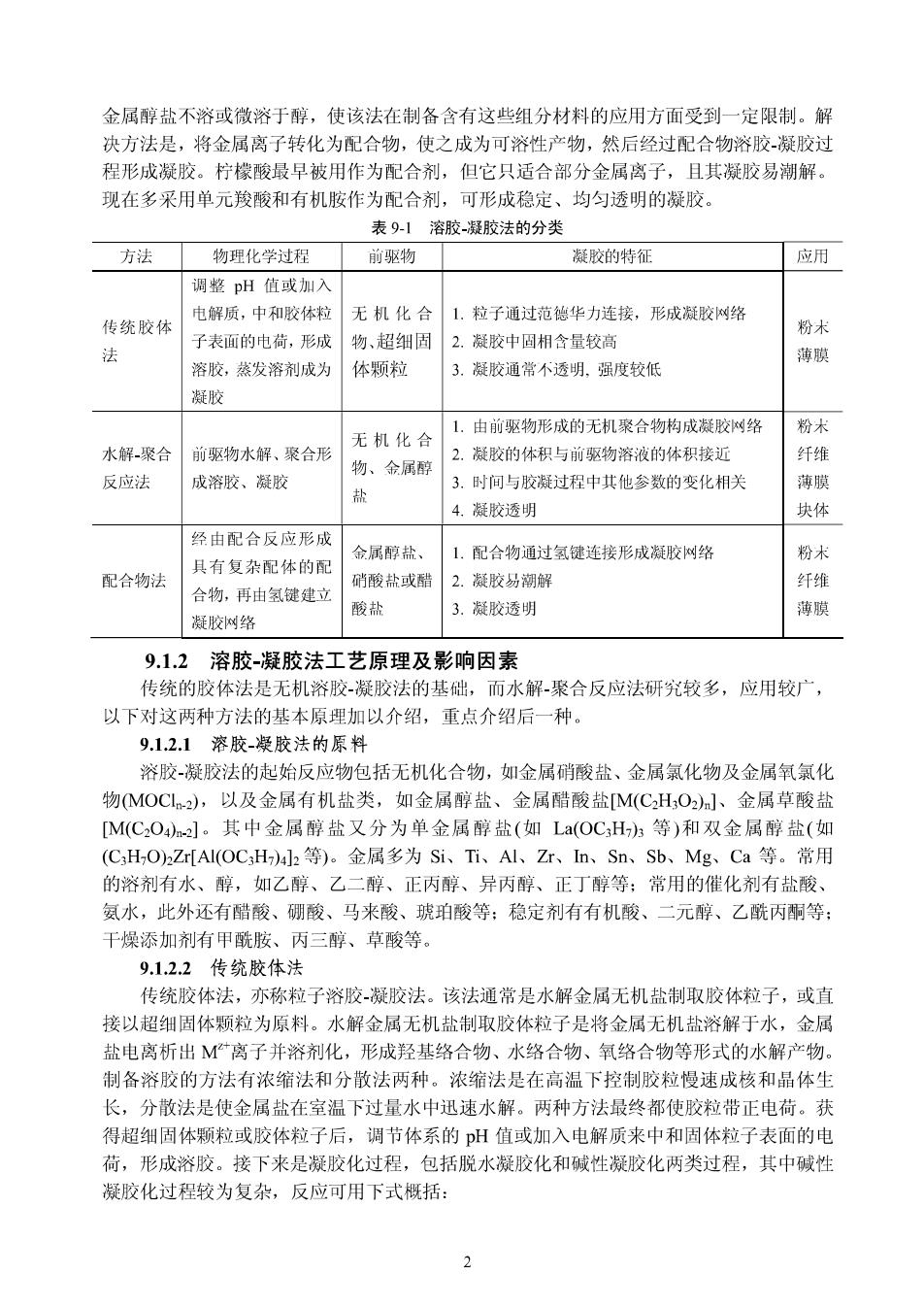
金属醇盐不溶或微溶于醇,使该法在制备含有这些组分材料的应用方面受到一定限制。解 决方法是,将金属离子转化为配合物,使之成为可溶性产物,然后经过配合物溶胶-凝胶过 程形成凝胶。柠檬酸最早被用作为配合剂,但它只适合部分金属离子,且其凝胶易潮解。 现在多采用单元羧酸和有机胺作为配合剂,可形成稳定、均匀透明的凝胶。 表9-1溶胶凝胶法的分类 方法 物甲化学村积 前驱物 凝胶的特征 应用 调整pH值或加入 电解质,中和胶体粒 无机化合1.粒子通过范他华力连接,形成搿胶络 传统胶体 子表面的电荷,形成 物、超细固2.凝胶中周相含量较高 粉术 法 薄膜 溶胶,鉴发溶剂成为 休颗粒 3.凝胶通常不透明,强度较低 健胶 无机化合 1.由前驱物形成的无机聚合物构成凝胶网络 粉术 水解聚合 前驱物水解、聚合形 2,凝胶的体积与前物溶液的体积接近 纤维 物、金尿翻 反应法 成溶胶、凝胶 3.时间与胶凝过程中其他参数的变化相关 薄膜 4.凝胶透明 块体 经由配合反应形成 金属醇盐、 1.配合物通过氢键连接形成凝胶网络 粉术 且右复杂配体的配 配合物法 硝磅盐或耐 2.解胶易潮解 纤维 合物,再由氢健建立 酸盐 3.凝胶透明 薄膜 凝胶网络 9.1.2 溶胶凝胶法工艺原理及影响因素 传统的胶体法是无机溶胶-凝胶法的基础,而水解聚合反应法研究较多,应用较广, 以下对这两种方法的基本原理加以介绍,重点介绍后一种。 9.1.2.1溶胶-凝胶法的原料 浴胶凝胶法的起始反应物包括无机化合物,如金属硝酸盐、金属氯化物及金属氧氯化 物MOC),以及金属有机盐类,如金属醇盐、金属醋酸盐M(C2HO2)]、金属草酸盐 [M(CO4)a-2]。其中金属醇盐又分为单金属醇盐(如La(OCH等)和双金属醇盐(如 (C,H,OzHAlOc:H-)al,等)。金属多为Si、Ti、AI、Zr、In、Sn、Sb、Mg、Ca等。常用 的溶剂有水、醇,如乙醇、乙二醇、正丙醇、异丙醇、正丁醇等:常用的催化剂有盐酸、 氨水,此外还有醋酸、硼酸、马来酸、號珀酸等:稳定剂有有机酸、二元醇、乙酰丙酮等: 干燥添加剂有甲酰胺、丙三醇、草酸等。 9.12.2传统胶体法 传统胶体法,亦称粒子溶胶凝胶法。该法通常是水解金属无机盐制取胶体粒子,或直 接以超细固体颗粒为原料。水解金属无机盐制取胶体粒子是将金属无机盐溶解于水,金属 盐电离析出M离子并溶剂化,形成羟基络合物、水络合物、氧络合物等形式的水解产物。 制备溶胶的方法有浓缩法和分散法两种。浓缩法是在高温下控制胶粒慢速成核和晶体生 长,分散法是使金属盐在室温下过量水中迅速水解。两种方法最终都使胶粒带正电荷。获 得超细固体颗粒或胶体粒子后,调节体系的pH值或加入电解质来中和固体粒子表面的电 荷,形成浴胶。接下来是凝胶化过程,包括脱水凝胶化和碱性凝胶化两类过程,其中碱性 凝胶化过程较为复杂,反应可用下式概括: 2

xM(H.O)+y+aAM.O.(OHD-2(H:O)A.+(x+u-n)H.O 式中A为胶浴过程中所加入的酸根离子。水解产物通过羟桥(M-OH-M)作用或氧桥 (M-OM)作用发生缩聚反应。当x=1时,形成单核聚合物:x>1时,形成多核聚合物。 胶体粒子交联聚集成网状结构后,即体系凝胶化后,再进行凝胶的干燥、干燥胶的热处理, 以制备所需的材料。 9.1.23水解-录合反应法 水解聚合反应法包括无机盐水解聚合反应法和金属醇盐水解聚合反应法,常用的是后者 A无机盐水解聚合反应法 无机盐溶解在纯水中时,阳离子M首先与偶极水分子发生溶剂化反应,生成水合 离子MHO)2,水合阳离子水解生成[MHO-1(OH,并放出质子H。多数情况下, 在水解的同时,有聚合反应发生,金属离子会与水、羟基(O、氧基(O)形成水配合物 羟基配合物、氧配合物等。在一定条件下,这些配合物可通过不同方式聚合形成二聚体或 多聚体,有些可聚合进一步形成骨架结构。具体成键情况有两种,一种是形成羟桥M-OH-M 的聚合体反应,如按亲核取代方式(S、)形成羟桥键MOH-M的羟基-水母体配合物 [M(OH(OHJ(x<N).C(D的二聚反应为: 14+ 2[Cr(OH)(OH2)s]- Cr(om) +H0 第二种是形成氧桥MOM的聚合反应,即氧基聚合反应。这种聚合过程要求在金属 的配位层中没有水配体,即如氧羟基母体MO,(OH]沙(x<N),如[MO(OH]M=W Mo)按亲核加成机理(AN)形成四聚体[MO1(OH)广,反应中形成边桥氧(O2》或面桥氧 (O)3),再如按加成消去机理(ABE,和ABE2)聚合的反应。Cr(V的二聚反应为: [HCrO4T+[HCrO4]-[Cr20]+H2O 影响上述反应的主要因素包括pH值、浓度、温度等。这些因素将决定水解程度、聚 合方式和最终产物。 B金属醇盐水解-聚合反应法 金属醇盐是用金属或金属无机盐和醇类发生反应而制得的、通式为M(OR)的化合物。 金属醇盐容易与醇类、羟基化合物、水等亲核试剂发生反应。溶胶凝胶过程中主要是采用 溶于醇类的醇盐浴液加水水解生成溶胶液,然后再经过缩合生成凝胶。水解和缩合反应的 方程式可以写成: M(OR)+xH2O-M(OR)(OH)x +xROH -M(OR)OH+-M(OR)-OH--M(OR)-O-M(OR)a-y-+H2O M(OR)mOH+-M(OR)--M(OR)-O-M(OR)-+ROH 以上三个反应不断进行,从而形成一系列线性、颗粒状或网状产物。实际反应过程十分复 杂,以上三个表达式只是对水解、缩水和缩醇过程的概括性描述。 金属醇盐水解聚合反应法制备材料的步骤包括均相溶液的制备、浴胶的制备、凝胶化 过程、干燥和热处理等步骤,其工艺流程如图91所示。 3

陈盐+陪剂 性 改性前翻作容液 水和催化剂 所段 透明海胶 感臭过利成诉过冈零化收闲配聚收 精膜口纤维☐粉末☐干超胶] 倒化处理阶段 成品☐ 图91醇盐水解聚合反应法工艺流程示意 a均相溶液的制备 金属醇盐水解聚合法的第一步是制取包含醇盐和水的均相溶液。由于金属醇盐在水中 的溶解度不大,一般要选用既与醇盐互溶、又与水互溶的醇作为溶剂。醇的加入量不宜过 大,因为醇盐水解要生成醇,所以醇对水解有抑制作用。水的加入量对溶胶制备及后续工 艺过程都有重要影响,对于一些水解活性高的醇盐,如钛醇盐,往往还需控制加水速度, 否则极易产生沉淀。此外,催化剂的种类和加入量对水解速率、缩聚速举以及溶胶陈化过 程中的结构演变也有重要影响。常用的酸催化剂为HC1,常用的碱催化剂为氨水。 b溶胶的制备 溶胶凝胶法中,最终产品的结构在溶胶形成过程中已初步形成,后续工艺均与溶胶的 性质直接相关,因此溶胶制备的质量十分重要。由均相溶液转变为溶胶的过程是醇盐水解 和缩聚的过程。以硅醇盐(硅酸酯)为例,硅醇盐的水解是由水中的氧原子与硅原子发生 的亲核结合:(RO)3Si-OR+HOH→(RO)Si-OH+ROH。 浴剂化效应、浴剂的极性等都对水解过程有重要影响。而且,在不同的介质中反应机 理也不同。在酸催化条件下,主要发生H,O对OR基团的亲电取代反应,水解速率快。随 者水解反应的进行,醇盐的水解活性随分子中的-O基团的减少而下降,很难充分水解为 S(O山4,缩聚反应在充分水解前即开始,因而缩聚产物的交联度低:在碱催化条件下,水 解反应主要是OH-对O的亲核取代反应,水解速*较酸催化慢,但醇盐的水解活性随分 子中-OR基团的减少而增大,4个-OR基很容易完全转变为-OH基团,进一步缩聚时易得 到高交联度的三维网状结构。硅、磷、硼以及许多金属元素(如铝、钛、铁等)的醇盐在 水解的同时均会发生聚合反应,如失水、缩聚、醇氧化、氧化、氢氧桥键合等。硅酸聚合 反应逐渐形成聚合物颗粒,生成溶胶,颗粒进一步交联组成三维网状即成凝胶, c凝胶化过程 凝胶是由细小颗粒聚集而成的由三维网状结构和连续分散相介质组成的具有固体特 征的胶态体系,按分散相介质不同有水凝胶、醇凝胶和气凝胶等。溶胶向凝胶的转变过程 是,缩聚反应形成的聚合物或粒子聚集体长大为小粒子簇,后者逐渐相互连接,形成粒子 藤一维车续固体网络,病相被句裹干固用骨架中,电整个体系失去活动性。在实际应用中, 制品的成型就是在此期间完成的,如成纤、涂膜、浇注等。成型过程只有在满足一定黏度 4

的条件下才能完成。但在凝胶点,黏度变化很快,溶胶黏度保持在一定范围内的时间往往 太短而不能满足工艺要求,因此,常需加入乙酰丙酮、乙二醇等来稳定黏度。影响醇盐水 解、缩聚速举的因素都会对凝胶化时间的长短产生影响 d凝胶的干燥 湿凝胶内包裹着大量的溶剂和水,干燥过程往往伴随着很大的体积收缩,因而容易引 起开裂。防止凝胶在干燥过程中开裂是溶胶凝胶工艺中至关重要而又较为困难的一环。特 别是制备尺寸较大的块体材料。 导致凝胶收缩、开裂的应力主要源于由充填凝胶骨架孔隙中液体的表面张力所产生的 毛细管力,凝胶尺寸越厚越易开裂。此外,干燥速*也是重要因素。为了获得有一定厚度 的完整凝胶,往往需要严格控制干燥条件(如温度、相对湿度等)使其缓慢干燥,有时需 要数日乃至数月的时间,因此干燥是浴胶凝胶法工艺中耗时最长的工序 解决开裂问题,可从增强固相骨架强度和减少毛细管力两方面考虑。前者包括控制水 解条件使其形成高交联度和高聚合度的缩聚物,或让湿凝胶在干燥前陈化一段时间以增强 骨架以及添加活性增强组分等:后者则可通过降低或消除液相表面张力入手,采用超临界 干燥是比较有效的方法。 凝胶干燥过程中的毛细管力来源于液气二相的表面张力,如果把凝胶中的有机溶剂或 水加湿加压至超过其临界温度和临界压力,液气界面就会消失,由此产生的毛细管力即不 复存在,基于这一原理的干漫方法即为招临界干操。由于水的临界温度(工=374℃)和临 界压力(P。=22MP)较高,且高温下水有解胶作用,通常的做法是先用醇脱水,然后采用 超临界干燥除去醇(甲醇:T=240℃,P=7.36Mpa:乙醇:T=243℃,P。=6.3MPa)。更好 的方法是在脱水后进一步用液态C02取代醇,再实施超临界干燥除CO2(液态C02: T。=31.1℃,P-7.36MPa)。超临界干燥不但可以大大缩短干燥时间,而且所制得的干凝胶 (气凝胶)的网络与孔隙结构与湿凝胶基本相同,在制备大块凝胶制品方面显示出极大的 优越性。 e干燥胶的热处理 热处理的目的是消除干燥凝胶中的气孔,使制品的相组成和显微结构满足产品的性能 要求。在加热过程中,干凝胶先在低温下脱去吸附在表面的水和醇。在265-300℃,-O求 基被氧化,300℃以上则脱去结构中的-0H。由于热处理伴随有较大的体积收缩和各种气体 (如CO2、HO、ROH)的释放,所以升温速率不宜过快。 由多孔疏松凝胶转变成致密玻璃至少有毛细收缩、缩合一聚合、结构驰豫和黏滞烧结 四个历程。在热处理过程中,由于凝胶的高比表面积和高活性,浇结温度常比粉料坯体低 数百度。采用热压烧结可缩短烧结时间,提高制品质量。升温制度将决定制品是玻璃态还 是晶态。 9.1.23形响溶胶-凝胶法的主要工艺因素 以上叙述可以看到有几个方面的因素对溶胶-凝胶法的工艺过程有主要影响,这些因素 包括加水量、醇浴剂、稳定剂、催化剂、干燥和热处理工艺等。 A水量的影响 加水量直接控制着醇盐的水解速度。加水量往往用水和醇盐的摩尔比π来表示。从理 论上讲,若催化得当,2<<4的金属醇盐较容易形成线性或连状聚合体;r在420的溶胶 容易形成网状或交联度较大的溶胶体系;>20基本是得到颗粒型溶胶。 5