
化学反应的平衡条件和反应进度x的关系 归东理大彩 SHANDONG UNIVERSITY OF TECHNOLOGY (dG).a n madx B eGδ =a nBm=D.Gm x or. B 这两个公式适用条件: (1)等温、等压、不作非膨胀功的一个化学反应; (2)反应过程中,各物质的化学势m保持不变
7 化学反应的平衡条件和反应进度 的关系 这两个公式适用条件: (1)等温、等压、不作非膨胀功的一个化学反应; (2)反应过程中,各物质的化学势 保持不变

判断化学反应的方向与限度 力东理王大 SHANDONG UNIVERSITY OF TECHNOLOGY ,An心,或D,G.h作判据都是等效的 用 B (D.Gm)r.<0 反应自发地向右进行 a ngm<0 B (D.Gm)T.2>0 反应自发地向左进行 ngm0 B (D.Gm)T.p=0 反应达到平衡 a nam=0
8 判断化学反应的方向与限度 用 作判据都是等效的 反应自发地向右进行 反应自发地向左进行 反应达到平衡

判断化学反应的方向与限度 归求理工大军 SHANDONG UNIVERSITY OF TECHNOLOGY 用 aGo 判断,这相当于G~x图上曲线的斜率 因为是微小变化,反应进度处于0~1mol之间。 cGǒ <0 xer.n 反应自发向右进行,趋向平衡 eGδ >0 反应自发向左进行,趋向平衡 xr. aJGo =0 xor.p 反应达到平衡
9 判断化学反应的方向与限度 用 判断,这相当于 图上曲线的斜率 反应自发向右进行,趋向平衡 反应自发向左进行,趋向平衡 反应达到平衡 因为是微小变化,反应进度处于0~1 mol之间
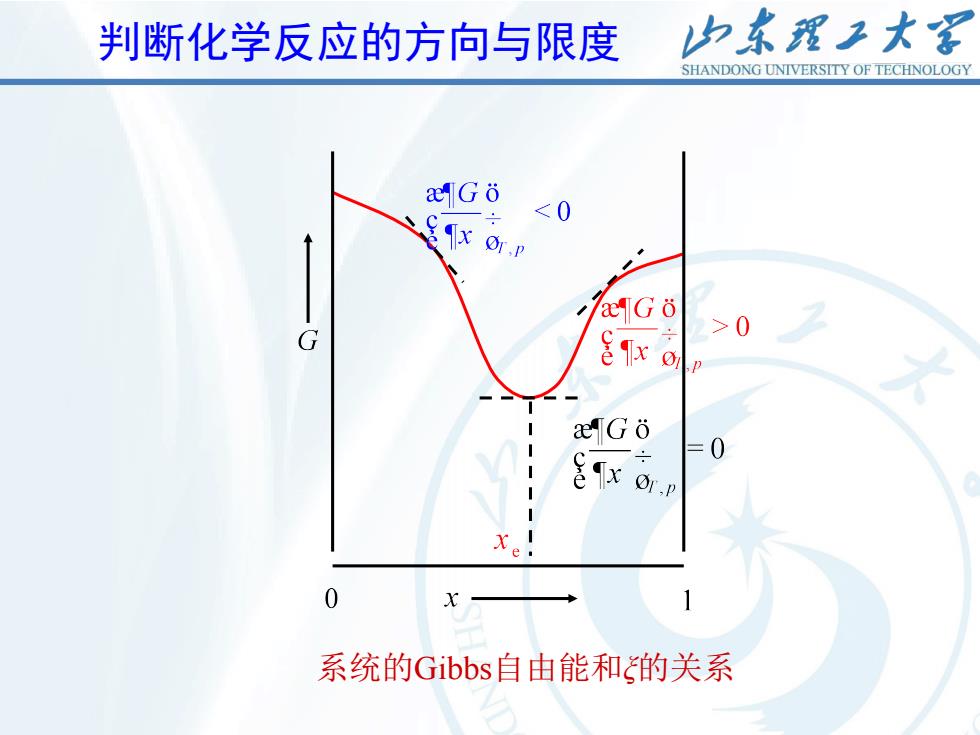
判断化学反应的方向与限度 归东理子大 SHANDONG UNIVERSITY OF TECHNOLOGY aTGo <0 x or.P >0 ěxo eGδ 系统的Gibbs自由能和的关系
10 判断化学反应的方向与限度 系统的Gibbs自由能和ξ的关系

为什么化学反应通常不能进行到底? 力东理卫大 SHANDONG UNIVERSITY OF TECHNOLOGY 严格讲,反应物与产物处于同一系统的反应都 是可逆的,不能进行到底。 只有逆反应与正反应相比小到可以忽略不计的 反应,可以粗略地认为可以进行到底。这主要是由 于存在混合Gibbs自由能的缘故
11 为什么化学反应通常不能进行到底? 严格讲,反应物与产物处于同一系统的反应都 是可逆的,不能进行到底。 只有逆反应与正反应相比小到可以忽略不计的 反应,可以粗略地认为可以进行到底。这主要是由 于存在混合Gibbs自由能的缘故