林影军 第九章可逆电池电动势及其应用 ENV (A) 1.5 02 Ew Fe3+ 1.0 B Fe2O3 A H B 0.5 腐蚀区 Es.c 0 (D) Fe2+ H20 (b) -0.5 -1.0 (C) Fe (a) -1.5 H2 02 468101214 Ex pH
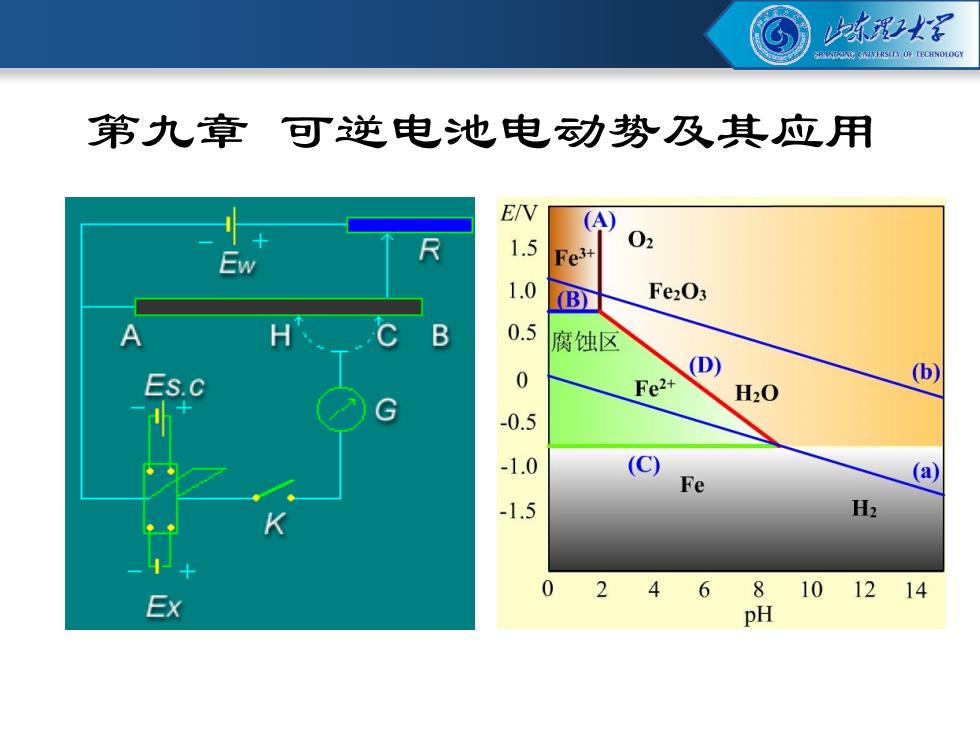
第九章 可逆电池电动势及其应用

冰2军 CNVERSETY OF TECHNOLOGY 第九章可逆电池的电动势及其应用 §9.1可逆电池和可逆电极 §9.2电动势的测定 §9.3可逆电池的书写方法及电动势的取号 §9.4可逆电池的热力学 §9.5电动势产生的机理 §9.6电极电势和电池的电动势 §9.7电动势测定的应用
第九章 可逆电池的电动势及其应用 §9.1 可逆电池和可逆电极 §9.2 电动势的测定 §9.3 可逆电池的书写方法及电动势的取号 §9.4 可逆电池的热力学 §9.5 电动势产生的机理 §9.6 电极电势和电池的电动势 §9.7 电动势测定的应用

冰影军 NGAVRSETY OF TECHNOLOG §9.1 可逆电池和可逆电极 1.可逆电池 1.1电化学与热力学的联系 1.2如何把化学反应转变成电能? 1.3组成可逆电池的必要条件 2.可逆电极和电极反应
§9.1 可逆电池和可逆电极 1. 可逆电池 2. 可逆电极和电极反应 1.1 电化学与热力学的联系 1.2 如何把化学反应转变成电能? 1.3 组成可逆电池的必要条件

1.可逆电池 冰影学 NCNVIRSETY OF IECHNOLOGY ●将化学能转化为电能的装置称为电池,若此转化是 以热力学可逆方式进行的,则称为“可逆电池”。 ●在可逆电池中(△,Grp=W=一nFE 其中n:电池输出电荷的物质的量,单位为mol; E:电池两电极间的电势差,在可逆条件下, 达最大值,称为电池的电动势
1. 可逆电池 ⚫ 将化学能转化为电能的装置称为电池,若此转化是 以热力学可逆方式进行的,则称为“可逆电池”。 ⚫ 在可逆电池中 (ΔrG)T,p = Wf = -nFE 其中 n:电池输出电荷的物质的量,单位为mol; E: 电池两电极间的电势差,在可逆条件下, 达最大值,称为电池的电动势
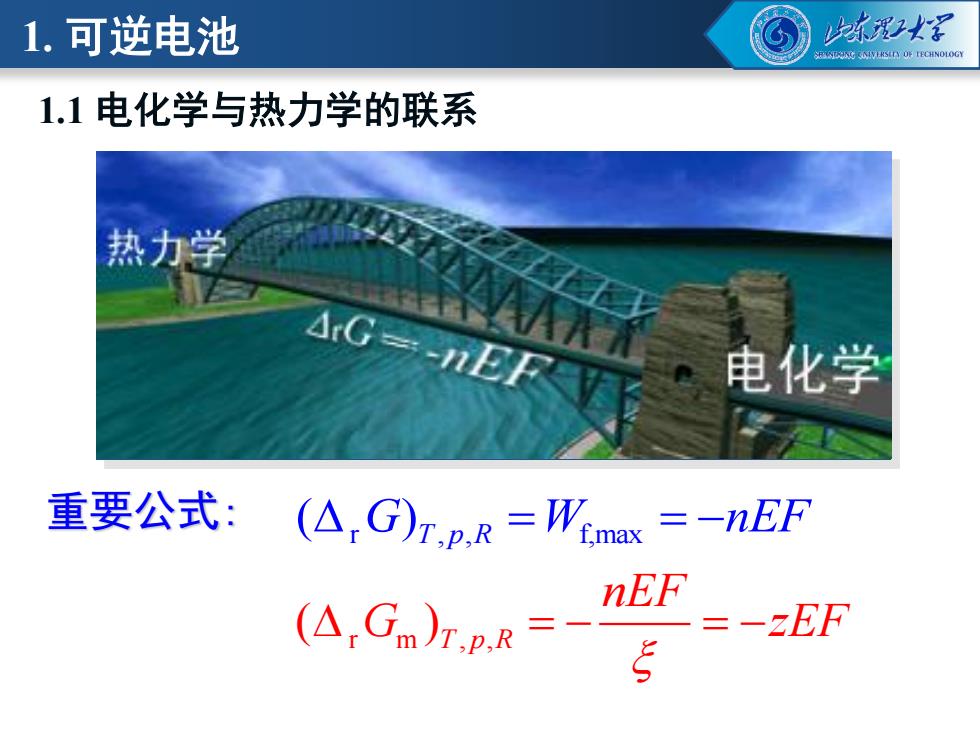
1.可逆电池 本理2深 1.1电化学与热力学的联系 热力学 AG=-nEF 电化学 重要公式:(△,G)r,p.R=Wmx=-nEF G.= nEF =-EF
重要公式: r , , f,max ( ) = = − G W nEF T p R r m , , ( )T p R nEF G zEF = − = − 1.1 电化学与热力学的联系 1. 可逆电池