3.氨基酸的主要理化性质 (1)两性解离特性 √氨基酸两端的-氨基和-羧基在溶液中均会 发生电离。 R-CH-COOH NH2 R-CH-COOH +OH R-CH-COO +OH R-CH-COO NH3" +H+ NH3+ +H+ NH2 pH<pI pH-pl pH>pI 阳离子 氨基酸的兼性离子 阴离子
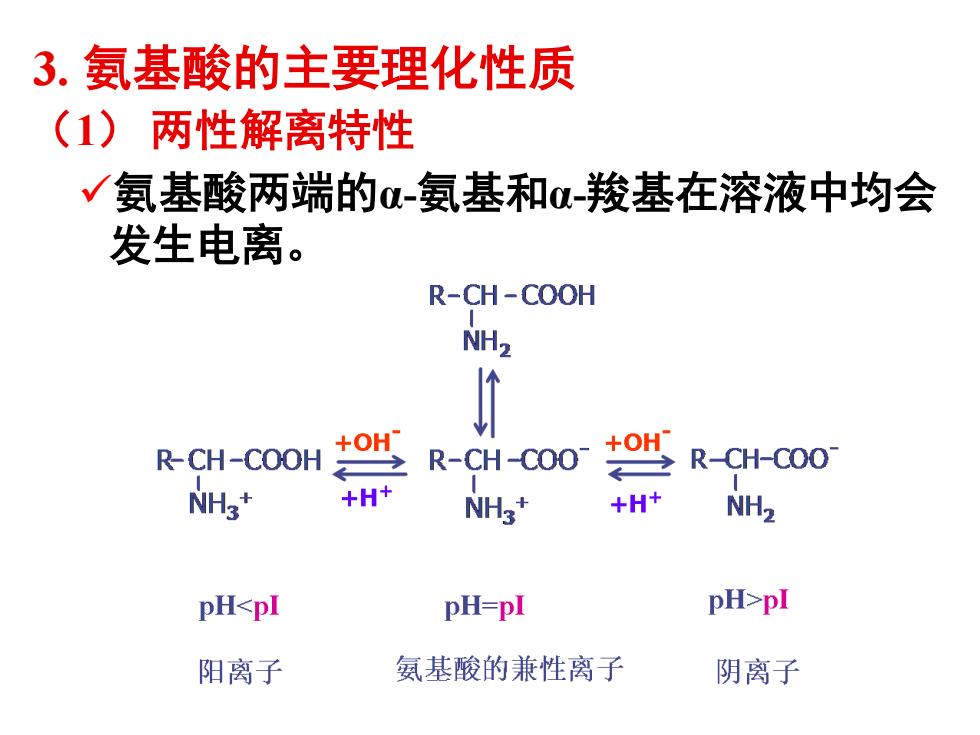
(1) 两性解离特性 ✓氨基酸两端的α-氨基和α-羧基在溶液中均会 发生电离。 3. 氨基酸的主要理化性质
√等电点(isoelectric point,pI):在某一特定的 pH,氨基酸以两性离子形式存在,且其所带的 正电荷数与负电荷数相等,即净电荷为零。该 pH值称为这种氨基酸的pl。 R-CH-COOH NH2 R-CH-COOH +OH R-CH-COO R-CH-COO NH3" +H+ NH3+ +H+ NH2 pH<pI pH=pI pH>pI 阳离子 氨基酸的兼性离子 阴离子
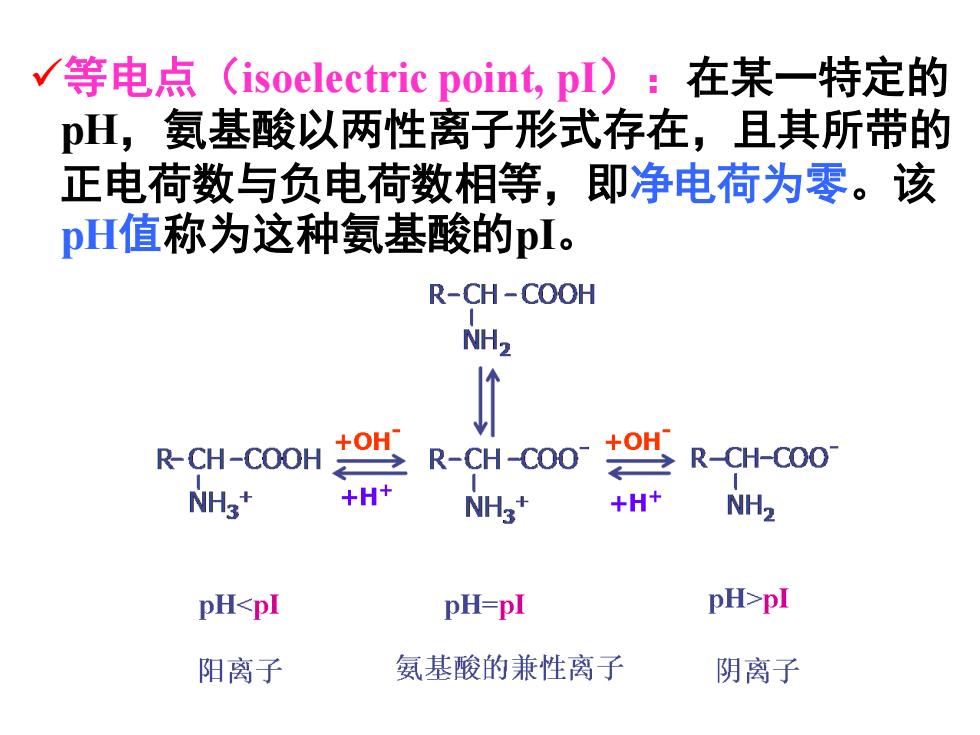
✓等电点(isoelectric point, pI):在某一特定的 pH,氨基酸以两性离子形式存在,且其所带的 正电荷数与负电荷数相等,即净电荷为零。该 pH值称为这种氨基酸的pI

(2)紫外吸收特性 √色氨酸和酪氨酸在紫外光区280nm左右有 最大吸收峰。 (3)茚三酮显色反应 √氨基酸和茚三酮反应生成蓝紫色化合物 √据此可用于氨基酸定量分析
(2)紫外吸收特性 ✓色氨酸和酪氨酸在紫外光区280nm左右有 最大吸收峰。 (3)茚三酮显色反应 ✓氨基酸和茚三酮反应生成蓝紫色化合物 ✓据此可用于氨基酸定量分析
三、肽 氨基酸通过肽键连接而形成肽(peptide) √肽键是由一个氨基酸的α-羧基与另一个氨基 酸的α-氨基脱水缩合形成的酰胺键。 R H R2 HgN-CH-C-OH H-N-CH-COO H2O R H R2 CH CH-COO
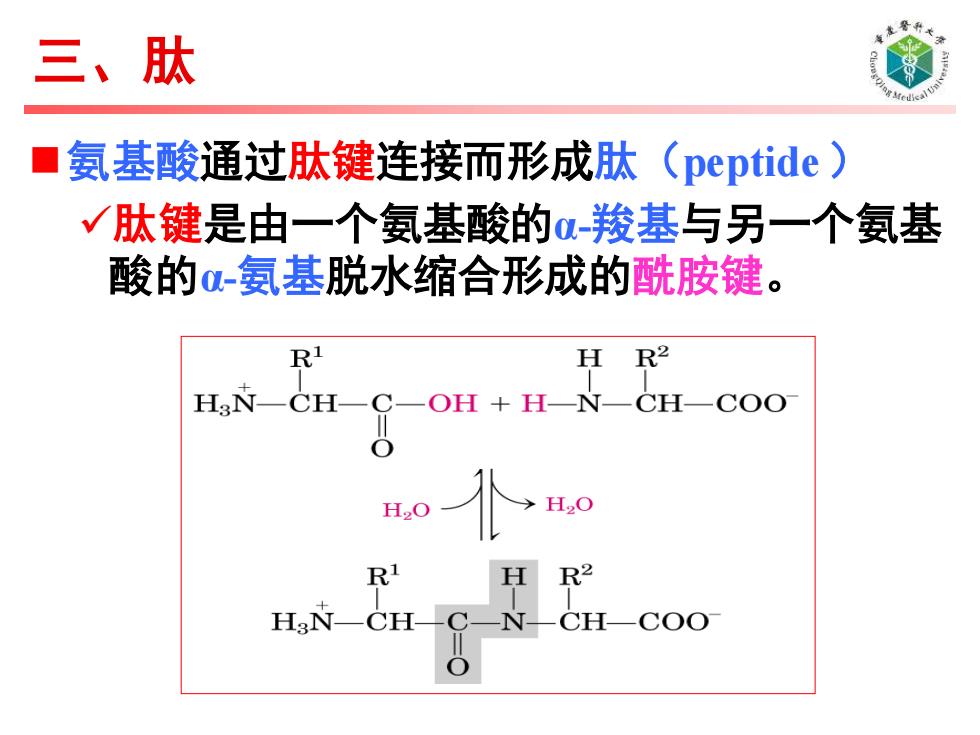
◼氨基酸通过肽键连接而形成肽(peptide ) ✓肽键是由一个氨基酸的α-羧基与另一个氨基 酸的α-氨基脱水缩合形成的酰胺键。 三、肽
√氨基酸残基:肽中的氨基酸因脱水缩合而基团不全 √多肽链:具有方向性,从N-端到C-端书写。 V寡肽(oligopeptide).:l0个氨基酸以内。 √多肽(polypeptide).:10-50个氨基酸。 √50个氨基酸以上习惯上叫蛋白质。 OH CH:CHa CH CH2OH H H CH2 H CHa H CH2 coo H H 中文书写:丝氨酰-甘氨酰-酪氨酰-丙氨酰-异亮氨酸 三字母缩写:Ser-Gly-Tyr-Ala-le;单字母缩写:S-G-Y-A-I
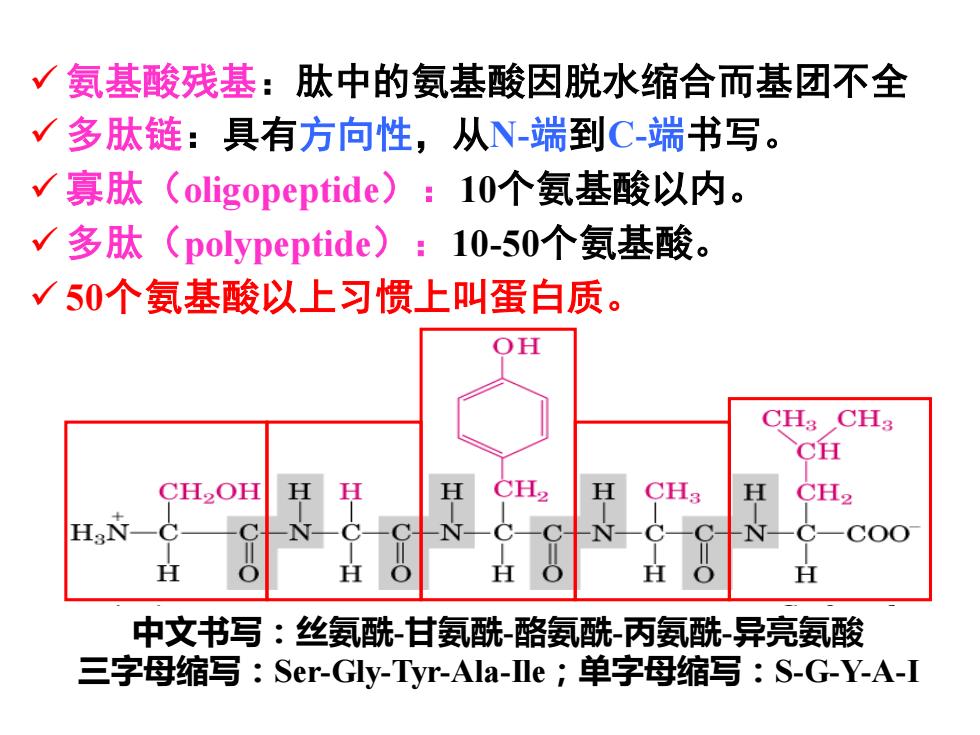
✓ 氨基酸残基:肽中的氨基酸因脱水缩合而基团不全 ✓ 多肽链:具有方向性,从N-端到C-端书写。 ✓ 寡肽(oligopeptide):10个氨基酸以内。 ✓ 多肽(polypeptide):10-50个氨基酸。 ✓ 50个氨基酸以上习惯上叫蛋白质。 中文书写:丝氨酰-甘氨酰-酪氨酰-丙氨酰-异亮氨酸 三字母缩写:Ser-Gly-Tyr-Ala-Ile;单字母缩写:S-G-Y-A-I