
2.偏摩尔量 又如: U=∑sUB Up=( aU )T,p.nc H-∑nsH aH H。=(h)pn Ong A=∑n4 A=( aA )T,p.nc B S=∑nSn as SB=( )T,p.nc B ns 6-24c aG G=0 )T,p.nc =4B 上一内容 下一内容 ◇回主目录 b返回 2024/9/5
上一内容 下一内容 回主目录 返回 2024/9/5 2.偏摩尔量 又如: c c c c c B B B , , B B B B B , , B B B B B , , B B B B B , , B B B B B , , B B B ( ) ( ) ( ) ( ) ( ) = T p n T p n T p n T p n T p n U U n U U n H H n H H n A A n A A n S S n S S n G G n G G n = = = = = = = = = =
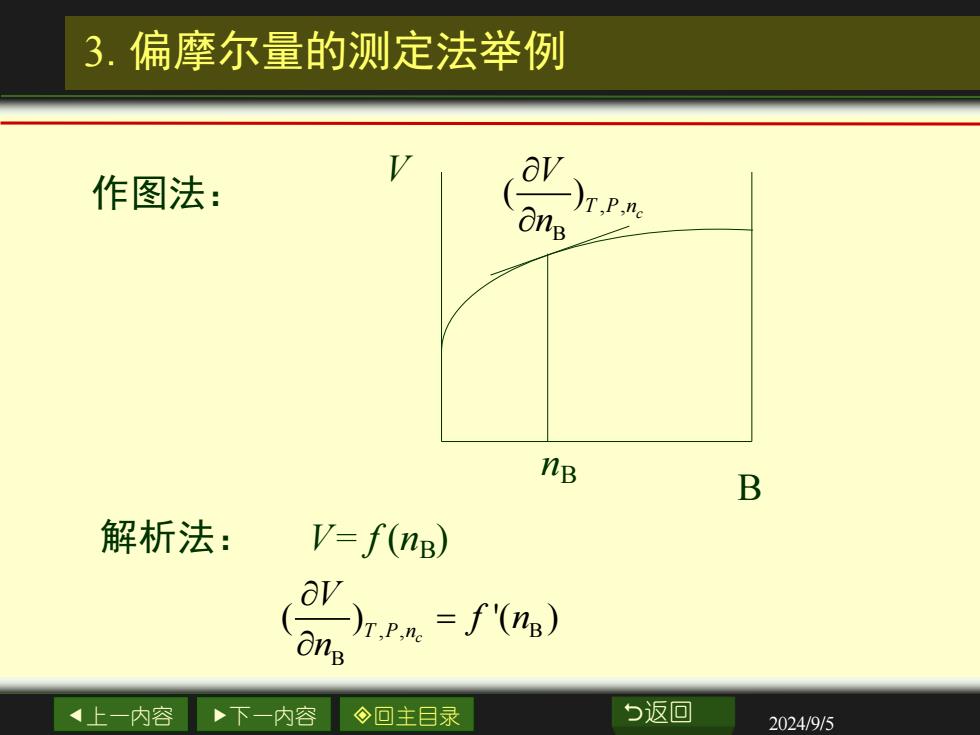
3.偏摩尔量的测定法举例 av 作图法: )T.P,nc nB B 解析法: V=f(nB) 上一内容 下一内容 ◇回主目录 b返回 2024/9/5
上一内容 下一内容 回主目录 返回 2024/9/5 3.偏摩尔量的测定法举例 , , B ( )T P nc V n V nB B 作图法: 解析法: V= f (nB) , , B B ( ) '( ) T P nc V f n n =

4.偏摩尔量与摩尔量的差别 摩尔量:纯组分的 V n 偏摩尔量:混合物 =(G V)T,Pn 若体系仅有一种组分(即纯物质),则根据摩尔 量的定义,X就是摩尔量。 4上一内容 下一内容 ◇回主目录 与返回 2024/9/5
上一内容 下一内容 回主目录 返回 2024/9/5 4.偏摩尔量与摩尔量的差别 摩尔量:纯组分的 m V V n = B , , c B ( )T p n V V n = 偏摩尔量:混合物 若体系仅有一种组分(即纯物质),则根据摩尔 量的定义,XB就是摩尔量

5.吉布斯-杜亥姆方程 如果在溶液中不按比例地添加各组分,则溶液浓 度会发生改变,这时各组分的物质的量和偏摩尔量均 会改变。 根据集合公式 X=nX,+n2X2+.+nXk 对X进行微分dX=h,dX,+Xdh+.+ndXk+Xdn (1) 在恒温、恒压下某均相体系任一容量性质的全微分为: dr =X dn +X2dn +.+Xrdng (2) 上一内容 下一内容 ◇回主目录 与返回 2024/9/5
上一内容 下一内容 回主目录 返回 2024/9/5 5.吉布斯-杜亥姆方程 如果在溶液中不按比例地添加各组分,则溶液浓 度会发生改变,这时各组分的物质的量和偏摩尔量均 会改变。 对X进行微分 d d d d d 1 X n X X n n X X n = + ++ + 1 1 1 1 k k k k ( ) 根据集合公式 X n X n X n X = + + + 1 1 2 2 k k 在恒温、恒压下某均相体系任一容量性质的全微分为: d d d d 2 X X n X n X n = + ++ 1 1 2 2 k k ( )

5.吉布斯-杜亥姆方程 (1)(2)两式相比,得: ndX +ndx2 +.+ndxs =0 即 ∑ndXa=0 这就称为Gibbs-Duhem方程,说明偏摩尔量之间 是具有一定联系的。某一偏摩尔量的变化可从其它偏 摩尔量的变化中求得。 4上一内容 下一内容 ◇回主目录 与返回 2024/9/5
上一内容 下一内容 回主目录 返回 2024/9/5 5.吉布斯-杜亥姆方程 这就称为Gibbs-Duhem方程,说明偏摩尔量之间 是具有一定联系的。某一偏摩尔量的变化可从其它偏 摩尔量的变化中求得。 (1)(2)两式相比,得: 1 k B B B=1 1 2 2 k k d d d 0 d 0 n X n X n n X + + + = X 即 =