
(二)金属型氢化物 氢气与过渡金属加热时发生反应,生成金属 型氢化物: M+H,△ MH. 2 金属氢化物有的是整比化合物,有的则是非整比 化合物,即原子数不是简单整数比的化合物。 金属型氢化物基本上保持着金属的外观,具 有金属光泽,也能导电。金属型氢化物从结构上 可以看作是金属原子组成的金属晶体的空隙中接 纳了半径较小的氢原子
无机化学 (二) 金属型氢化物 氢气与过渡金属加热时发生反应,生成金属 型氢化物: 2 M + H MH 2 x x △ 金属氢化物有的是整比化合物,有的则是非整比 化合物,即原子数不是简单整数比的化合物。 金属型氢化物基本上保持着金属的外观,具 有金属光泽,也能导电。金属型氢化物从结构上 可以看作是金属原子组成的金属晶体的空隙中接 纳了半径较小的氢原子

(三)分子型氢化物 氢元素与卩区元素(稀有气体及铟、铊元素除 外)形成的氢化物称为分子型氢化物。分子型氢化 物的熔点、沸点较低,在常温下多为气体。 分子型氢化物的热稳定性差别很大,有些在室 温下就发生分解,而有些在高温下也不分解。元素 的电负性越大,所形成的分子型氢化物的热稳定性 越高。 除氟化氢以外,其他分子型氢化物都具有还原 性。同一周期元素,从左到右,形成的分子型氢化 物的还原性减弱;同一族元素,自上而下,形成的 分子型氢化物的还原性增强
无机化学 (三)分子型氢化物 氢元素与 p 区元素(稀有气体及铟、铊元素除 外)形成的氢化物称为分子型氢化物。分子型氢化 物的熔点、沸点较低,在常温下多为气体。 分子型氢化物的热稳定性差别很大,有些在室 温下就发生分解,而有些在高温下也不分解。元素 的电负性越大,所形成的分子型氢化物的热稳定性 越高。 除氟化氢以外,其他分子型氢化物都具有还原 性。同一周期元素,从左到右,形成的分子型氢化 物的还原性减弱;同一族元素,自上而下,形成的 分子型氢化物的还原性增强

13族和14族元素的氢化物B,H6、A1H3、GaH3、 SH4与水作用时放出氢气: SiH+4H,O-HSiO+4H,1 14族和15族元素的氢化物CH4、GeH4、SnH4、 PH3、AsH3、SbH3与水不发生任何作用;NH3溶于水 与H叶加合,使溶液显弱碱性: NH,+H,O=NH+OH 16族和17族元素的氢化物H,S、H,Se、H,Te、 HF溶于水发生微弱解离,溶液显弱酸性。例如: H,S+H,O=HS+H.O" HCI、HBr、HI溶于水发生解离,溶液显强酸性: HCI+H,O=CI+H.O
无机化学 13 族和 14 族元素的氢化物 B2H6、AlH3、GaH3、 SiH4 与水作用时放出氢气: + NH + H O NH + OH 3 2 4 − SiH + 4H O H SiO + 4H 4 2 4 4 2 ↑ 14 族和15 族元素的氢化物 CH4、GeH4、SnH4、 PH3、AsH3、SbH3 与水不发生任何作用;NH3溶于水 与 H+ 加合,使溶液显弱碱性: 16 族和17 族元素的氢化物 H2S、H2Se、H2Te、 HF 溶于水发生微弱解离,溶液显弱酸性。例如: + H S + H O HS + H O 2 2 3 − HCl、HBr、HI 溶于水发生解离,溶液显强酸性: HCl + H O Cl + H O 2 3 − +

第一节碱金属和碱土金属元素概述 第1族中的锂、钠、钾、如、铯、钫六种金 属元素的氢氧化物都是易溶于水的强碱,所以称 为碱金属元素。 第2族包括铍、镁、钙、银、钡、镭六种元 素,由于钙、银、钡的氧化物的性质介于“碱性 的”碱金属氧化物和“土性的”难溶氧化物 AO3之间,因此称为碱土金属元素,通常把铍 和镁元素也包括在碱土金属元素之内
第二节 碱金属和碱土金属元素概述 第1族中的锂、钠、钾、铷、铯、钫六种金 属元素的氢氧化物都是易溶于水的强碱,所以称 为碱金属元素。 第 2 族包括铍、镁、钙、锶、钡、镭六种元 素,由于钙、锶、钡的氧化物的性质介于 “碱性 的” 碱金属氧化物和“土性的” 难溶氧化物 Al2O3 之间,因此称为碱土金属元素,通常把铍 和镁元素也包括在碱土金属元素之内
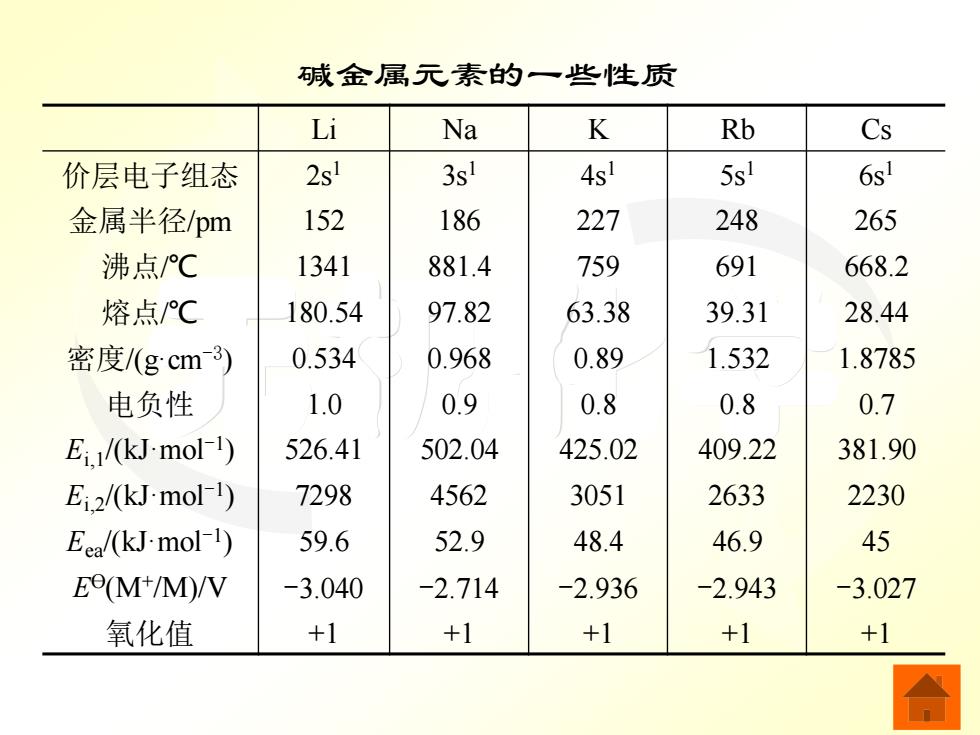
碱金属元素的一些性质 Li Na K Rb Cs 价层电子组态 2s1 3sl 4s! 5s! 6s1 金属半径pm 152 186 227 248 265 沸点℃ 1341 881.4 759 691 668.2 熔点C 180.54 97.82 63.38 39.31 28.44 密度/(gcm3) 0.534 0.968 0.89 1.532 1.8785 电负性 1.0 0.9 0.8 0.8 0.7 Ei./(kJ-mol-1) 526.41 502.04 425.02 409.22 381.90 Ei2/(kJ-mol-1) 7298 4562 3051 2633 2230 Eea/(kJ-mol-1) 59.6 52.9 48.4 46.9 45 Ee(M+/M)/V -3.040 -2.714 -2.936 -2.943 -3.027 氧化值 +1 +1 +1 +1 +1
无机化学 碱金属元素的一些性质 Li Na K Rb Cs 价层电子组态 2s1 3s1 4s1 5s1 6s1 金属半径/pm 152 186 227 248 265 沸点/℃ 1341 881.4 759 691 668.2 熔点/℃ 180.54 97.82 63.38 39.31 28.44 密度/(g·cm-3 ) 0.534 0.968 0.89 1.532 1.8785 电负性 1.0 0.9 0.8 0.8 0.7 Ei,1/(kJ·mol-1 ) 526.41 502.04 425.02 409.22 381.90 Ei,2/(kJ·mol-1 ) 7298 4562 3051 2633 2230 Eea/(kJ·mol-1 ) 59.6 52.9 48.4 46.9 45 E Ө(M+ /M)/V -3.040 -2.714 -2.936 -2.943 -3.027 氧化值 +1 +1 +1 +1 +1