
②规定熵或标准熵 a)规定熵(标准熵): 在标准状态下(T,P),1mol纯物质的熵值 S) m:1mol; 0:标态; 298K:温度 b)化学反应熵的计算 (1) 由规定嫡计算化学反应的△SM29sK △,S228K)=(∑y,S)产(∑Si)反应物
1 ②规定熵或标准熵 a)规定熵(标准熵): 在标准状态下(T,P θ),1mol 纯物质的熵值 S m(298K) b)化学反应熵的计算 (1)由规定熵计算化学反应的Δr S m(298K) Δr S m(298K) =( ) , m j j j S 产物 - ( ) , m i i i S 反应物 m: 1mol;θ:标态; 298K:温度
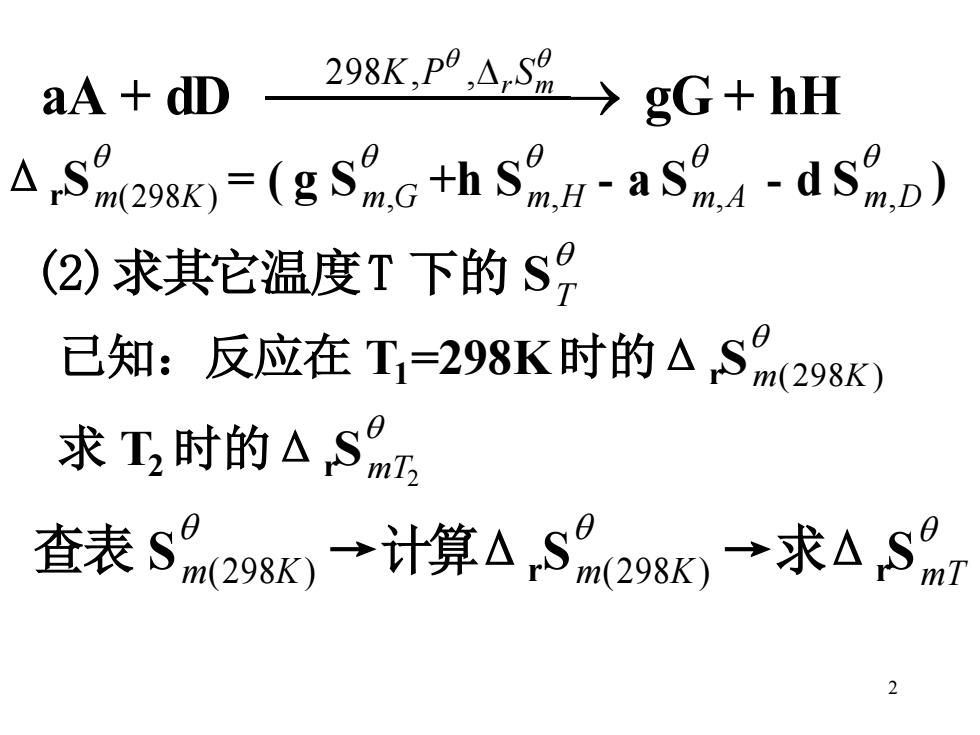
aA dD 298Kp4s8→gG+hH A S(298K)=(gSthSdmo) (2)求其它温度T下的S 己知:反应在T1=298K时的△SM298K 求工,时的△S9m 查表S9m28K)→计算△rS%298K→求△rSr 2
2 aA + dD ⎯⎯⎯⎯ ⎯→ 298K,P , r S m gG + hH Δr S m(298K) = ( g S m,G +h S m,H - a S m,A - d S m,D ) (2)求其它温度T 下的 S T 已知:反应在 T1 =298K时的Δr S m(298K) 求 T2 时的Δr S m T2 查表 S m(298K) →计算Δr S m(298K) →求Δr S m T
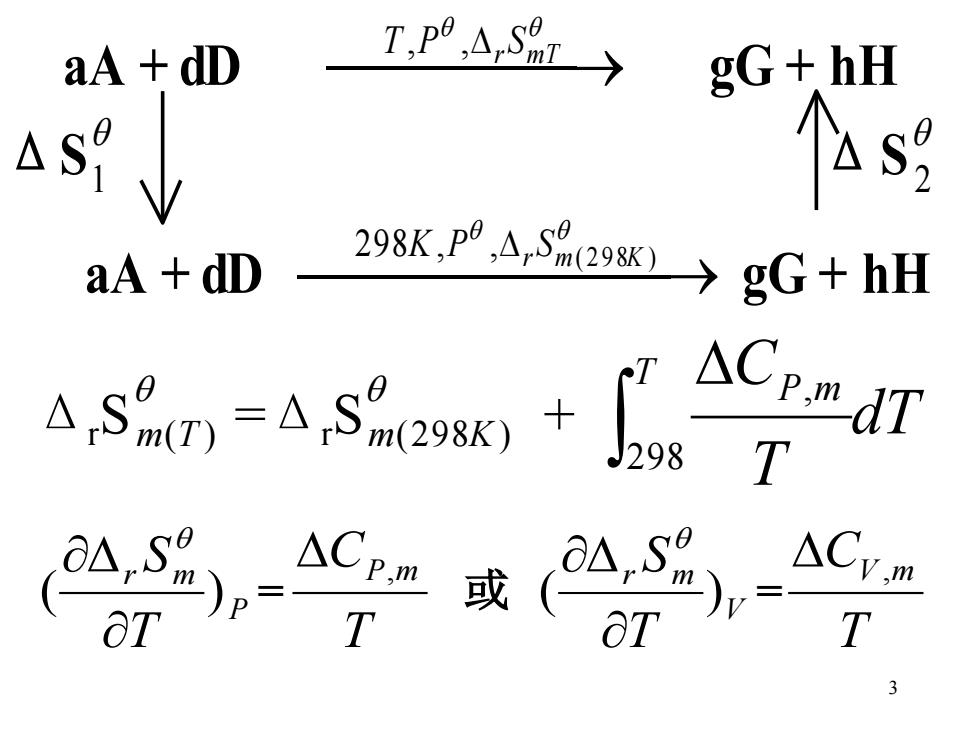
aA dD Tp9,d→ gG+hH s aA dD 298K,p9,A,S9298x →gG+hH T △Cpm T T 3
3 aA + dD ⎯⎯⎯⎯→ r m T T ,P , S gG + h H ΔS 1 ΔS 2 aA + dD ⎯⎯⎯⎯⎯ ⎯→ ( 298 ) 298 , , r m K K P S gG + h H Δ r S m(T ) =Δ r S m(298K) + dT T T CP m 298 , P r m T S ( ) = T CP,m 或 V r m T S ( ) = T CV ,m

联想:( 2).-sc 当ACrm0时,△m,△H与T无关 适用范围:等TP,等TV化学变化和相变化 说明:若有相变化发生,需考虑可逆相变化 的熵值 AS A(S,T→0) →A(1,T2) 个 A(S,T)A→A(1,T)
4 联想: P r m T H ( ) =CP,m 当CP,m =0 时,Δr S m ,Δr H m 与 T无关 适用范围:等 TP,等 TV 化学变化和相变化 说明:若有相变化发生,需考虑可逆相变化 的熵值 ΔS1 ΔS3 A(s,T1 )⎯ ⎯S2 → A(l,T1 ) A(s,T→0) ⎯⎯→ S A(l,T2 )
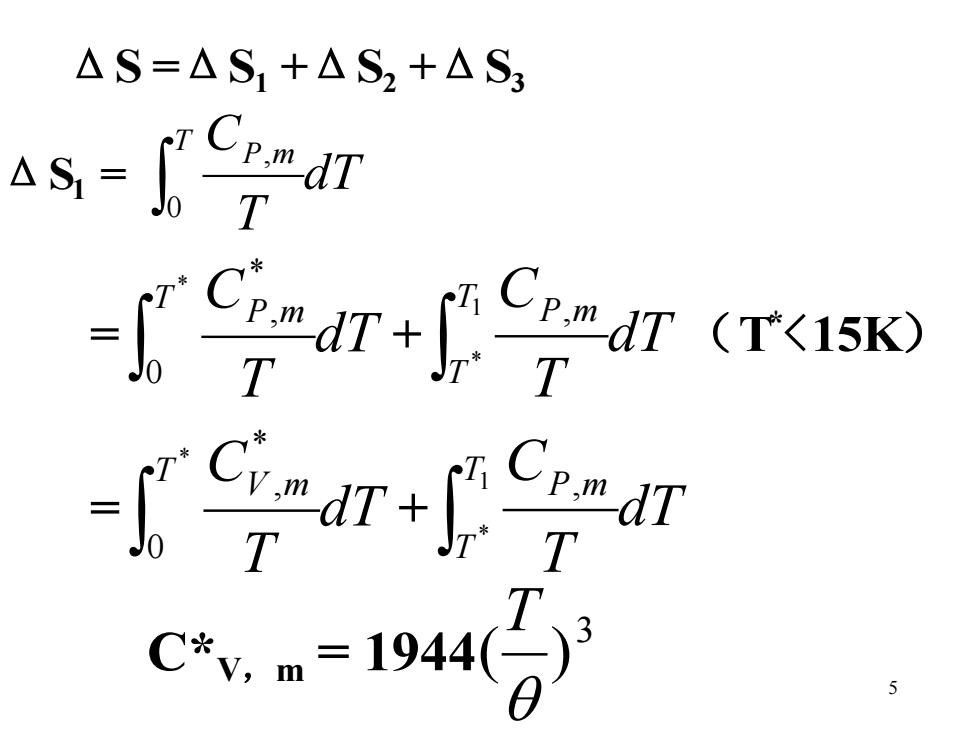
△S=△S1+△S2+AS3 △S= T CPm dT T C7+ pm dT T 5
5 ΔS =ΔS1 +ΔS2 +ΔS3 ΔS1 = dT T T CP m 0 , = dT T T CP m * 0 * , + dT T T C T P m 1 * , (T * <15K) = dT T T CV m * 0 * , + dT T T C T P m 1 * , C*V,m = 1944 3 ( ) T