x热力学基础内能(Internal energy, U)体系内部含有的总能量内能改变的方式surroumndings分子的平动能分子间的势能systemworkheat分子内部的转动能和振动能mass电子运动能核能内能将发生改变
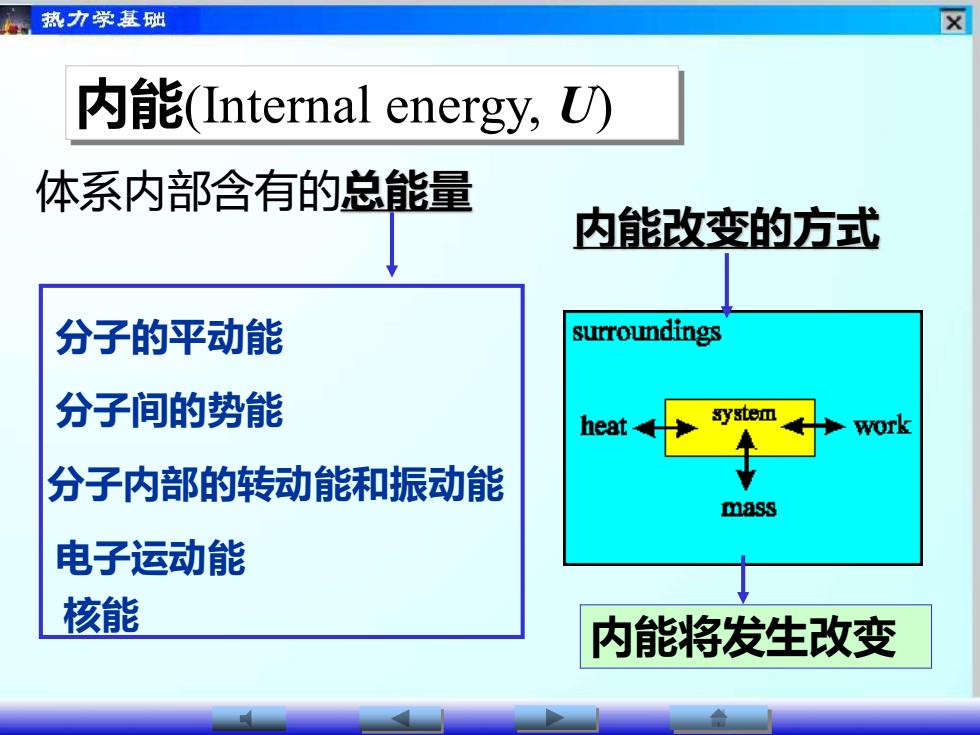
内能(Internal energy, U) 体系内部含有的总能量 分子的平动能 分子间的势能 分子内部的转动能和振动能 电子运动能 核能 内能改变的方式 内能将发生改变

X热力学基础1.内能(internal energy ,U)系统内部能量的总和。包括:动能;势能;核能等。2.说明:★内能是状态函数:状态一定,U一定。★内能属广度性质:能量都具有加和性★内能的绝对值无法确定:微观粒子运动的复杂性
1. 内能(internal energy , U) 系统内部能量 的总和。包括:动能;势能;核能等。 2. 说明: 内能是状态函数:状态一定,U一定。 内能属广度性质:能量都具有加和性。 内能的绝对值无法确定:微观粒子运动 的复杂性
X热力学基础五、热力学第一定建自然界的一切物质都具有能量能量有各种不同形式,能够从一种形式转化成另一种形式,在转化过程中能量的总和不变。能量守恒定律
五、 热力学第一定律 自然界的一切物质都具有能量, 能量有各种不同形式,能够从一种形 式转化成另一种形式,在转化过程中 能量的总和不变。 能量守恒定律
x热力学基础据能量守恒转化定律surroundingsclosedTeyetemheatworkAU= + W的代
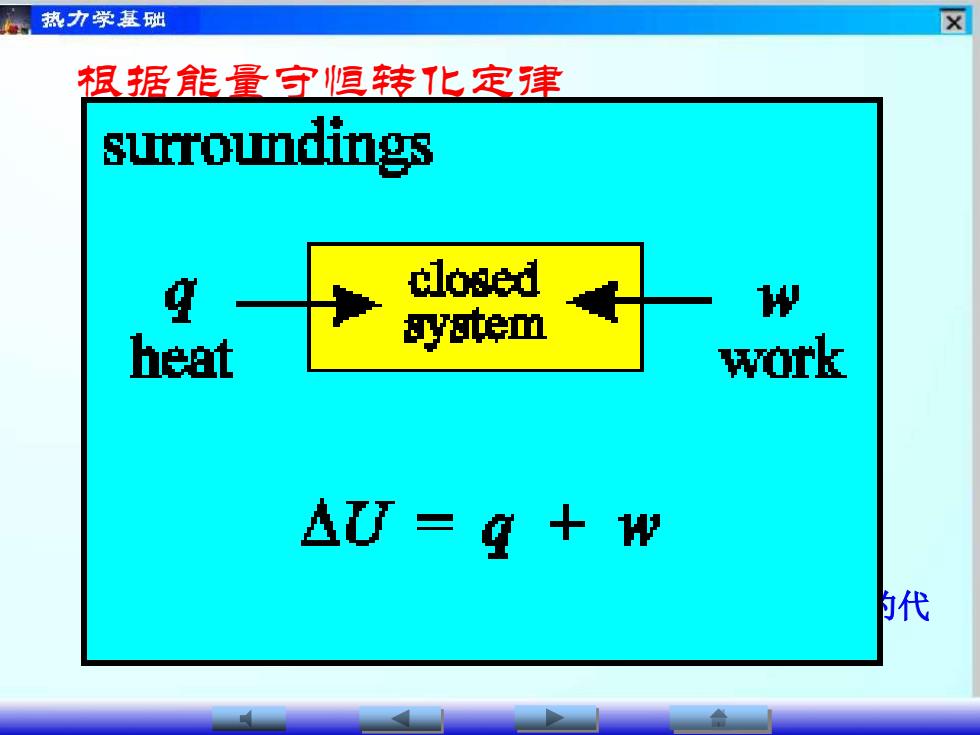
热力学能(U): 系统内所有微观粒子的全部 能量之和,也称内能。 U是状态函数。 在封闭系统中,系统和环境之间只有热和功的交换; 若环境对体系作功W,体系从环境吸热Q,则系统的能量 必有增加,则增加的这部分能量等于W与Q之和,即: 根据能量守恒转化定律 U = Q +W 热力学能变化只与始态、终态有关,与变化途径无关。 对封闭体系,途径不同,热和功也不同;但他们的代 数和与过程有关而与途径无关

x热力学基础例体系从环境吸热O=10kJ体系状态1状态2Ui体系对环境作功W=15kJU2AU体= U2- Ui = Q + W= 10+(-15) = -5 kJAU环=U2- U, =Q + W= (-10)+15 = 5 kJAU环=0+△U体体系和环境总能量守恒
例 体系对环境作功W=15kJ 体系状态1 U1 状态2 U2 体系从环境吸热 Q=10kJ ΔU体= U2 - U1 = Q + W = 10+(-15) = -5 kJ ΔU环= U2 - U1 = Q + W = (-10)+15 = 5 kJ U 体 + U 环 = 0 体系和环境总能量守恒