
如: CH;-CH-CH2-CH-CH2-CH-CH CH3-CH2-CH-CH3 CHs 2)主链编号:从靠近取代基的一端开始,用阿拉伯数字给主链碳原子依次编 号,确定取代基的位次。若有选择,应使小的取代基位次以及多个取代基位次和 尽可能小。 CH:-CH2-CH-CH-CH-CH CH:-CH-CH-CH-CH-CH-CH CH:CH-CH; CH CH:CH: 3)书写名称:把取代基的名称写在“某烷”之前,取代基的位次写在取代基 名称的前面,中间用短线隔开。如有相同的取代基,就将其合并,取代基的数目 用二、三等汉字表示,写在取代基的名称前,表示取代基位次的阿拉伯数字之间 要用“,”号隔开:如果几个取代基不同,应把小的取代基写在前面,大的取代 基写在后面。常见烷基的大小次序为:甲基<乙基<丙基<丁基<异丁基<异丙 基<仲丁基(见第三章第一节中“次序规则”相关内容)。 CH3-CH-CH2-CH2-CHs CH3-CH2-CH-CH2-CH-CH3 CH-CH: CH2-CH:CH3 3-甲基己烷 2-甲基-4-乙基己烷 CH3 CH3 -CH-CH2-CH CHs-CH:-CH-CH-CH-CH-CH; CH.CH CH3 CH2-CH2-CH3 2,2,3-三甲基戊烷 2,3,5三甲基-4-丙基庚烷 课堂互动 命名下列化合物或根据名称写出结构式 (1)CH3-CH-CH-CH-CH3 CHs C2Hs CH (2)2,2,5-三甲基己烷 四、烷烃的物理性质 有机化合物的物理性质通常包括物态、沸点、熔点、密度、溶解度和光谱性
如: CH3-CH2-CH-CH2-CH3 CH2-CH2-CH3 3 2 1 4 5 6 CH3-CH2-CH2-CH-CH2-CH-CH3 CH3-CH2-CH CH3 CH3 4 3 2 1 7 6 5 2)主链编号:从靠近取代基的一端开始,用阿拉伯数字给主链碳原子依次编 号,确定取代基的位次。若有选择,应使小的取代基位次以及多个取代基位次和 尽可能小。 CH3-CH2-CH-CH-CH2-CH3 1 2 3 4 5 6 CH3-CH-CH2-CH2-CH-CH-CH3 CH3 7 6 5 4 3 2 1 CH3 CH2CH3 CH3 CH3 3)书写名称:把取代基的名称写在“某烷”之前,取代基的位次写在取代基 名称的前面,中间用短线隔开。如有相同的取代基,就将其合并,取代基的数目 用二、三等汉字表示,写在取代基的名称前,表示取代基位次的阿拉伯数字之间 要用“,”号隔开;如果几个取代基不同,应把小的取代基写在前面,大的取代 基写在后面。常见烷基的大小次序为:甲基<乙基<丙基<丁基<异丁基<异丙 基<仲丁基(见第三章第一节中“次序规则”相关内容)。 CH3-CH-CH2-CH2-CH3 CH2-CH3 CH3-CH2-CH-CH2-CH-CH3 CH2-CH3 CH3 CH3-C-CH-CH2-CH3 CH3 CH3 CH3 CH3-CH2-CH-CH-CH-CH-CH3 CH3 CH3 CH3 CH2-CH2-CH3 3- 2- -4- 2,2,3- 2,3,5- -4- 甲基己烷 甲基 乙基己烷 三甲基戊烷 三甲基 丙基庚烷 课堂互动 命名下列化合物或根据名称写出结构式 CH3 CH CH3 CH C2H5 CH CH3 (1) CH3 (2) 2,2,5-三甲基己烷 四、烷烃的物理性质 有机化合物的物理性质通常包括物态、沸点、熔点、密度、溶解度和光谱性
质等。它们在一定条件下有固定的数值,这些数值称为物理常数。烷烃同系物的 物理性质随分子中碳原子数目的增加而呈现规律性的变化。部分正烷烃的某些物 理常数见表2-2。 表2-2部分正烷烃的某些物理常数 名称 分子式 沸点(℃) 熔点(℃)密度(kgL)(20C) 甲烷 CH -161.7 -182.6 乙烷 C.H -88.6 -172.0 丙烷 C He -422 -187.1 0.5000 -0.5 -135 0.5788 36. -129.7 0.6260 心 68. -94.0 0.659 CH 98.4 -90.5 0.6837 辛烷 CsH 125.7 -56.8 0.7028 壬烷 150.7 -53.7 0.7179 癸烷 297 十五烷 0 十六烷 C16H4 280 0.774 十七烷 CiH 303 22.0 0.7767 十八烷 CH 308 28.0 0.7767 十九 32.0 0.7767 二十炉 C:oH4 36.4 0.777 三十烷 C30H62 66 四十烷 C4oHs2 81 在常温(25℃)和常压(101.325kPa)下,C1~C4的正烷烃是无色的气体,Cs C,的正烷烃是无色的液体,C1g以上的正烷烃是无色的固体。 (一)沸点 烷烃是非极性分子,分子间的作用力主要是色散力,色散力具有加和性,随 分子中碳原子数和氢原子数的增加,色散力加大,因此正烷烃的沸点(即)随着分 子量的增加而表现出规律性的升高。在低级烷烃中,因分子量增加的幅度比较大 沸点升高比较明显。而在高级烷烃中,分子量增加的幅度较慢,这种影响就不太 明显了。 同碳原子数的支链烷烃的沸点比直链烷烃低,这是由于支链的存在使分子不 能相互靠得更近,减弱了色散力,因此使沸点降低。支链越多,沸点越低。 (二)熔点 直链烷烃的熔点(mp),基本上也是随分子量的增加而逐渐升高。但偶数碳原
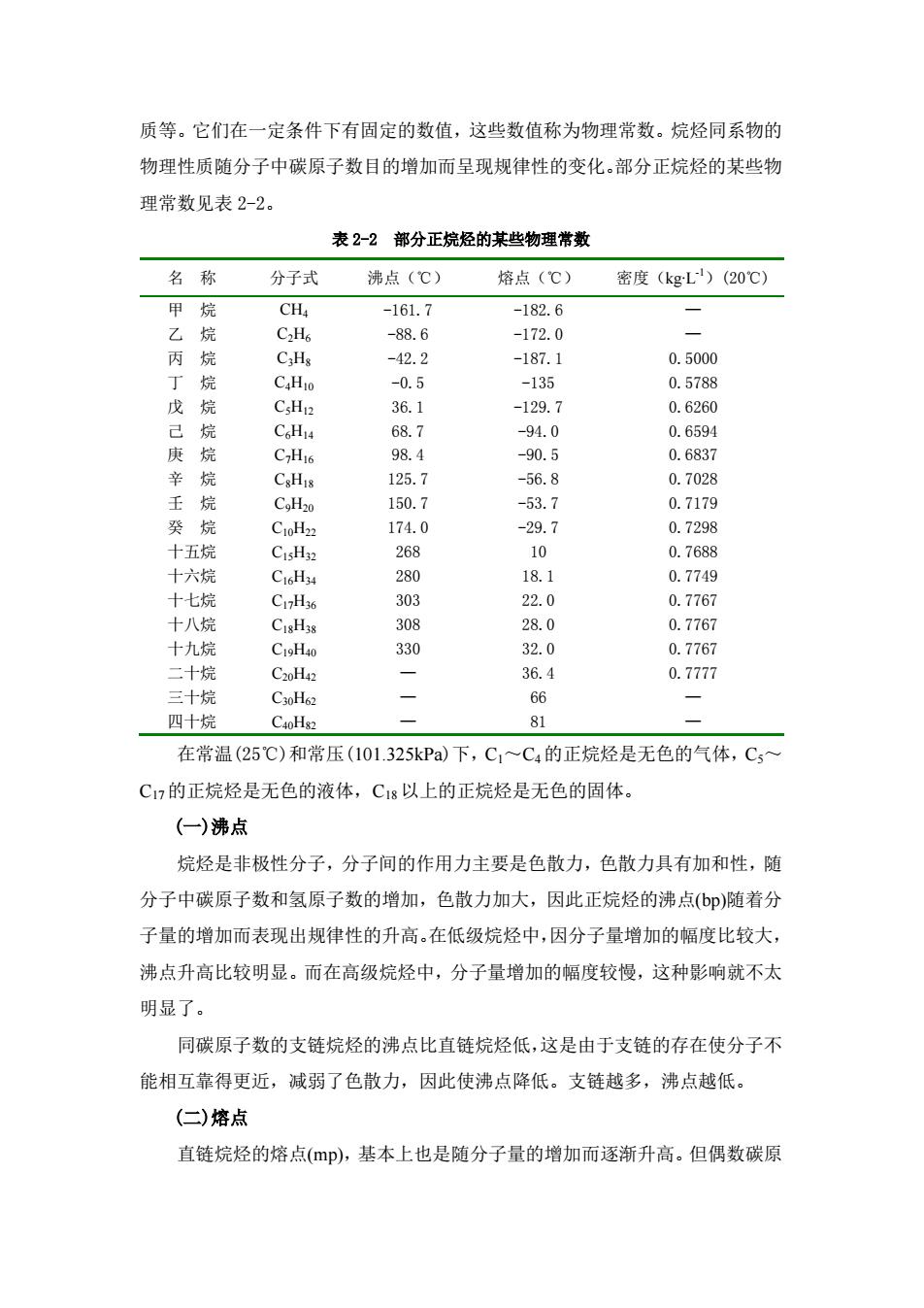
质等。它们在一定条件下有固定的数值,这些数值称为物理常数。烷烃同系物的 物理性质随分子中碳原子数目的增加而呈现规律性的变化。部分正烷烃的某些物 理常数见表 2-2。 表 2-2 部分正烷烃的某些物理常数 名 称 分子式 沸点(℃) 熔点(℃) 密度(kg∙L-1)(20℃) 甲 烷 乙 烷 丙 烷 丁 烷 戊 烷 己 烷 庚 烷 辛 烷 壬 烷 癸 烷 十五烷 十六烷 十七烷 十八烷 十九烷 二十烷 三十烷 四十烷 CH4 C2H6 C3H8 C4H10 C5H12 C6H14 C7H16 C8H18 C9H20 C10H22 C15H32 C16H34 C17H36 C18H38 C19H40 C20H42 C30H62 C40H82 -161.7 -88.6 -42.2 -0.5 36.1 68.7 98.4 125.7 150.7 174.0 268 280 303 308 330 — — — -182.6 -172.0 -187.1 -135 -129.7 -94.0 -90.5 -56.8 -53.7 -29.7 10 18.1 22.0 28.0 32.0 36.4 66 81 — — 0.5000 0.5788 0.6260 0.6594 0.6837 0.7028 0.7179 0.7298 0.7688 0.7749 0.7767 0.7767 0.7767 0.7777 — — 在常温(25℃)和常压(101.325kPa)下,C1~C4的正烷烃是无色的气体,C5~ C17 的正烷烃是无色的液体,C18 以上的正烷烃是无色的固体。 (一)沸点 烷烃是非极性分子,分子间的作用力主要是色散力,色散力具有加和性,随 分子中碳原子数和氢原子数的增加,色散力加大,因此正烷烃的沸点(bp)随着分 子量的增加而表现出规律性的升高。在低级烷烃中,因分子量增加的幅度比较大, 沸点升高比较明显。而在高级烷烃中,分子量增加的幅度较慢,这种影响就不太 明显了。 同碳原子数的支链烷烃的沸点比直链烷烃低,这是由于支链的存在使分子不 能相互靠得更近,减弱了色散力,因此使沸点降低。支链越多,沸点越低。 (二)熔点 直链烷烃的熔点(mp),基本上也是随分子量的增加而逐渐升高。但偶数碳原