-CH 酶-CH一OH+ =0 -CH2-0 =0+FH CH3- -CH 有机化合物能强烈地抑 系统有关的乙酰 酰 0 (CH,)N+CH,CHOC -(CH,),N+CH,CH,OH+CH,COOH CH, 乙酰胆碱 胆碱 乙酸 在农业上,抑制作用常被用于设计开发新型农药,如敌百虫、敌敌畏、乐果等有机 磷农药能专一地抑制乙酰胆碱酯酶的活力,因而使昆虫体内大量积累乙酰胆碱影响神经 传导失去知觉 除 有机磷化合物 外,有机汞、有机碑化合 胺对 制剂。 碘乙酸等作 抑制剂 逆结合,可用透析、过滤等物理方法除去抑制剂而恢复酶的 活力。这和 作用叫做司逆 业作田 查的之间存在者一个平衡。根据抑制剂与底物的关系,可逆抑制作用分为三种类型。 1.竞争性抑制作用 竞争性抑制剂分子的结构与底物分子的结构非常近似。竞争性抑制剂能以非共价键 在酶分子的活性中心处与酶分子结合。抑制剂与底物分子竞争酶的活性中心。若用大写 的英文字母I表示抑制剂,竞争性的抑制作用(competitive inhibition)可用下式表示: +S一ES一E+P E1(无活性中间产物) 竞争性抑制剂的作用机理,在于它占据了酶分子的活性中心,使酶的活性中心无法 与底物分子结合,因而也就无法催化底物发生反应。这时,抑制剂并没有破坏酶分子的 特定构象,也没有使酶分子的活性中心解体。由于竞争性抑制剂与酶的结合是可逆的, 可用加入大量底物,提高底物竞争力的办法,消除竞争性抑制剂的抑制作用。 116
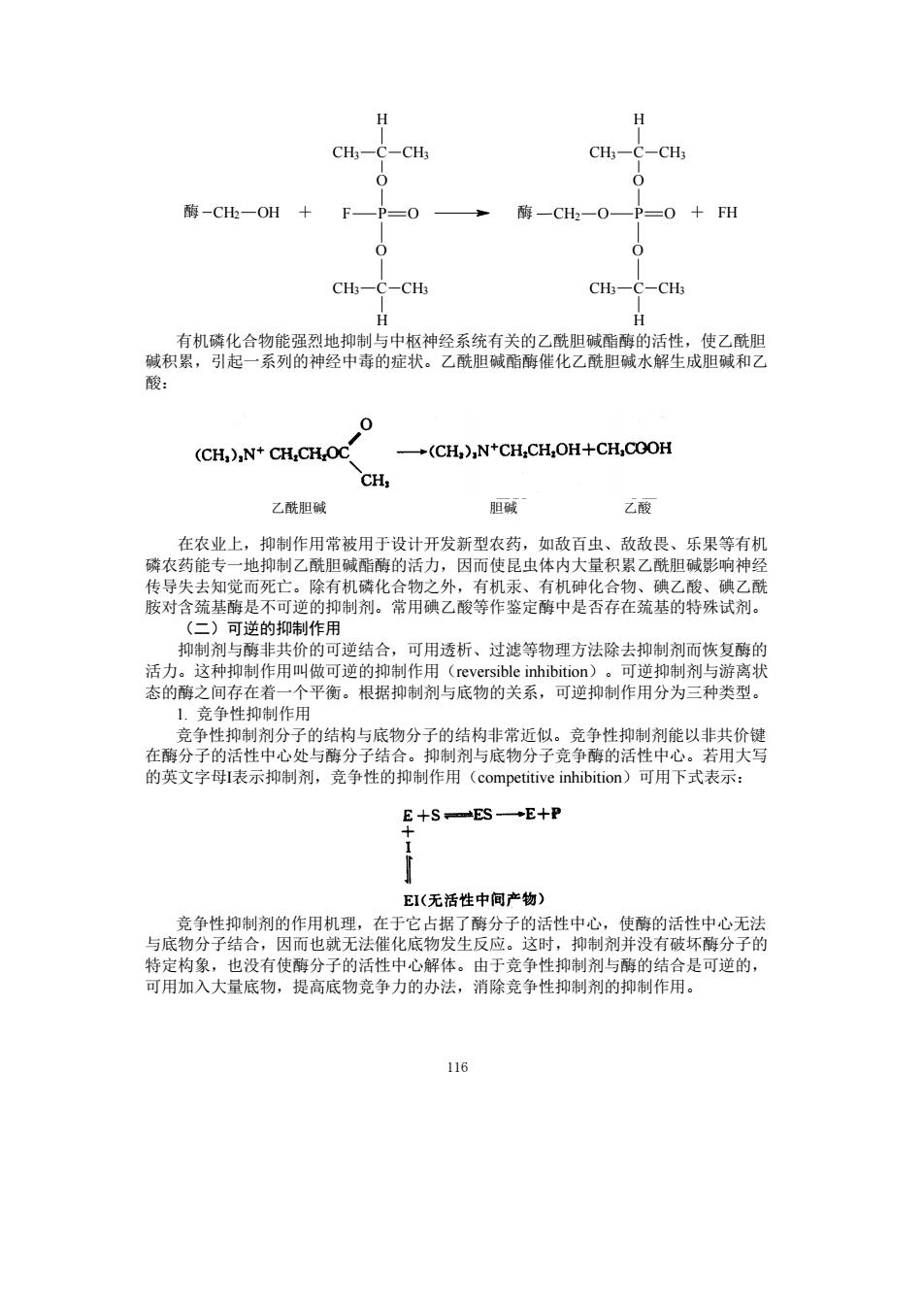
116 C O P C O CH3 CH3 H CH3 CH3 H 酶 CH2 OH + F O C O P C O CH3 CH3 H CH3 CH3 H 酶 CH2 O O + FH 有机磷化合物能强烈地抑制与中枢神经系统有关的乙酰胆碱酯酶的活性,使乙酰胆 碱积累,引起一系列的神经中毒的症状。乙酰胆碱酯酶催化乙酰胆碱水解生成胆碱和乙 酸: 乙酰胆碱 胆碱 乙酸 在农业上,抑制作用常被用于设计开发新型农药,如敌百虫、敌敌畏、乐果等有机 磷农药能专一地抑制乙酰胆碱酯酶的活力,因而使昆虫体内大量积累乙酰胆碱影响神经 传导失去知觉而死亡。除有机磷化合物之外,有机汞、有机砷化合物、碘乙酸、碘乙酰 胺对含巯基酶是不可逆的抑制剂。常用碘乙酸等作鉴定酶中是否存在巯基的特殊试剂。 (二)可逆的抑制作用 抑制剂与酶非共价的可逆结合,可用透析、过滤等物理方法除去抑制剂而恢复酶的 活力。这种抑制作用叫做可逆的抑制作用(reversible inhibition)。可逆抑制剂与游离状 态的酶之间存在着一个平衡。根据抑制剂与底物的关系,可逆抑制作用分为三种类型。 1. 竞争性抑制作用 竞争性抑制剂分子的结构与底物分子的结构非常近似。竞争性抑制剂能以非共价键 在酶分子的活性中心处与酶分子结合。抑制剂与底物分子竞争酶的活性中心。若用大写 的英文字母I表示抑制剂,竞争性的抑制作用(competitive inhibition)可用下式表示: 竞争性抑制剂的作用机理,在于它占据了酶分子的活性中心,使酶的活性中心无法 与底物分子结合,因而也就无法催化底物发生反应。这时,抑制剂并没有破坏酶分子的 特定构象,也没有使酶分子的活性中心解体。由于竞争性抑制剂与酶的结合是可逆的, 可用加入大量底物,提高底物竞争力的办法,消除竞争性抑制剂的抑制作用
最典型的竞争性抑制的例子是丙二酸、草酰乙酸、苹果酸对琥珀酸脱氢酶的抑制作 用。琥珀酸脱氢酶可催化琥珀酸脱氢变成延胡索酸,是糖在有氧代谢时三羧酸循环中的 步反应。比较丙二酸、草酰乙酸、苹果酸与琥珀酸的结构式: COOH COOH COOH COOH CH C-0 CHOH COOH COOH COOH COOH 内二酸 草酰乙 苹果酸 玻珀酸 在 非常相似,所以丙二酸、草酰乙酸、苹果酸可作 结合 在此图 d0+ 验结果作的代变化线 达到 需物的浓度明显地增大,即米氏常 Km变 按照推导米氏方程的方法可以导出竞争性抑制作用的速度方程为: V= Km(1+)+S 式中k=E四 设K=K(1+),则V= 式中的Km称表观K 将上式做双倒数处理得下式: 1+)+ 用时对的作图,得相应的Linewever-Burk图(见图4-8直线b)· “无 K。 K‘(变大) 图47竞争性抑制剂对促反应速度的影 117
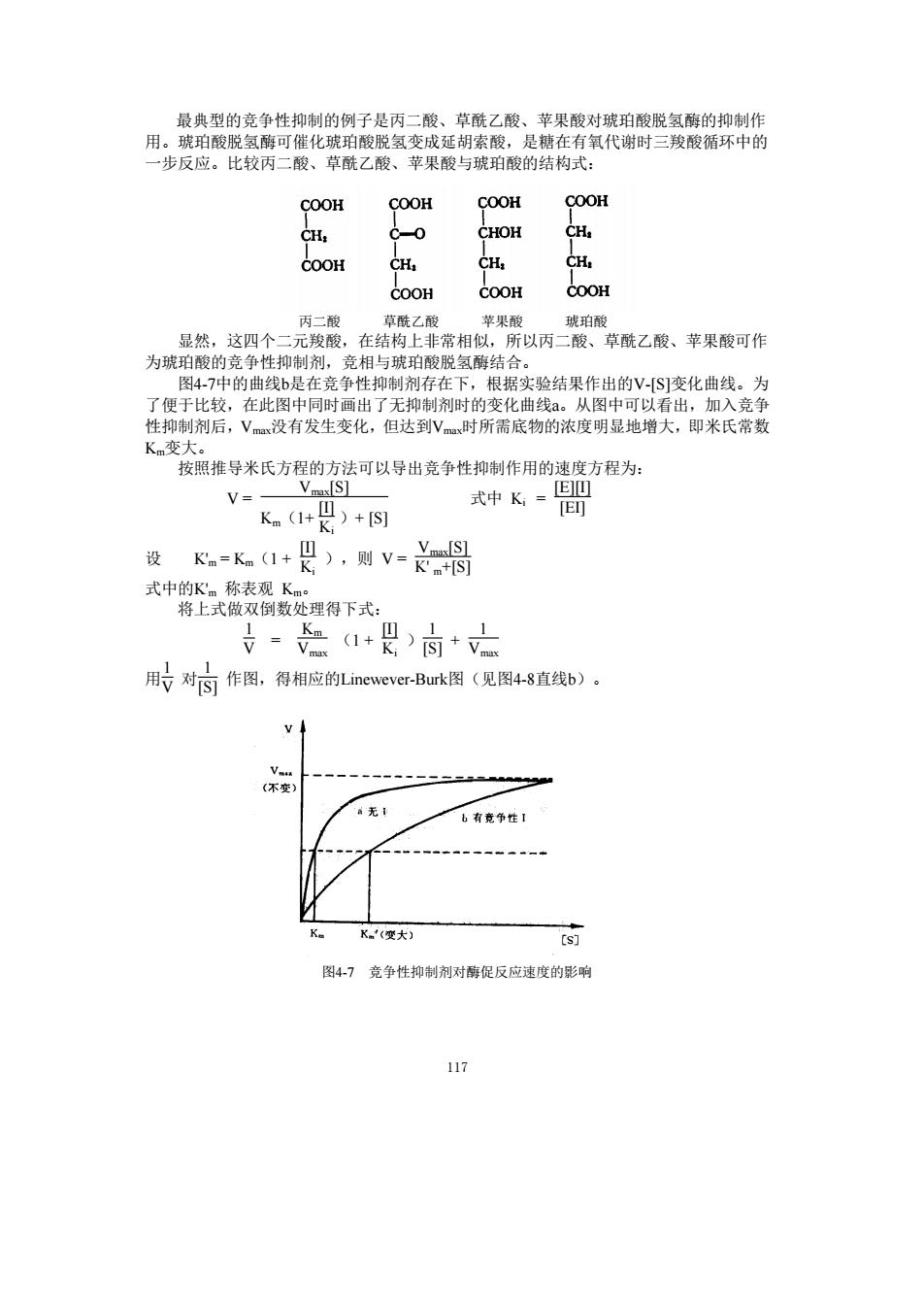
117 最典型的竞争性抑制的例子是丙二酸、草酰乙酸、苹果酸对琥珀酸脱氢酶的抑制作 用。琥珀酸脱氢酶可催化琥珀酸脱氢变成延胡索酸,是糖在有氧代谢时三羧酸循环中的 一步反应。比较丙二酸、草酰乙酸、苹果酸与琥珀酸的结构式: 丙二酸 草酰乙酸 苹果酸 琥珀酸 显然,这四个二元羧酸,在结构上非常相似,所以丙二酸、草酰乙酸、苹果酸可作 为琥珀酸的竞争性抑制剂,竞相与琥珀酸脱氢酶结合。 图4-7中的曲线b是在竞争性抑制剂存在下,根据实验结果作出的V-[S]变化曲线。为 了便于比较,在此图中同时画出了无抑制剂时的变化曲线a。从图中可以看出,加入竞争 性抑制剂后,Vmax没有发生变化,但达到Vmax时所需底物的浓度明显地增大,即米氏常数 Km变大。 按照推导米氏方程的方法可以导出竞争性抑制作用的速度方程为: V = Vmax[S] Km(1+ [I] Ki )+ [S] 式中 Ki = [E][I] [EI] 设 K'm = Km(1 + [I] Ki ),则 V = Vmax[S] K' m+[S] 式中的K'm 称表观 Km。 将上式做双倒数处理得下式: 1 V = Km Vmax (1 + [I] Ki ) 1 [S] + 1 Vmax 用 1 V 对 1 [S] 作图,得相应的Linewever-Burk图(见图4-8直线b)。 图4-7 竞争性抑制剂对酶促反应速度的影响