
第二部分生物化学基本实验 这部分内容为配合生物化学基本技术和技能训练,验证理论教学所设计的基本实验:内容 安排上以生物化学的理论系统为顺序,每个实验包括基本原理、 试剂、主要器材、操作步骤、结果、计算及正常值等,使学生能在实验前对实验有概括性的了解。 试剂部分介绍实验中所需用的全部试剂及配制保管方法,水溶液仅注明浓度,非水溶液均有注解。 在配制方法中所列出的量仅表示在配制过程中的数量关系,而非实验的实际需要量,实际的需要 量需按参加实验的人数,并考虑一定的耗损比例,按配制方法另行计算。器材部分仅列出需在实 验室配备和临时分发的主要器材设备,常用的仪器已在仪器单中列出,器材项内不再包括。操作 部分介绍进行实验的过程,计算方法。注意事项中所讨论的内容应在实验过程中随时注意,使实 验能顺利进行。 实验1铜的比色测定 原理」 氢氧化铵作为显色剂与Cu2*结合成深蓝色的铜氨络离子CuNH)HP,其颜色的深浅与Cu2+ 浓度呈正比关系,与同样处理的标准液进行比色,可求得待测液中C*的含量。 试剂 1.氢氧化铵溶液(氨水溶液):2mo/L 2.标准Cu2*溶液(100mg%):称取3.927g化学纯CuS045H0置于100ml容量瓶中,加40ml 水溶解,再加入5ml浓HSO:防止铜盐水解,最后加水至刻度并充分混匀。 [主要器材 1.试管及试管架 2.刻度吸量管 3.721型分光光度计 [操作步骤剽
第二部分 生物化学基本实验 这部分内容为配合生物化学基本技术和技能训练,验证理论教学所设计的基本实验;内容 安排上以生物化学的理论系统为顺序,每个实验包括基本原理、 试剂、主要器材、操作步骤、结果、计算及正常值等,使学生能在实验前对实验有概括性的了解。 试剂部分介绍实验中所需用的全部试剂及配制保管方法,水溶液仅注明浓度,非水溶液均有注解。 在配制方法中所列出的量仅表示在配制过程中的数量关系,而非实验的实际需要量,实际的需要 量需按参加实验的人数,并考虑一定的耗损比例,按配制方法另行计算。器材部分仅列出需在实 验室配备和临时分发的主要器材设备,常用的仪器已在仪器单中列出,器材项内不再包括。操作 部分介绍进行实验的过程,计算方法。注意事项中所讨论的内容应在实验过程中随时注意,使实 验能顺利进行。 实验 1 铜的比色测定 [原理] 氢氧化铵作为显色剂与 Cu2+结合成深蓝色的铜氨络离子[Cu(NH3)4] 2+,其颜色的深浅与 Cu2+ 浓度呈正比关系,与同样处理的标准液进行比色,可求得待测液中 Cu2+的含量。 [试剂] 1. 氢氧化铵溶液(氨水溶液): 2mol/L 2.标准 Cu2+溶液(100mg%):称取 3.927g 化学纯 CuSO4 .5H2O 置于 100ml 容量瓶中,加 40ml 水溶解,再加入 5ml 浓 H2SO4 防止铜盐水解,最后加水至刻度并充分混匀。 [主要器材] 1. 试管及试管架 2. 刻度吸量管 3.721 型分光光度计 [操作步骤]
取试管3支,编号,按表4操作: 表4 试剂(ml) 空白(B)标准(S)测定(U 未知Cu2*溶液 0.5 标准Cu2*溶液(100mg%) 0.5 蒸馏水 2.5 2.0 2.0 NHOH (2mol/L) 2.0 2.0 2.0 室温充分混匀,在58Onm波长处,以空白管调零,读取各管OD值。 [结果计算 Cu2mg%测定管光密度 ×100 标准管光密度 [注意事项 1.测定用玻璃器皿必须用去离子水冲洗干净,不得有离子污染。 2.标准C+溶液有较强的酸性,而氢氧化铵溶液有较强的碱性,使用时应注意安全。 实验2肝组织中核酸的分离和核酸组分的鉴定 [原理] 动物肝组织中的核蛋白可用水提取,用酚破坏核酸与蛋白质之间的结合键,再用乙醚抽提除 去蛋白质及其杂质,最后用乙醇沉淀核酸。 核酸(DNA和RNA)可被酸水解成磷酸、有机碱(嘌呤碱和嘧啶碱)以及戊糖(核糖和脱 氧核糖)。它们分别可用下列方法鉴定: 1.磷酸的鉴定:磷酸能与钼酸试剂作用生成磷钼酸,后者在还原剂氨基茶酚磺酸钠的作用 下还原成蓝色的钼蓝。 H3PO4+12H2MoO4- 一HP04-12MoO312H20 磷酸钼酸 磷钼酸 2
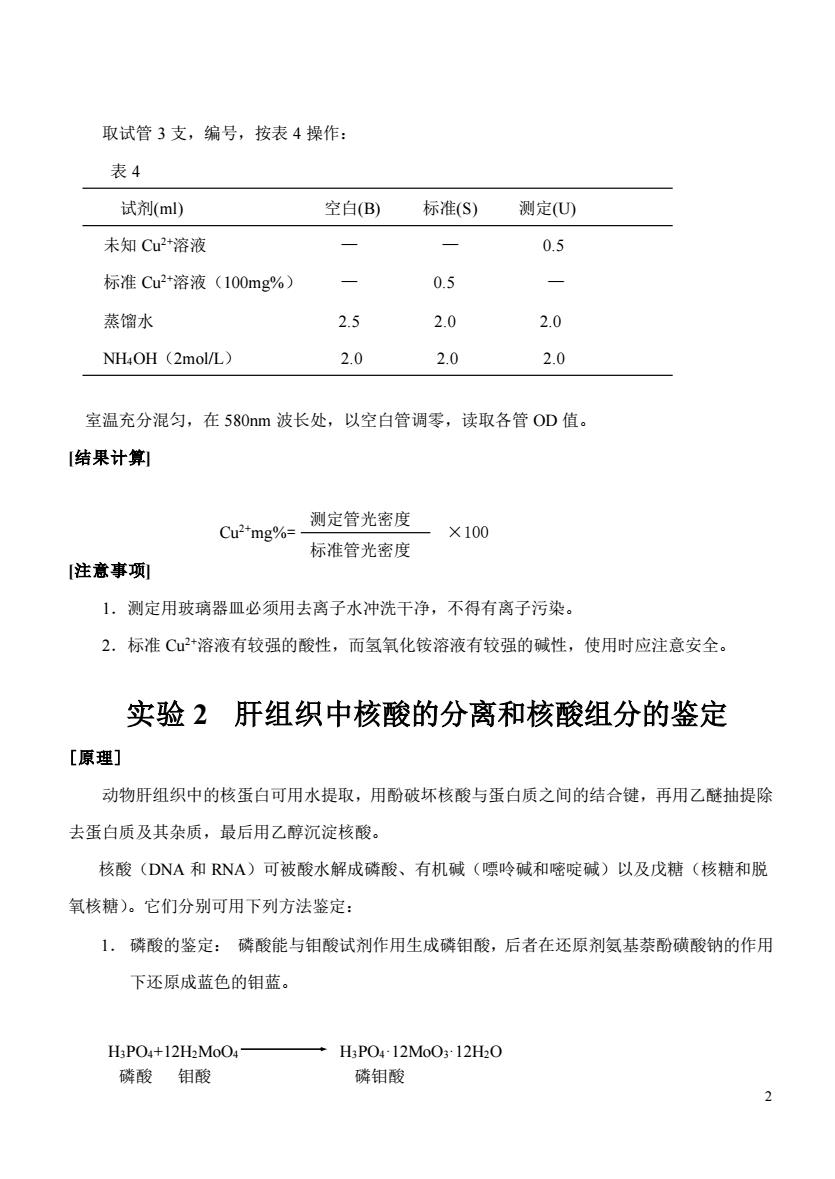
2 取试管 3 支,编号,按表 4 操作: 表 4 试剂(ml) 空白(B) 标准(S) 测定(U) 未知 Cu2+溶液 — — 0.5 标准 Cu2+溶液(100mg%) — 0.5 — 蒸馏水 2.5 2.0 2.0 NH4OH(2mol/L) 2.0 2.0 2.0 室温充分混匀,在 580nm 波长处,以空白管调零,读取各管 OD 值。 [结果计算] Cu2+mg%= ×100 [注意事项] 1.测定用玻璃器皿必须用去离子水冲洗干净,不得有离子污染。 2.标准 Cu2+溶液有较强的酸性,而氢氧化铵溶液有较强的碱性,使用时应注意安全。 实验 2 肝组织中核酸的分离和核酸组分的鉴定 [原理] 动物肝组织中的核蛋白可用水提取,用酚破坏核酸与蛋白质之间的结合键,再用乙醚抽提除 去蛋白质及其杂质,最后用乙醇沉淀核酸。 核酸(DNA 和 RNA)可被酸水解成磷酸、有机碱(嘌呤碱和嘧啶碱)以及戊糖(核糖和脱 氧核糖)。它们分别可用下列方法鉴定: 1. 磷酸的鉴定: 磷酸能与钼酸试剂作用生成磷钼酸,后者在还原剂氨基萘酚磺酸钠的作用 下还原成蓝色的钼蓝。 H3PO4+12H2MoO4 H3PO4·12MoO3·12H2O 磷酸 钼酸 磷钼酸 标准管光密度 测定管光密度

6H+H3PO412MoO312H2O- -H3PO46MoO33MoOs-12H2O+3H2O 磷钼酸 还原剂 钼蓝 2.嘌吟碱的鉴定:嘌吟碱能与苦味酸作用形成针状结晶。 3.核糖的鉴定:核糖与强酸共热生成糠醛,后者与苔黑酚(3,5.-二羟甲苯,orcinol)反应, 缩合成绿色化合物 H -OH HO- 浓硫酸 0 H-C-HC +3H0 △ OH OH H 核糖 OH OH 糠醛 3,5-二羟甲苯 绿色化合物 4.脱氧核糖的鉴定脱氧核糖在强酸中加热可生成。-羟基-Y-酮基戊醛,后者与二苯胺 作用生成蓝色化合物。 CHO CHO CH2 CHOH 强酸 CH2 +H2O △ CHOH C-0 CH2OH CH2OH 脱氧核糖 @羟基-Y酮基戊醛
3 6H+H3PO4·12MoO3·12H2O H3PO4·6MoO3·3MoO5·12H2O+3H2O 磷钼酸 钼蓝 2.嘌呤碱的鉴定: 嘌呤碱能与苦味酸作用形成针状结晶。 3.核糖的鉴定: 核糖与强酸共热生成糠醛,后者与苔黑酚(3,5,-二羟甲苯,orcinol)反应, 缩合成绿色化合物。 4. 脱氧核糖的鉴定 脱氧核糖在强酸中加热可生成ω-羟基-γ-酮基戊醛,后者与二苯胺 作用生成蓝色化合物。 还原剂 OH CH3 H HO O O —C H3C OH O CH3 O —C 糠醛 3,5-二羟甲苯 绿色化合物 + CH2 CHO CHOH CHOH CH2OH CH2 CHO CH2 C=O CH2OH +H2O 强酸 脱氧核糖 -羟基--酮基戊醛 OH OH H H HO—C C—OH H—C—H C—C H 核糖 O 浓硫酸 H O O —C +3H2O 糠醛 H

CHO CH2 《NC →蓝色化合物 0-0 CH2OH -羟基-Y酮基戊醛 二苯胺 试剂 (一)90%苯酚溶液。 (二)乙醚。 (三)95%乙醇 (四)5%疏酸 (五)钼酸试剂钼酸铵5g溶于100ml蒸馏水中,再加入浓硫酸15ml,冷却后加蒸馏水至 1000ml。冷处保存(一个月内稳定)。 (六)氨基萘酚磺酸钠溶液1,2,4氨基萘酚磺酸钠0.5g溶于195ml15%亚硫酸氢钠与5ml 20%亚硫酸钠溶液中,加塞振摇助溶。贮存于棕色瓶中,冰箱保存(可用4周)用时取上清液。 (七)饱和苦味酸溶液苦味酸约13g溶于100ml蒸馏水中,静置过夜。临用前取上清液。 (八)Bial试剂苔黑酚1.5g加入浓盐酸500ml中,再加10%氯化高铁20-30滴。临用前配 制,冰箱保存。 (九)二苯胺试剂取二苯胺1g溶于100ml冰醋酸中,加入浓硫酸2.75ml,临用前配制, 贮于棕色瓶中。 [主要器材打 (一)离心机 (二)沸水浴 (三)研钵 [操作步骤] (一)肝组织中核酸的提取:按以下流程操作:
4 [试剂] (一)90%苯酚溶液。 (二)乙醚。 (三)95%乙醇。 (四)5%硫酸 (五)钼酸试剂 钼酸铵 5g 溶于 100ml 蒸馏水中,再加入浓硫酸 15ml,冷却后加蒸馏水至 1000ml。冷处保存(一个月内稳定)。 (六)氨基萘酚磺酸钠溶液 1,2,4-氨基萘酚磺酸钠 0.5g 溶于 195ml 15%亚硫酸氢钠与 5ml 20%亚硫酸钠溶液中,加塞振摇助溶。贮存于棕色瓶中,冰箱保存(可用 4 周)用时取上清液。 (七)饱和苦味酸溶液 苦味酸约 1.3g 溶于 100ml 蒸馏水中,静置过夜。临用前取上清液。 (八)Bial 试剂 苔黑酚 1.5g 加入浓盐酸 500ml 中,再加 10%氯化高铁 20~30 滴。临用前配 制,冰箱保存。 (九)二苯胺试剂 取二苯胺 1g 溶于 100ml 冰醋酸中,加入浓硫酸 2.75ml,临用前配制, 贮于棕色瓶中。 [主要器材] (一)离心机 (二)沸水浴 (三)研钵 [操作步骤] (一) 肝组织中核酸的提取:按以下流程操作: CH2 CHO CH2 C=O CH2OH N H -羟基--酮基戊醛 二苯胺 + 蓝色化合物
肝润(约1g,置研体中) 加少量净沙研磨至糊状 加蒸馏水3ml,研磨3min 加90%苯酚5ml,研磨10min(移入玻璃小试管) 离心5min(3000r/min,) 上层液(移至塑料小试管) 下层液 加乙酰2ml,试管口覆盖聚乙烯膜、用拇指将管口 按住,用力振摇1-2min(或用玻棒搅拌) 离心5min(3000r/min) 上清液 中层液 下层液(全部移至塑料小试管) 加95%乙醇2ml(用玻棒搅拌约2min) 离心3min(3000r/min) 上清液 阮淀 |加5%H2S044ml (二)核酸水解: !(移至玻璃大试管)置沸水浴15min 核酸水解液 (三)核酸组分的鉴定 核酸水解液用流水冷却后进行定性鉴定。 1.磷酸的鉴定:试管2支、标号,按表5操作: 表5 试剂(滴) 测定管对照管 核酸水解液 10 5%陆移 10 钼酸试剂 氨基萘酚磺酸钠溶液 4 4
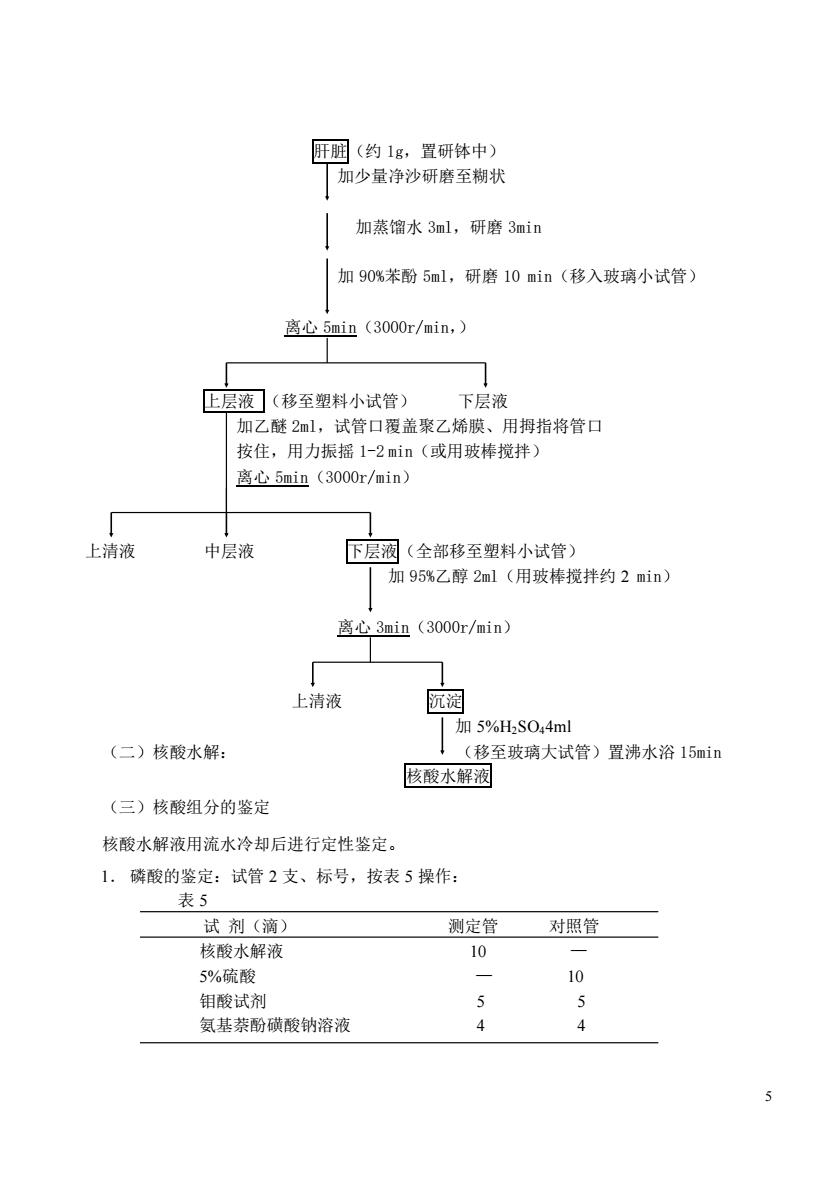
5 肝脏(约 1g,置研钵中) 加少量净沙研磨至糊状 加蒸馏水 3ml,研磨 3min 加 90%苯酚 5ml,研磨 10 min(移入玻璃小试管) 离心 5min(3000r/min,) 上层液 (移至塑料小试管) 下层液 加乙醚 2ml,试管口覆盖聚乙烯膜、用拇指将管口 按住,用力振摇 1-2 min(或用玻棒搅拌) 离心 5min(3000r/min) 上清液 中层液 下层液(全部移至塑料小试管) 加 95%乙醇 2ml(用玻棒搅拌约 2 min) 离心 3min(3000r/min) 上清液 沉淀 加 5%H2SO44ml (二)核酸水解: (移至玻璃大试管)置沸水浴 15min 核酸水解液 (三)核酸组分的鉴定 核酸水解液用流水冷却后进行定性鉴定。 1. 磷酸的鉴定:试管 2 支、标号,按表 5 操作: 表 5 试 剂(滴) 测定管 对照管 核酸水解液 10 — 5%硫酸 — 10 钼酸试剂 5 5 氨基萘酚磺酸钠溶液 4 4