
全程设计 实验活动 简单配合物的形成
实验活动 简单配合物的形成

导航 一、实验准备 (一)实验目的 1.加深对配合物的认识。 2.了解配合物的形成。 3.探究简单离子与配离子的区别
导航 一、实验准备 (一)实验目的 1.加深对配合物的认识。 2.了解配合物的形成。 3.探究简单离子与配离子的区别

二)实验原理 配合物是由中心原子或离子与一定数目的中性分子或阴离子 以配位键结合而形成的一类化合物。中心离子形成配合物后 性质不同于原来的金属离子,具有新的化学特性。 (三)实验用品 1.仪器:试管、胶头滴管。 2.药品:硫酸铜溶液、氨水、硝酸银溶液、氯化钠溶液、氯 化铁溶液、硫氰化钾溶液、K3F(CN)6溶液、蒸馏水、乙 醇
导航 (二)实验原理 配合物是由中心原子或离子与一定数目的中性分子或阴离子 以配位键结合而形成的一类化合物。中心离子形成配合物后 性质不同于原来的金属离子,具有新的化学特性。 (三)实验用品 1.仪器:试管、胶头滴管。 2.药品:硫酸铜溶液、氨水、硝酸银溶液、氯化钠溶液、氯 化铁溶液、硫氰化钾溶液、K3 [Fe(CN)6 ]溶液、蒸馏水、乙 醇

导航 探究过程 (一)实验步骤及分析解释 1.简单配合物的形成。 序号 实验步骤 实验现象 解释 向盛有硫酸铜 溶液的试管里 Cu2++2NH3H2O-- (1) 出现蓝色沉淀 加入氨水 Cu(OH)24+2NH4
导航 二、探究过程 (一)实验步骤及分析解释 1.简单配合物的形成。 序号 实验步骤 实验现象 解释 (1) 向盛有硫酸铜 溶液的试管里 加入氨水 出现蓝色沉淀 Cu2++2NH3·H2O== Cu(OH)2↓+2 N𝐇𝟒 +
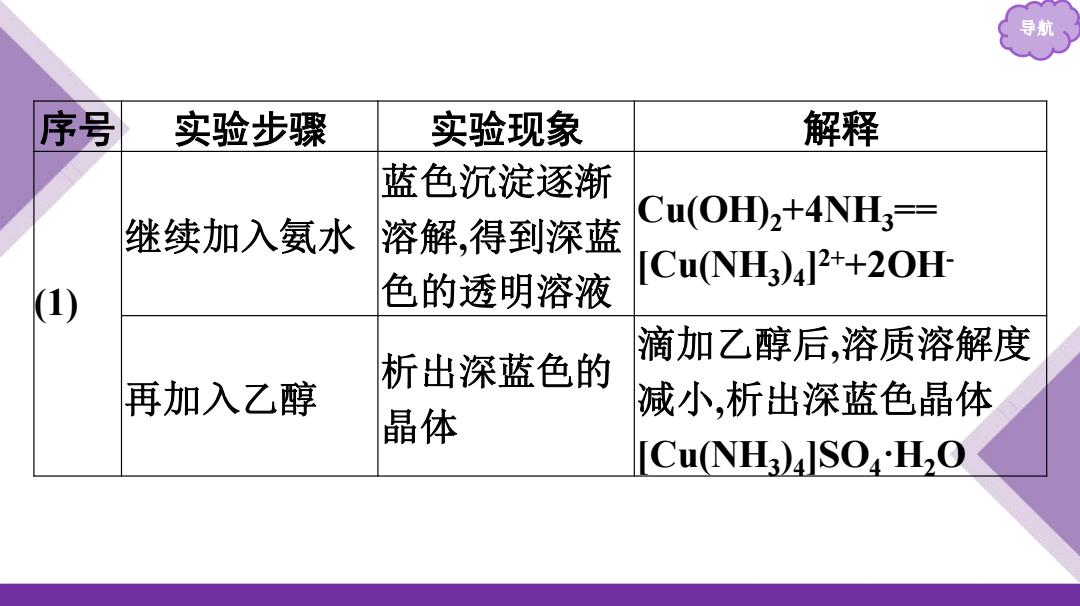
导航 序号 实验步骤 实验现象 解释 蓝色沉淀逐渐 Cu(H),+4NH== 继续加入氨水 溶解,得到深蓝 色的透明溶液 [CuNH3)4]2+20H (1) 滴加乙醇后,溶质溶解度 析出深蓝色的 再加入乙醇 减小,析出深蓝色晶体 晶体 CuNH3)JSOH2O
导航 序号 实验步骤 实验现象 解释 (1) 继续加入氨水 蓝色沉淀逐渐 溶解,得到深蓝 色的透明溶液 Cu(OH)2+4NH3 == [Cu(NH3 )4 ] 2++2OH- 再加入乙醇 析出深蓝色的 晶体 滴加乙醇后,溶质溶解度 减小,析出深蓝色晶体 [Cu(NH3 )4 ]SO4·H2O