第三章:共价键和双原子分子的结构 3.3MO理论和双原子分子的结构 分子轨道理论的基本要点 下图业为s轨道,为p轨道,键轴为Z。各有一 半区域为同号重叠,另一半为异号重叠,两者正好抵 消,净成键效应为零,因此不能组成分子轨道,亦称 两个原子轨道对称性不匹配而不能组成分子轨道。 对称性不匹配,B=0 6
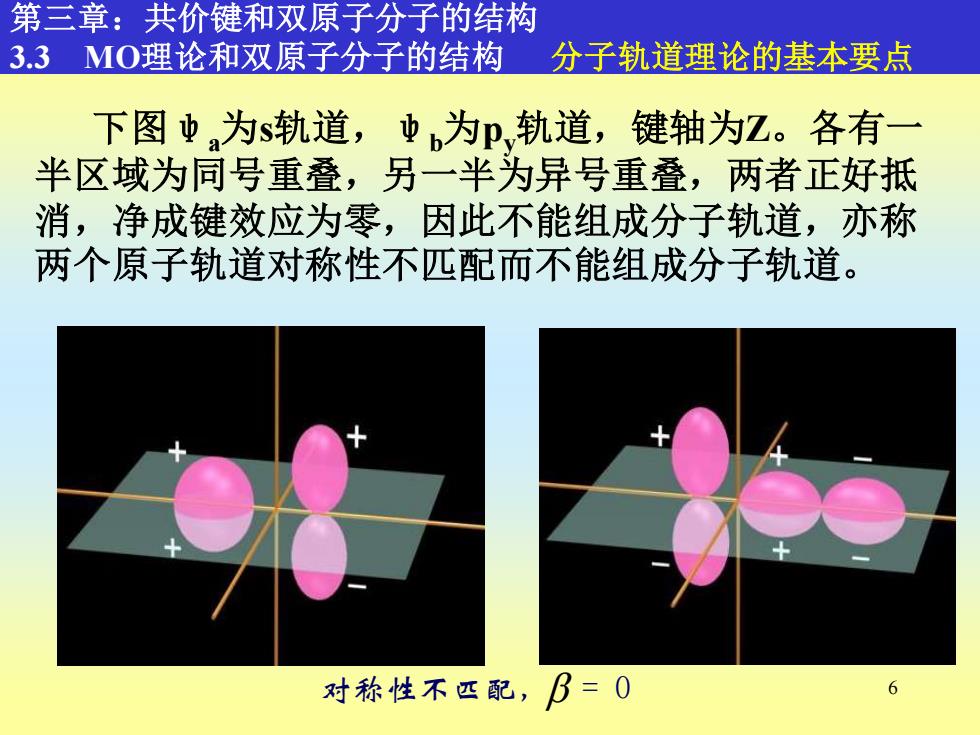
6 第三章:共价键和双原子分子的结构 3.3 MO理论和双原子分子的结构 分子轨道理论的基本要点 下图ψa为s轨道,ψb为py轨道,键轴为Z。各有一 半区域为同号重叠,另一半为异号重叠,两者正好抵 消,净成键效应为零,因此不能组成分子轨道,亦称 两个原子轨道对称性不匹配而不能组成分子轨道。 对称性不匹配, = 0
第三章:共价键和双原子分子的结构 33MO理论和双原子分子的结构分子轨道理论的基本要点 (2)能量相近原则:只有能量相近的原子轨道才能组合 成有效的分子轨道。能量愈相近,组成的分子轨道越有 效。若两条原子轨道相差很大,则不能组成分子轨道。 E2 B Cb : B 7
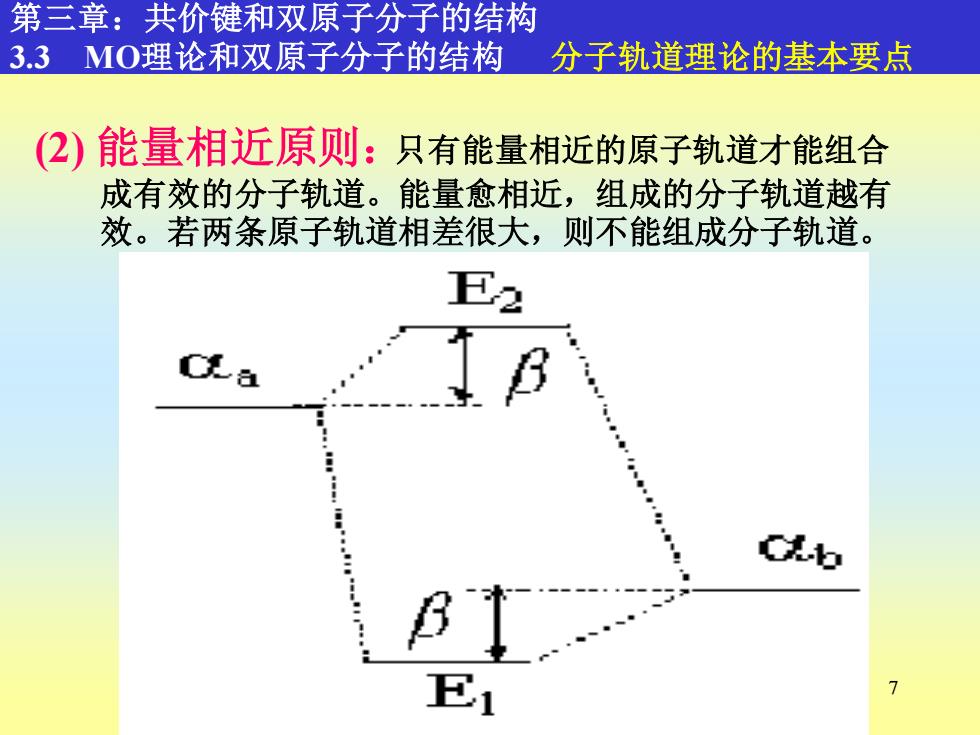
7 只有能量相近的原子轨道才能组合 成有效的分子轨道。能量愈相近,组成的分子轨道越有 效。若两条原子轨道相差很大,则不能组成分子轨道。 第三章:共价键和双原子分子的结构 3.3 MO理论和双原子分子的结构 分子轨道理论的基本要点 (2) 能量相近原则:
第三章:共价键和双原子分子的结构 3.3MO理论和双原子分子的结构 分子轨道理论的基本要点 (3)最大重叠原则:原子轨道发生重叠时,在对称性匹配 的条件下,原子轨道Ψ,和Ψ的重叠程度愈大,成键轨道相对 于组成的原子轨道的能量降低得愈显著,成键效果强,形成的 化学键愈稳定。 a 在核间距不变时,后者有较大重叠,可以形成较强的化学键, 这就是轨道景大重叠原则 成键三个原则:对称性匹配,轨道最大重叠, 能量相近 对称性匹配 是先决条件,决定是否成键 轨道最大重叠,能量相近 等是影响成键效果, 8
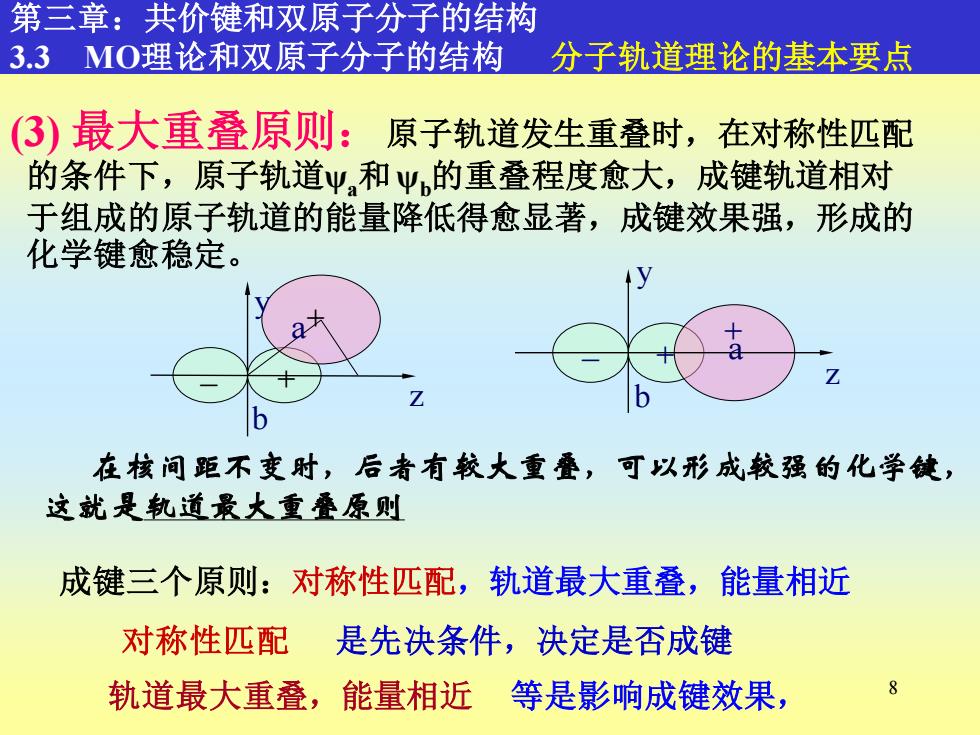
8 原子轨道发生重叠时,在对称性匹配 的条件下,原子轨道ψa和ψb的重叠程度愈大,成键轨道相对 于组成的原子轨道的能量降低得愈显著,成键效果强,形成的 化学键愈稳定。 (3) 最大重叠原则: 第三章:共价键和双原子分子的结构 3.3 MO理论和双原子分子的结构 分子轨道理论的基本要点 成键三个原则:对称性匹配,轨道最大重叠,能量相近 对称性匹配 是先决条件,决定是否成键 轨道最大重叠,能量相近 等是影响成键效果, b + _ y z +a a + + _ y z b 在核间距不变时,后者有较大重叠,可以形成较强的化学键, 这就是轨道最大重叠原则
第三章:共价键和双原子分子的结构 3.3MO理论和双原子分子的结构 分子轨道理论的基本要点 1.c轨道和o键 轨道的分布是圆柱对称的,任意转动键轴,分子轨道的 符号和大小都不变,这样的轨道称为σ轨道。 节面 S轨道与S轨道的组合 H2 墨 H H 6 分子轨道.avi
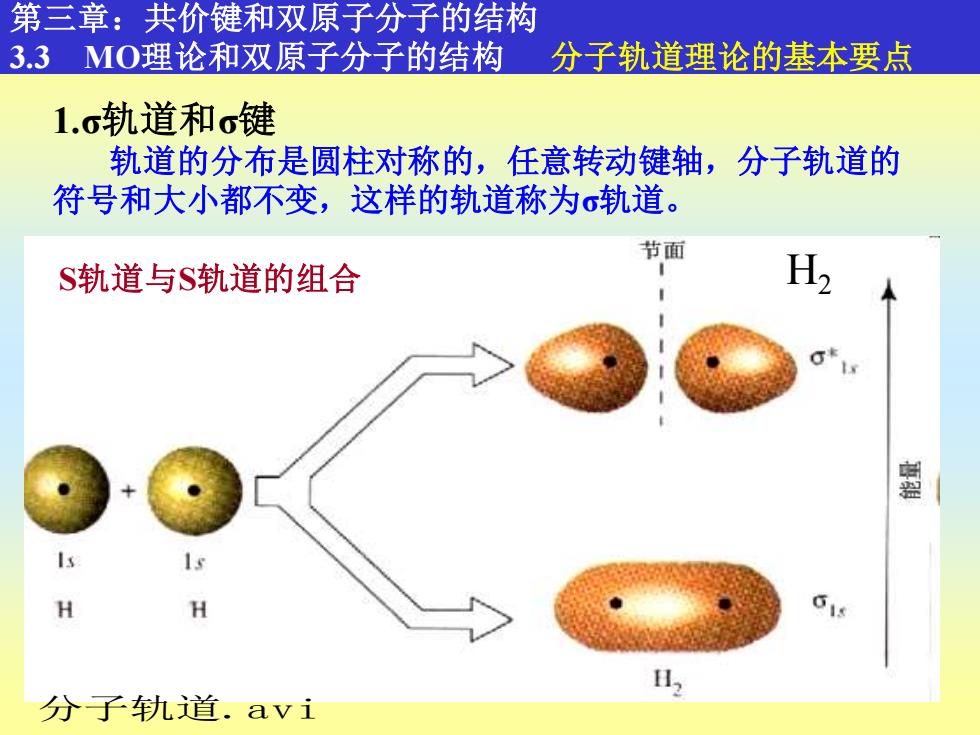
9 第三章:共价键和双原子分子的结构 3.3 MO理论和双原子分子的结构 分子轨道理论的基本要点 1.σ轨道和σ键 轨道的分布是圆柱对称的,任意转动键轴,分子轨道的 符号和大小都不变,这样的轨道称为σ轨道。 S轨道与S轨道的组合 H2 分子轨道.avi
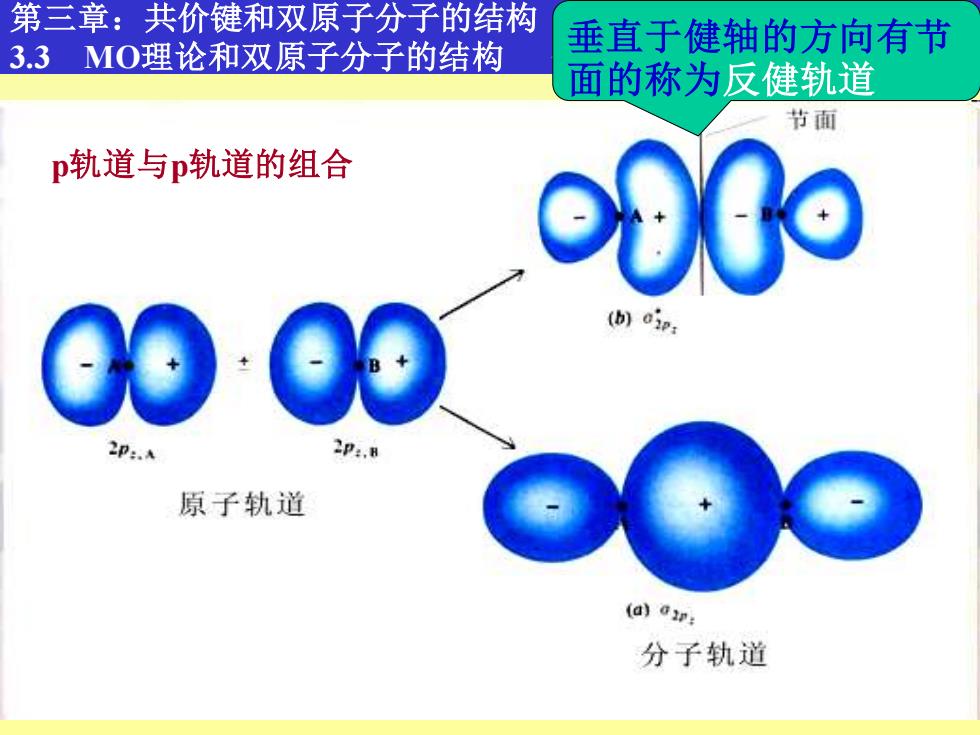
第三章:共价键和双原子分子的结构 垂直于健轴的方向有节 3.3MO理论和双原子分子的结构 面的称为反健轨道 节面 p轨道与p轨道的组合 000 (b)oip p:.A p:. 原子轨道 (a)ar: 分子轨道
10 第三章:共价键和双原子分子的结构 3.3 MO理论和双原子分子的结构 分子轨道理论的基本要点 p轨道与p轨道的组合 垂直于健轴的方向有节 面的称为反健轨道