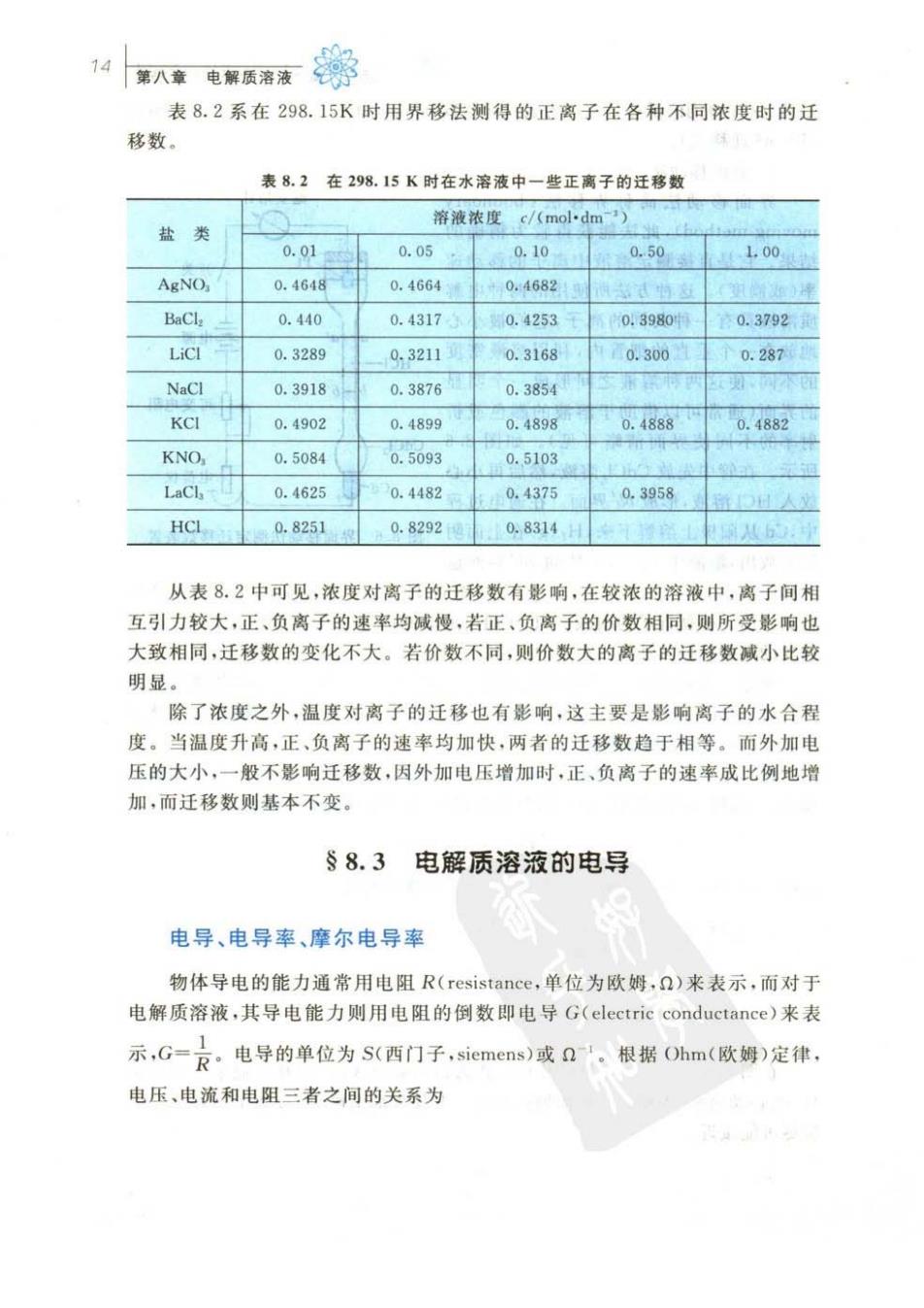
第入车电系质帝度养 14 表8.2系在298.15K时用界移法测得的正离子在各种不同浓度时的迁 移数 表8.2在298,15K时在水溶液中一些正离子的迁移数 溶液浓度c/(mol-dm) 盐类 0.01 0.05 0.10 .0.5014.100 AgNO, 0.4648 0.4664 0.46821 BaCla 0.440 0.4317 0.4253 0.3980 0.3792 0.3289 0.3211 0.3168 0.300 0.287 NaCl 0.3918 0.3876 0.3854 KCI 0.4902 0.4899 0.4898 0.4888 0.4882 KNO. 0.5084 0.5093 0.5103 LaCl 0.4625 0.4482 0.4375 0.3958 HC10.82510.8292地0.8314H 从表8.2中可见,浓度对离子的迁移数有影响,在较浓的溶液中,离子间相 互引力较大,正、负离子的速率均减慢,若正、负离子的价数相同,则所受影响也 大致相同,迁移数的变化不大。若价数不同,则价数大的离子的迁移数减小比较 明显。 除了浓度之外,温度对离子的迁移也有影响,这主要是影响离子的水合程 度。当温度升高,正、负离子的速率均加快,两者的迁移数趋于相等。而外加电 压的大小,一般不影响迁移数,因外加电压增加时,正、负离子的速率成比例地增 加,而迁移数则基本不变。 §8.3电解质溶液的电导 电导、电导率、摩尔电导率 物体导电的能力通常用电阻R(resistance,单位为欧姆,)来表示,而对于 电解质溶液,其导电能力则用电阻的倒数即电导G(electric conductance)来表 示,G=是。电导的单位为S(西门子,siemens)或'。根据Ohm(欧姆)定律。 电压、电流和电阻三者之间的关系为
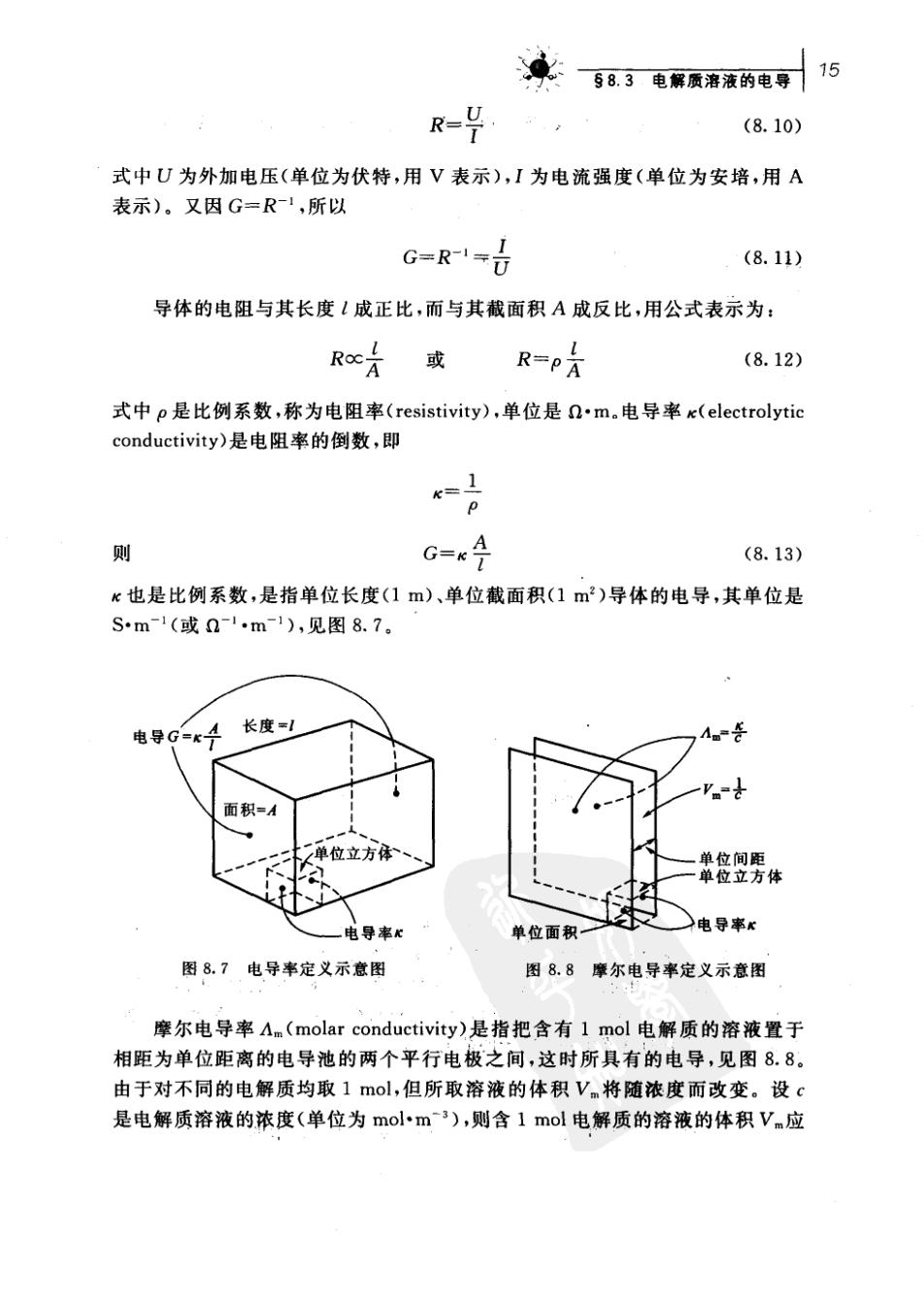
、百8,3电解质溶液的电导15 R=9 (8.10) 式中U为外加电压(单位为伏特,用V表示),I为电流强度(单位为安培,用A 表示)。又因G=R,所以 G=R1=司 (8.11) 导体的电阻与其长度1成正比,而与其截面积A成反比,用公式表示为: Roc斤 或 R=P合 (8.12) 式中p是比例系数,称为电阻率(resistivity),单位是n~m.电导率x(electrolytic conductivity)是电阻率的倒数,即 则 G=x4 (8.13) x也是比例系数,是指单位长度(1m)、单位截面积(1m2)导体的电导,其单位是 Sm1(或n1m1),见图8.7。 电导G=k4 长度 V a 面积=A 电导率x 单位面积一 芬电导事 图87电导率定义示意图 图8,8摩尔电导率定义示意图 摩尔电导率Am(molar conductivity)是指把含有lmol电解质的溶液置于 相距为单位距离的电导池的两个平行电极之间,这时所具有的电导,见图8.8。 由于对不同的电解质均取1mol,但所取溶液的体积V.将随浓度而改变。设c 是电解质溶液的浓度(单位为mol小·m3),则含1mol电解质的溶液的体积Vm应

16第八童电聚质浩清务 等于二,根据电导率x的定义,摩尔电导率A与电导率心之间的关系用公式表 示为: A det v (8.14) 因为心的单位为S·m',c的单位为mol·m3,所以摩尔电导率A的单位为 Sm2mol。 例题在291K时.浓度为10mol·m的CuS),溶液的电导率为 0.1434Sm,试求CuS),的摩尔电导率A(CS(),)和一CuS),的摩尔电导率 A.(2CuS),). 解 A.(Cuso,)-(CuSo. =0.134m=14.3别×10m2mol 10mol·m A(2Cus0.) (Cuso. 0.1434Sm -2x10 mol-m 17x10S.m.mol 注意:(1)当浓度c的单位是以mol·dm表示时,则要换算成以mom 表示,然后进行计算,即在数字运算的同时,单位也进行运算,才能获得正确的 结果 (2)在使用摩尔电导率这个量时,应将浓度为。的物质的基本单元置于A 后的括号中,以免出错。例如1,A(CuSO)和A(CuS),)都可称为摩尔电导 率,只是所取的基本单元不同,显然A(CS0)=2A(号CuS),) 引入摩尔电导率的概念是很有用的。因为一般电解质的电导率在不太浓的 情况下都随着浓度的增高而变大,因为导电粒子数增加了。为了便于对不同类 型的电解质进行导电能力的比较,人们常选用摩尔电导率,因为这时不但电解质 有相同的量(都含有1m©l的电解质),而且电极间距离也都是单位距离。当然, 在比较时所选取的电解质基本粒子的荷电荷量应相同。 “电导的测定 电导的测定在实验中实际上是测定电阻。随着实验技术的不断发展,目前
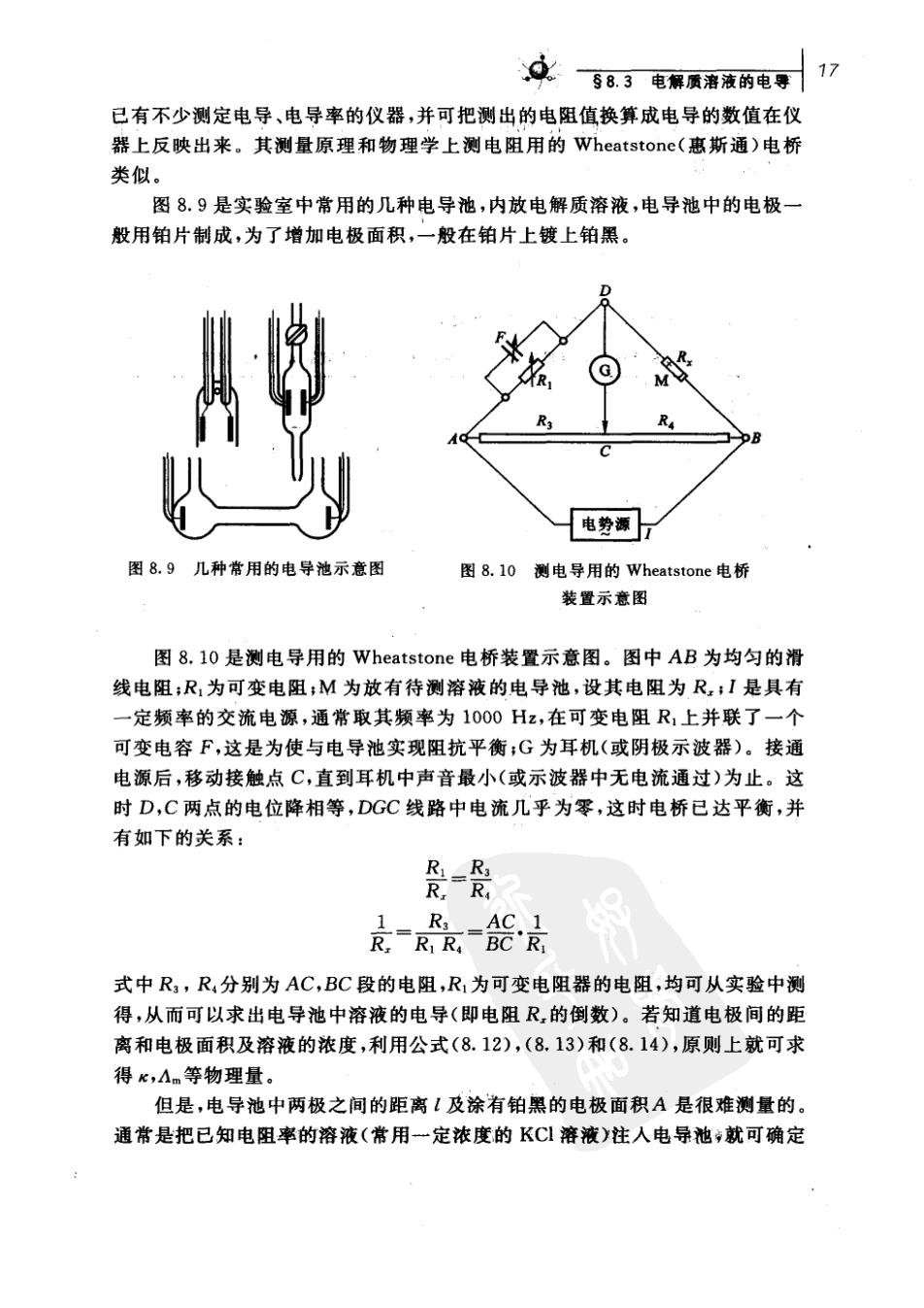
58,号电解质溶液的电零17 已有不少测定电导、电导率的仪器,并可把测出的电阻值换算成电导的数值在仪 器上反映出来。其测量原理和物理学上测电阻用的Wheatstone(惠斯通)电桥 类似。 图8.9是实验室中常用的几种电导池,内放电解质溶液,电导池中的电极 般用铂片制成,为了增加电极面积,一般在铂片上镀上铂黑。 R3 电势源7 图8.9几种带用的电导池示意图 图8.l0测电导用的Wheatstone电桥 装置示意图 图8.10是测电导用的Wheatstone电桥装置示意图。图中AB为均匀的滑 线电阻:R,为可变电阻:M为放有待测溶液的电导池,设其电阻为R:I是具有 一定频率的交流电源,通常取其频率为1000Hz,在可变电阻R:上并联了一个 可变电容F,这是为使与电导池实现阻抗平衡:G为耳机(或阴极示波器)。接通 电源后,移动接触点C,直到耳机中声音最小(或示波器中无电流通过)为止。这 时D,C两点的电位降相等,DGC线路中电流几乎为零,这时电桥已达平衡,并 有如下的关系: 是-受 是-R能最 式中R,R,分别为AC,BC段的电阻,R,为可变电阻器的电阻,均可从实验中测 得,从而可以求出电导池中溶液的电导(即电阻R的倒数)。若知道电极间的距 离和电极面积及溶液的浓度,利用公式(8.12),(8.13)和(8.14),原则上就可求 得,Am等物理量。 但是,电导池中两极之间的距离!及涂有铂黑的电极面积A是很难测量的 通常是把已知电阻率的溶液(常用一定浓度的KC溶液)注入电导池,就可确定
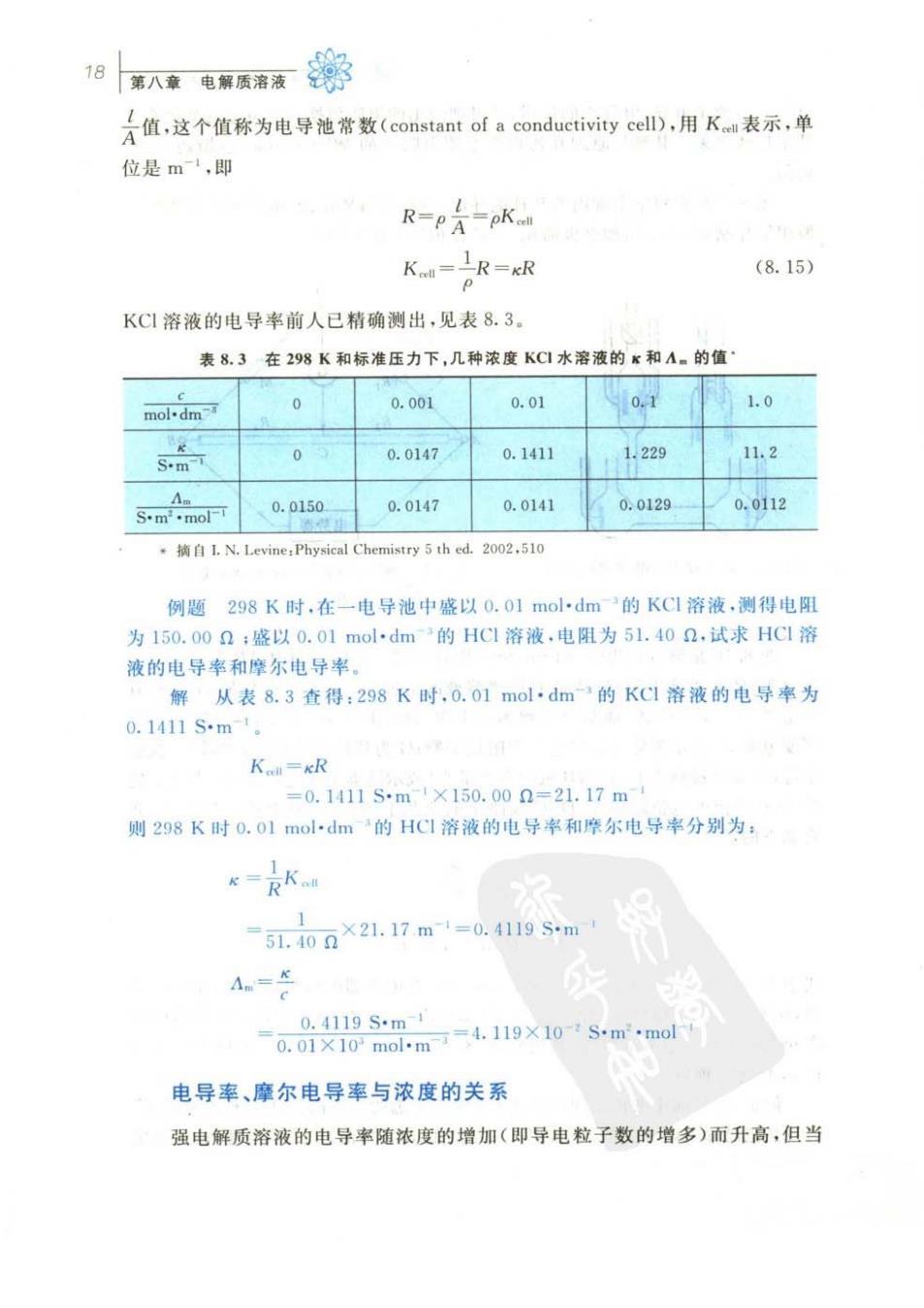
8男八康电彩质语疾第 名值,这个值称为电导池常数(constant ofa conductivity cell),用K表示,单 位是m,即 R-PA-pK Ka-IR-gR (8.15) KC1溶液的电导率前人已精确测出,见表8.3。 表83在298K和标准压力下,几种浓度KC水溶液的K和A。的值 mol.dm 0 0.001 0.01 0.1 1.0 S.m 0.0147 0.1411 1229 11.2 0.015d 0.0147 0.0141 0.0129 0.0112 摘自1.N.Levine,Physical Chemistry5thcd.2002,510 例题298K时,在一电导池中盛以0.01mol·dm的KC1溶液,测得电 为150.000:盛以0.01mol·dm的HC溶液,电阻为5L.402,试求HC1溶 液的电导率和摩尔电导率」 解从表8.3查得:298K时,0.01mol·dm的KC1溶液的电导率为 0.1411Sm Ko=kR =0.1411Sm1×150.000=21.17m 则298K时0.o1mol·dm的HC1溶液的电导率和摩尔电导率分别为 -51.40n×21.17m1=0.41195m -0.01x10m0m=4.19×10 S.mmol 0.4119S.m1 电导率、摩尔电导率与浓度的关系 强电解质溶液的电导率随浓度的增加(即导电粒子数的增多)而升高,但当