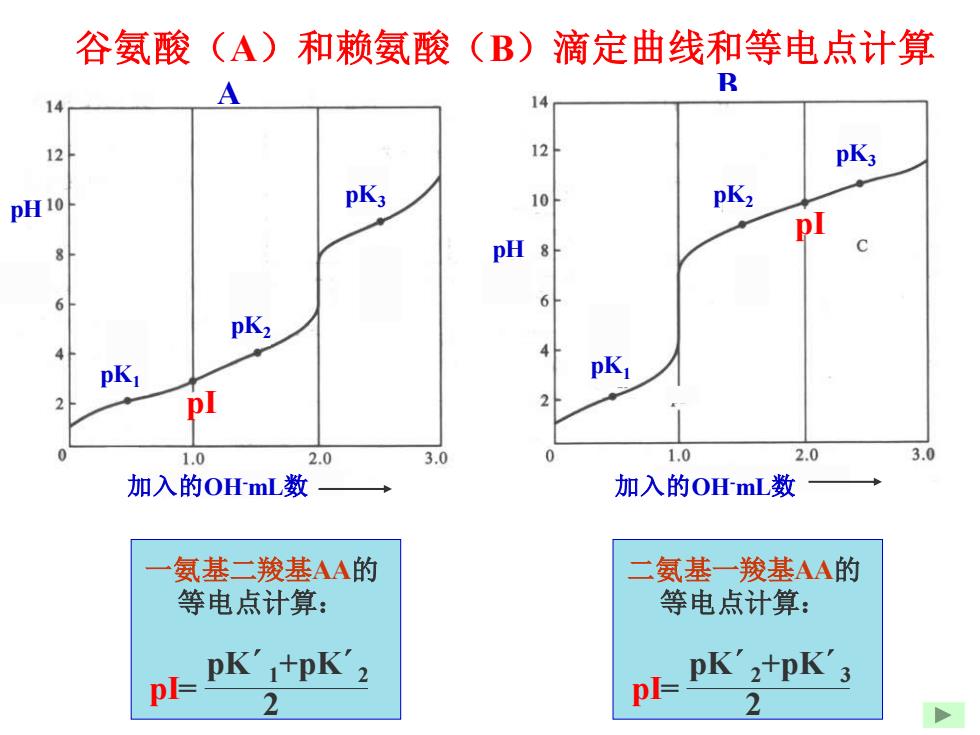
谷氨酸(A)和赖氨酸(B)滴定曲线和等电点计算 A R 12 12 pK3 pH 10 pK3 10 pK2 pI pH 8 6 pK2 pI 1.0 2.0 3.0 1.0 2.0 3.0 加入的OHmL数 加入的OHmL数 氨基二羧基AA的 二氨基一羧基AA的 等电点计算: 等电点计算: p pK'+pK'2 pK'2+pK'3 2 p 2
谷氨酸(A)和赖氨酸(B)滴定曲线和等电点计算 一氨基二羧基AA的 等电点计算: pI= 2 pK´ 1+pK´ 2 二氨基一羧基AA的 等电点计算: pI= 2 pK´ 2+pK´ 3 A B pK1 pK2 pI pI pK3 pK3 pK2 pK1 加入的OH-mL数 加入的OH-mL数 pH pH

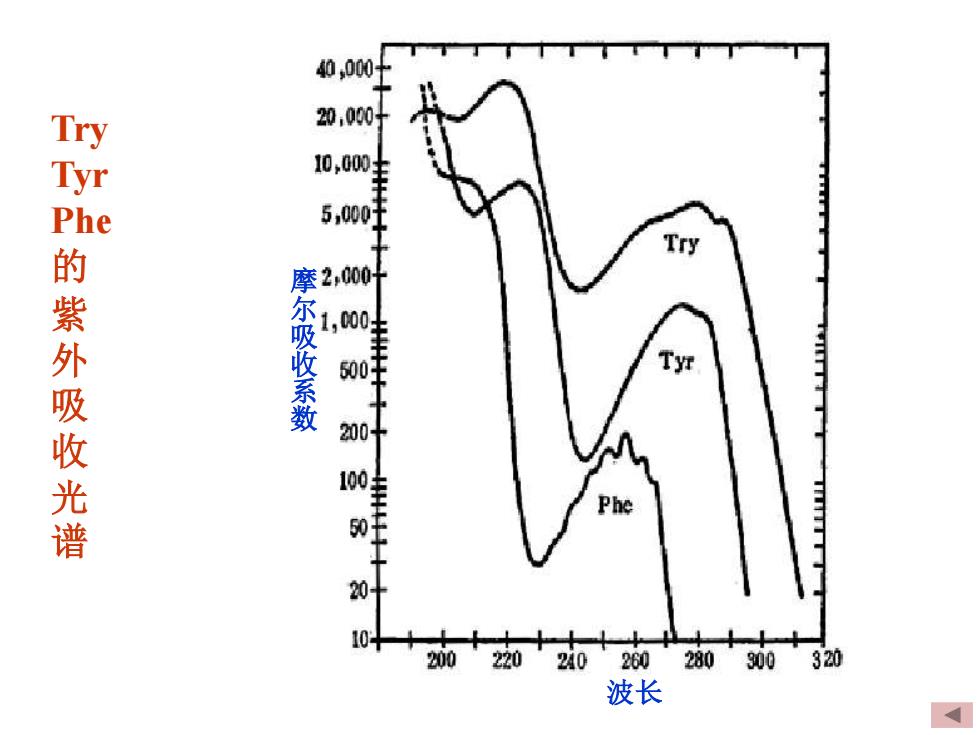
氨基酸光学活性和光谱性质 1、旋光性:除甘氨酸外,所有天然-氨基酸都有不对称碳原子 , 因此所有天然氨基酸都具有旋光性。 2、紫外吸收光谱:参与蛋白质组成的20种氨基酸中色氨酸 (Trp)、酪氨酸(Tyr)和苯丙氨酸(Phe)的R基团中含有苯环共轭双 键系统,在紫外光区显示特征的吸收谱带,最大光吸收(2ax )分别为280、275、和257nm。由于大多数蛋白质都含有这些 氨基酸残基,因此用紫外分光光度法可测定蛋白质含量。 3、核磁共振(nuclear magnetic resonance,.NMR)波谱:原子 核带有正电荷,只要自旋量子数不等于零,其行为就象饶轴自 旋的小磁体,因而能与外加磁场相互作用,产生核磁共振。例 如3H、13C、2H、14H、32P的核都属于这一类
氨基酸光学活性和光谱性质 1、旋光性:除甘氨酸外,所有天然α-氨基酸都有不对称碳原子 ,因此所有天然氨基酸都具有旋光性。 2、紫外吸收光谱:参与蛋白质组成的20种氨基酸中色氨酸 (Trp)、酪氨酸(Tyr)和苯丙氨酸(Phe)的R基团中含有苯环共轭双 键系统,在紫外光区显示特征的吸收谱带,最大光吸收(max )分别为280、275、和257nm。由于大多数蛋白质都含有这些 氨基酸残基,因此用紫外分光光度法可测定蛋白质含量。 3、核磁共振(nuclear magnetic resonance,NMR)波谱:原子 核带有正电荷,只要自旋量子数不等于零,其行为就象饶轴自 旋的小磁体,因而能与外加磁场相互作用,产生核磁共振。例 如3H、 13C、 2H、 14H、 32P的核都属于这一类
10,000 Phe Try 2,0001 紫外吸收光谱 摩尔吸收系数 Tyr Phe 200 260 280 300 320 波长
Try Tyr Phe 的紫外吸收光谱 摩尔吸收系数 波长

的紫外吸收光谱 摩尔吸收系数 波长
Try Tyr Phe 的紫外吸收光谱 摩尔吸收系数 波长
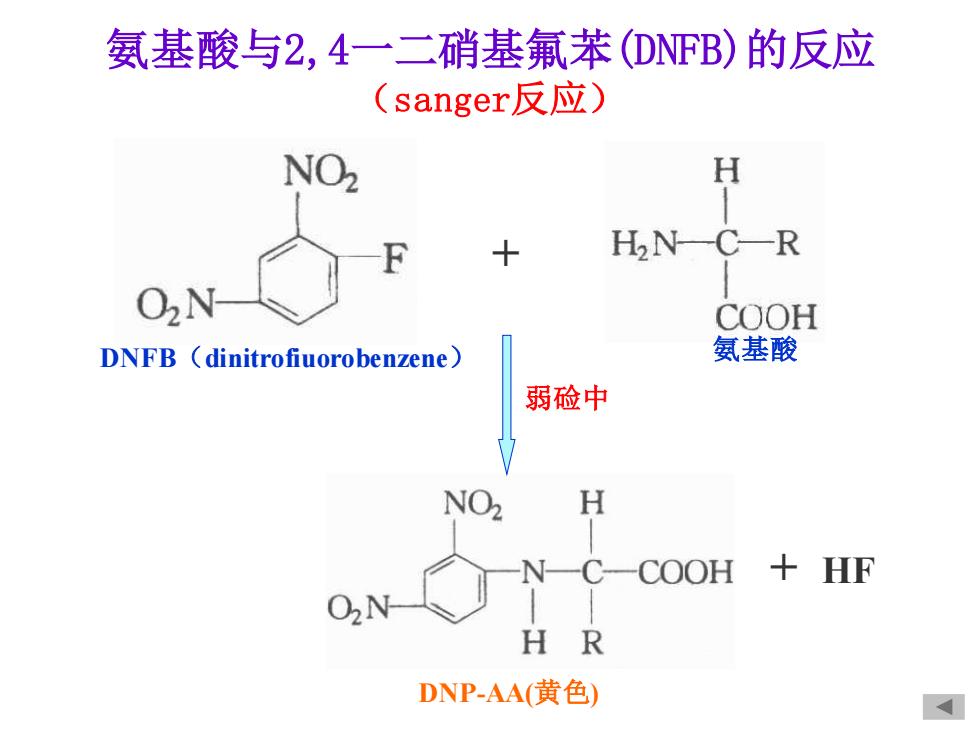
氨基酸与2,4一二硝基氟苯(DNFB)的反应 (sanger,反应) NO2 H HN CR COOH DNFB (dinitrofiuorobenzene) 氨基酸 弱硷中 NO2 H N-C-COOH 十 HF 02N H R DNP-AA(黄色)
氨基酸与2,4一二硝基氟苯(DNFB)的反应 (sanger反应) DNFB(dinitrofiuorobenzene) DNP-AA(黄色) + + HF 弱硷中 氨基酸