
醇、酚和醚 二、醇的物理性质 特点是存在分子间的氢键作用 为什么醇具有较高的沸点?(分子间氢键缔合) R R H H B- 醇分子中烃基对氢键缔合有阻碍作用。 多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5℃ 197C 290°℃
醇、酚和醚 特点是存在分子间的氢键作用 为什么醇具有较高的沸点? (分子间氢键缔合) 醇分子中烃基对氢键缔合有阻碍作用。 多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5 oC 197 oC 290 oC O H R O R H O H R H O R 二、醇的物理性质
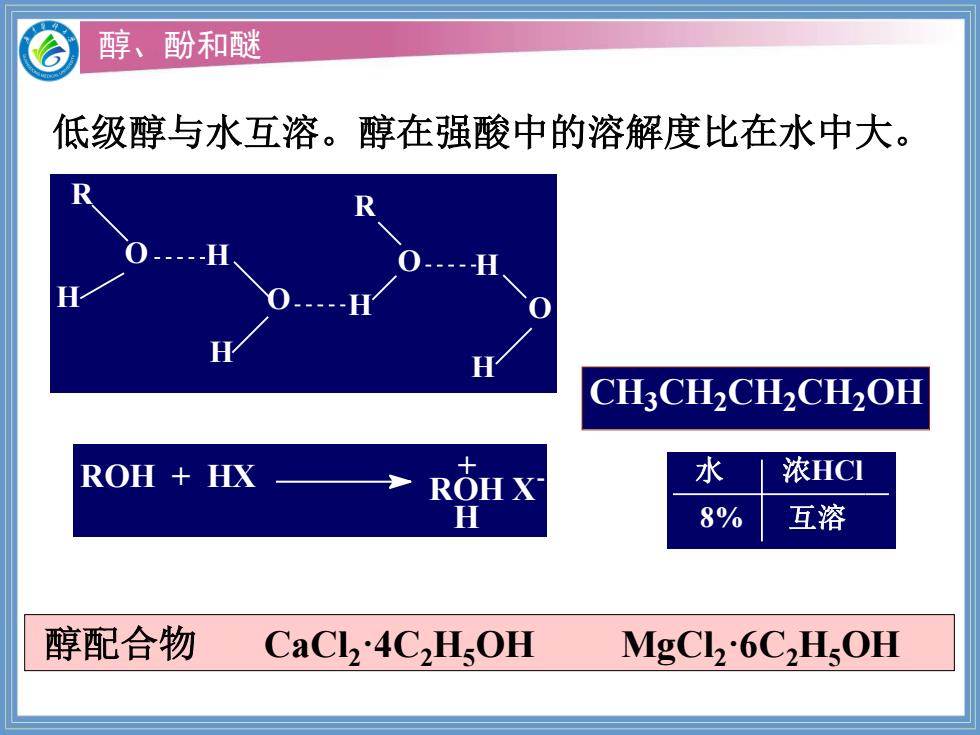
醇、酚和醚 低级醇与水互溶。醇在强酸中的溶解度比在水中大。 R H CH3CH2CH2CH2OH ROH HX ROH X 水 浓HC】 H 8% 互溶 醇配合物 CaCL,4C,H.OH MgCl2·6C,HOH
醇、酚和醚 R O H H O H H O R H O H ROH + HX ROH X - H + CH3CH2CH2CH2OH 水 浓HCl 8% 互溶 醇配合物 CaCl2·4C2H5OH MgCl2·6C2H5OH 低级醇与水互溶。醇在强酸中的溶解度比在水中大
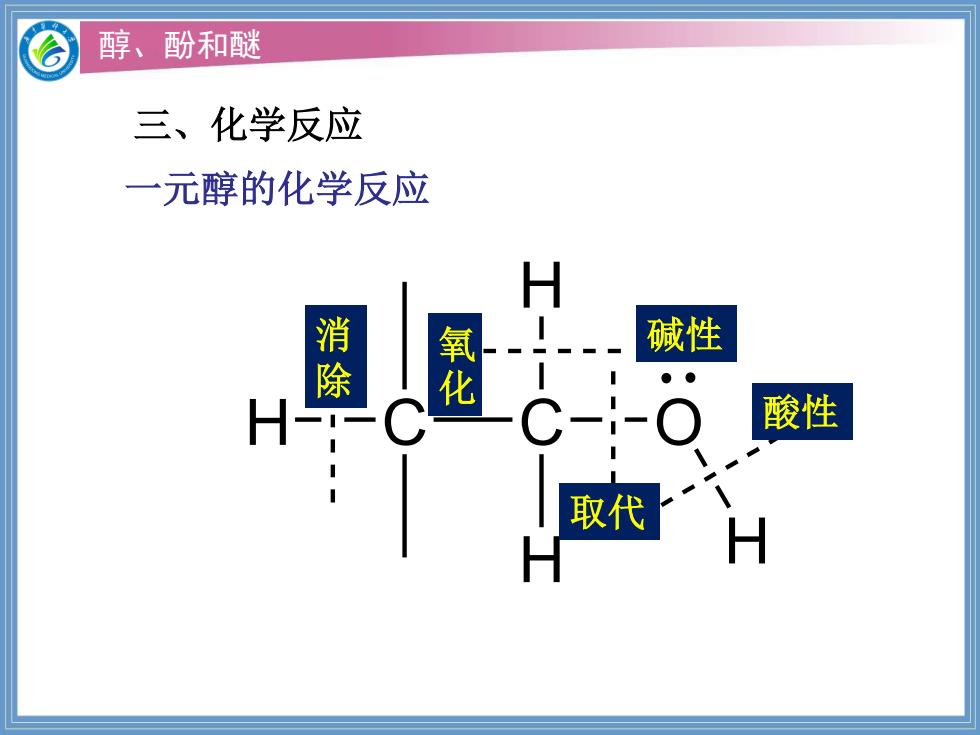
醇、酚和醚 三、化学反应 一元醇的化学反应 H 除 碱性 化 酸性 取代 H
醇、酚和醚 H C C O H H H 消 除 氧 化 取代 酸性 碱性 三、化学反应 一元醇的化学反应

醇、酚和醚 b a G- HH 结构与反应性: a.O-H键极性一 酸性H反应 b.C-O键极性 亲核取代 c.涉及B-H断裂 消除 d.涉及a-H断裂 一氧化
醇、酚和醚 R CH H CH H O H b a c d 结构与反应性: a. O-H键极性——酸性H反应 b. C-O键极性——亲核取代 c. 涉及β-H断裂——消除 d. 涉及 α-H断裂——氧化

醇、酚和醚 (一)酸碱性 (1)酸性 极性键,可异裂 极性键,可异裂 :活泼氢,有酸性 活泼氢,有酸性, H-0-H 68 PKa=14 R-0-H 但酸性更弱(R斥电子) 64 PKa=15-18 ROH Na->RONa + 2州 醇钠 反应活性: 2ROH+Mg→(RO)2Mg+H2 (1)随R↑,反应活性↓ 醇镁 6(CH3)2CHOH 2AI-> (2)CH30H>1°>2°>3R0H 2[(CH3)2CH0]3AI+3H2 (三)异丙醇铝
醇、酚和醚 (一) 酸碱性 PKa=14 PKa=15-18 R O H + − 但酸性更弱(R斥电子) 活泼氢,有酸性 极性键,可异裂 , H O H 极性键,可异裂 − + 活泼氢,有酸性 ROH + Na 2 1 RONa + H2 2ROH + Mg (RO)2Mg + H2 反应活性: CH3OH>1 >2 >3 ROH 。 。 。 (1) 随R ,反应活性 (2) 醇钠 醇镁 2[(CH3)2CHO]3Al + 3H2 6(CH3)2CHOH + 2Al (三)异丙醇铝 (1) 酸性