
导期 2.下列物质发生状态变化时,克服了范德华力的是( ) A.食盐熔化B.HCI溶于水 C.碘升华D.氢氧化钠熔化 答案:C 解析:氯化钠、氢氧化钠均是离子化合物,熔化时离子键断 裂,A、D项错误。HCI溶于水时克服的是共价键,B项错误 碘升华时克服的是范德华力,C项正确
导航 2.下列物质发生状态变化时,克服了范德华力的是( )。 A.食盐熔化 B.HCl溶于水 C.碘升华 D.氢氧化钠熔化 答案:C 解析:氯化钠、氢氧化钠均是离子化合物,熔化时离子键断 裂,A、D项错误。HCl溶于水时克服的是共价键,B项错误。 碘升华时克服的是范德华力,C项正确

导 3.下列关于氢键的说法正确的是( A.由于冰中的水分子间存在氢键,所以其密度大于液态水 B.可以用氢键解释接近沸点的水蒸气的相对分子质量的测定 值比用化学式H,0)计算出来的相对分子质量大 C.分子间氢键和分子内氢键都会使物质的熔、沸点较高 D.水加热到很高的温度都难以分解,这是由于氢键所致 答案:B
导航 3.下列关于氢键的说法正确的是( )。 A.由于冰中的水分子间存在氢键,所以其密度大于液态水 B.可以用氢键解释接近沸点的水蒸气的相对分子质量的测定 值比用化学式(H2O)计算出来的相对分子质量大 C.分子间氢键和分子内氢键都会使物质的熔、沸点较高 D.水加热到很高的温度都难以分解,这是由于氢键所致 答案:B

解析:由于冰中的水分子间存在氢键,增大了水分子之间的距 离,所以其密度小于液态水,A项错误。由于水分子之间存在 氢键,使相当量的水分子因氢键而相互缔合,所以接近沸,点的 水蒸气的相对分子质量的测定值比用化学式H,O)计算出来 的相对分子质量大,B项正确。分子间氢键使物质的熔、沸点 较高,而分子内氢键则会使物质的熔、沸点较低,C项错误。 水加热到很高的温度都难以分解,这是由于分子内的H一O共 价键强的缘故,与分子间的氢键无关,D项错误
导航 解析:由于冰中的水分子间存在氢键,增大了水分子之间的距 离,所以其密度小于液态水,A项错误。由于水分子之间存在 氢键,使相当量的水分子因氢键而相互缔合,所以接近沸点的 水蒸气的相对分子质量的测定值比用化学式(H2O)计算出来 的相对分子质量大,B项正确。分子间氢键使物质的熔、沸点 较高,而分子内氢键则会使物质的熔、沸点较低,C项错误。 水加热到很高的温度都难以分解,这是由于分子内的H—O共 价键强的缘故,与分子间的氢键无关,D项错误

4.在同一温度下,下列有机化合物在水中的溶解性最好的是 A.乙烷 B.乙醇 C苯 D.四氯化碳 答案:B 解析:乙烷是非极性分子,难溶于水,而且几乎所有的烃都难溶 于水;乙醇是极性分子,与水分子间形成氢键,所以极易溶于水; 苯和四氯化碳均是非极性分子,难溶于水
导航 4.在同一温度下,下列有机化合物在水中的溶解性最好的是 ( )。 A.乙烷 B.乙醇 C.苯 D.四氯化碳 答案:B 解析:乙烷是非极性分子,难溶于水,而且几乎所有的烃都难溶 于水;乙醇是极性分子,与水分子间形成氢键,所以极易溶于水; 苯和四氯化碳均是非极性分子,难溶于水
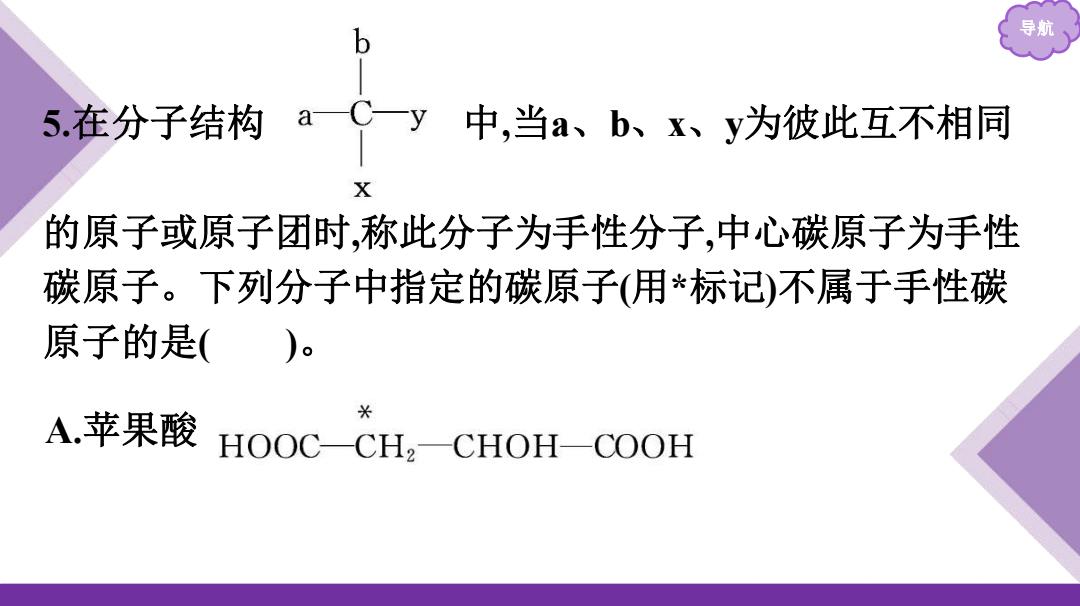
导则 b 5.在分子结构 a Cy 中,当a、b、x、y为彼此互不相同 X 的原子或原子团时,称此分子为手性分子,中心碳原子为手性 碳原子。下列分子中指定的碳原子(用*标记)不属于手性碳 原子的是( A.苹果酸 HOOC CH2—( CHOH-COOH
导航 5.在分子结构 中,当a、b、x、y为彼此互不相同 的原子或原子团时,称此分子为手性分子,中心碳原子为手性 碳原子。下列分子中指定的碳原子(用*标记)不属于手性碳 原子的是( )。 A.苹果酸