
(2)转化率 0.023 0= ×100%=42.6% 0.054
(2)转化率 100% 42.6% 0.054 0.023 = =
三、K与 △G(T)的关系 当体系处于非平衡状态时,此时反应物和生成物 浓度间的关系为: 对气体反应,aA(g)+bB(g) dD(g)+eE (g) Pol(Py (PIP)(P/p) 2p叫分压商,简称反应商。它的形式、写法和K完 全相同,但Q表示式中的各物质分压为任意状态的分压。 而K各物质分压为平衡分压
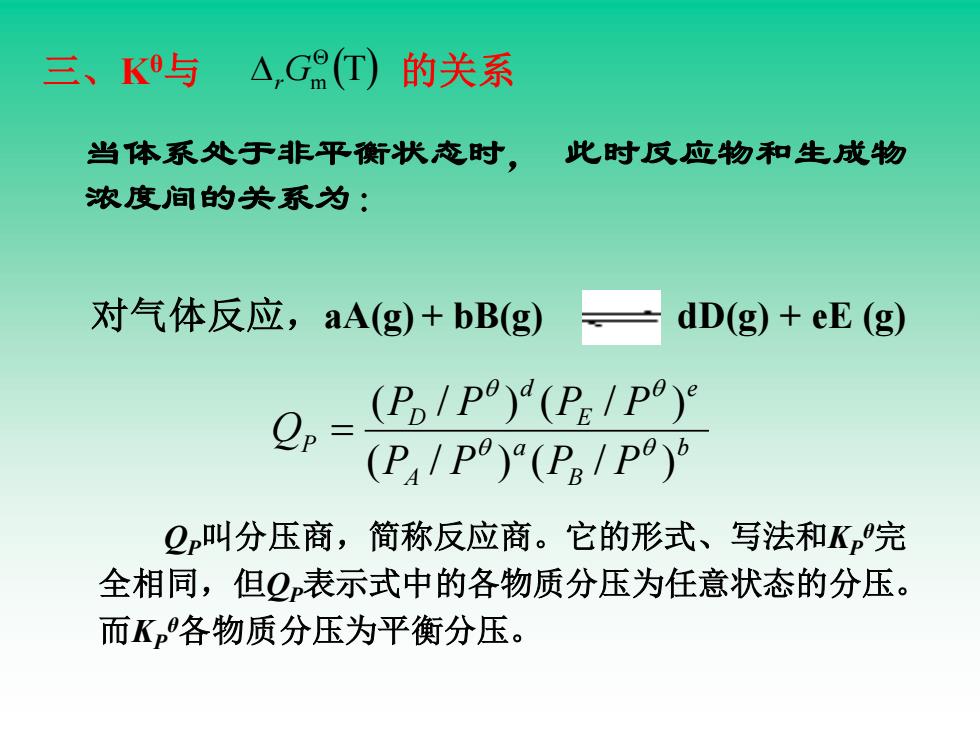
当体系处于非平衡状态时, 此时反应物和生成物 浓度间的关系为: b B a A e E d D P P P P P P P P P Q ( / ) ( / ) ( / ) ( / ) = 对气体反应,aA(g) + bB(g) dD(g) + eE (g) QP叫分压商,简称反应商。它的形式、写法和KP θ完 全相同,但QP表示式中的各物质分压为任意状态的分压。 而KP θ各物质分压为平衡分压。 三、Kθ与 (T) 的关系 Θ r Gm

任意一化学反应的摩尔吉布斯能变△,Gm,都可以用化学 反应的Vant Hoff等温方程式进行计算: △,Gnm=△,G%+2.303RTg2。 (4-1) 反应达到平衡时,△Gm=0,此时反应商2用Kp代替: 0=△,G+2.303 RT Ig Ko gK日- △,G品 (5-5) 2.303RT
任意一化学反应的摩尔吉布斯能变ΔrGm,都可以用化学 反应的Van, t Hoff等温方程式进行计算: p r Gm = r Gm + 2.303RT lg Q (4-1) 反应达到平衡时, ΔrGm = 0,此时反应商 Q 用 KP θ 代替: θ P 0 = r Gm + 2.303RT lg K RT G K θ r m P 2.303 lg = − (5-5)