导航 3.共价键的类型。 (1)6键。 形成由成键原子的s轨道或p轨道“ ”重叠形成 S-s型 H H HH HH ⊙ H一H的s-Sσ键的形成 类 s-p型 -&-8 CI H CI HCI H一CI的s-po键的形成 8-8-88-8 CI CI CI p-p型 C一CI的p-po键的形成
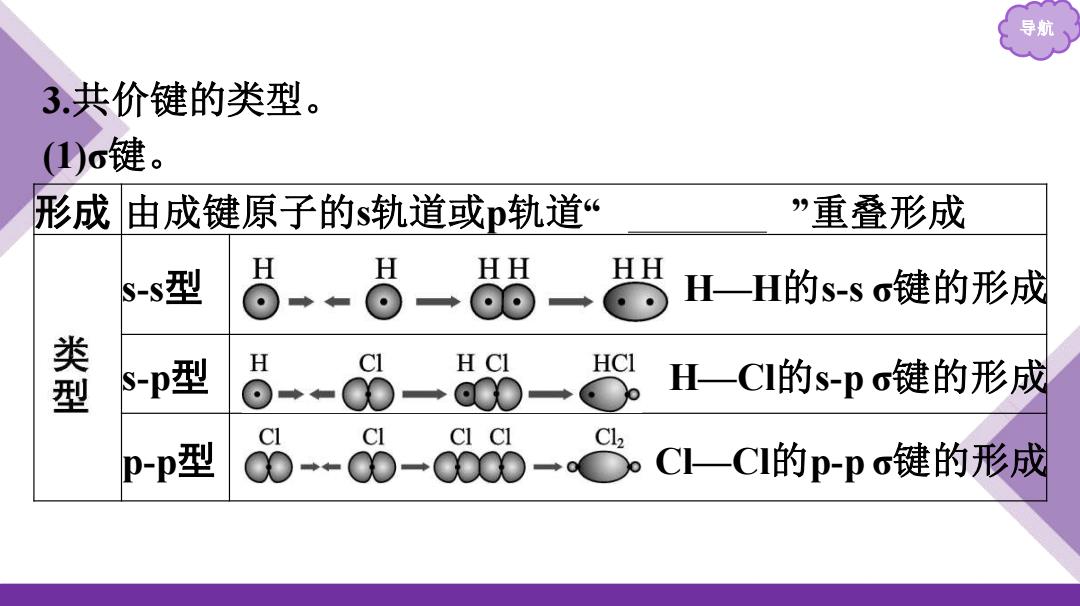
导航 3.共价键的类型。 (1)σ键。 形成 由成键原子的s轨道或p轨道“ 头碰头 ”重叠形成 s-s型 H—H的s-s σ键的形成 s-p型 H—Cl的s-p σ键的形成 p-p型 Cl—Cl的p-p σ键的形成

导航 ①以形成化学键的两原子核的 为轴做旋转操 特征 作,共价键的电子云的图形 ,这种特征称为 ②σ键的强度
导航 特征 ①以形成化学键的两原子核的 连线 为轴做旋转操 作,共价键的电子云的图形 不变 ,这种特征称为 轴对称 ; ②σ键的强度 较大

导航 (2)π键。 形成 由两个原子的p轨道“ ”重叠形成 p-p型 8-8-88-87成 ①π键的电子云具有 对称性,即每个π键的电 特征 子云由两块组成,它们互为 ②π键 旋转;一般不如σ键牢固,较易
导航 (2)π键。 形成 由两个原子的p轨道“ 肩并肩 ”重叠形成 p-p型 p-p π键的形成 特征 ①π键的电子云具有 镜面 对称性,即每个π键的电 子云由两块组成,它们互为 镜像 ; ②π键 不能 旋转;一般不如σ键牢固,较易 断裂

导航 (3)判断σ键、π键的一般规律。 共价单键为 键;共价双键中有一个 键、一个 键共价三键由一个键和两个 键构成
导航 (3)判断σ键、π键的一般规律。 共价单键为 σ 键;共价双键中有一个 σ 键、一个 π 键;共价三键由一个 σ 键和两个 π 键构成

导航 微思考1乙烯和乙炔的化学性质为什么比乙烷活泼呢? 提示:乙烯分子中的碳碳双键和乙炔分子中的碳碳三键中分 别含有1个π键和2个π键,π键的原子轨道重叠程度小,不稳定, 容易断裂。而乙烷分子中没有π键,σ键稳定,不易断裂
导航 微思考1 乙烯和乙炔的化学性质为什么比乙烷活泼呢? 提示:乙烯分子中的碳碳双键和乙炔分子中的碳碳三键中分 别含有1个π键和2个π键,π键的原子轨道重叠程度小,不稳定, 容易断裂。而乙烷分子中没有π键,σ键稳定,不易断裂