导航 3.硝酸与金属反应的计算。 两个 N原子守恒 守恒 得失电子守恒 金属 表现 酸性 M(NO3)x 起酸性作用的HNO3的物 参加 表现 质的量等于生成的硝酸 反应 氧化性 NO、NO2等 关系 盐中NO?的物质的量 HNO3 未参加 全部电离,可以 反应 参加其他反应 利用离子方程式快速找 技巧 出各种量的相互关系
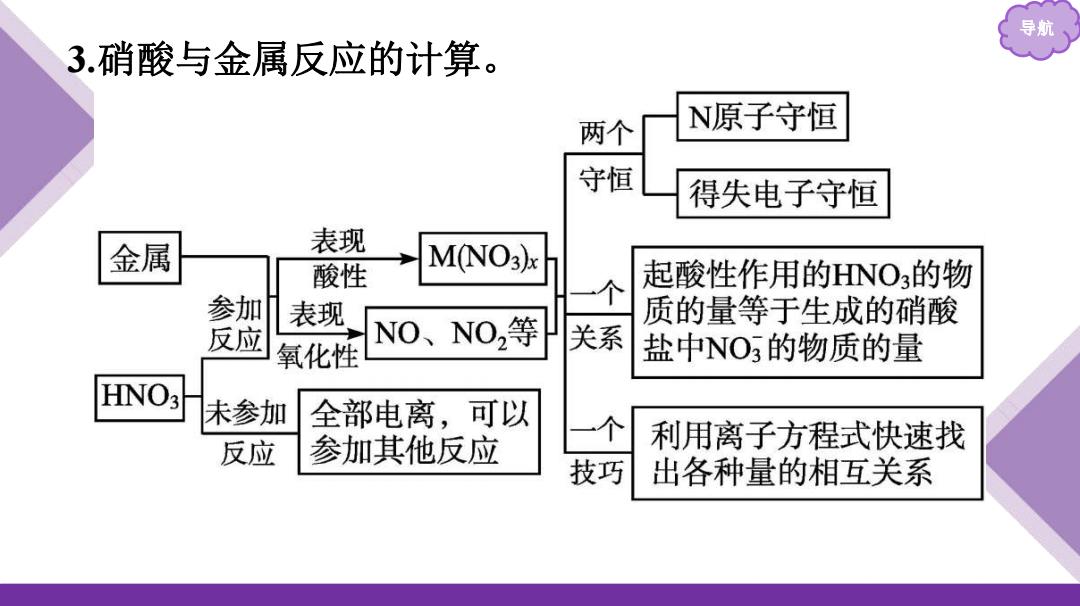
导航 3.硝酸与金属反应的计算

导 ()电子守恒法:硝酸与金属反应属于氧化还原反应,氮原子得到 的电子总数等于金属原子失去的电子总数。 (2)原子守恒法:硝酸与金属反应时,反应前硝酸中的N03一部分 仍以NO,的形式存在,一部分转化为还原产物,这两部分中氮原 子的物质的量之和与反应消耗的硝酸中氮原子的物质的量相等
导航 (1)电子守恒法:硝酸与金属反应属于氧化还原反应,氮原子得到 的电子总数等于金属原子失去的电子总数。 (2)原子守恒法:硝酸与金属反应时,反应前硝酸中的 N𝐎𝟑 - 一部分 仍以 N𝐎𝟑 - 的形式存在,一部分转化为还原产物,这两部分中氮原 子的物质的量之和与反应消耗的硝酸中氮原子的物质的量相等

导航 3)利用离子方程式计算。 硝酸与硫酸的混合液与金属的反应,当金属足量时,不能用硝酸 与金属反应的化学方程式计算,应用离子方程式计算,因为生成 的硝酸盐中的NO,与硫酸电离出的H仍能继续与金属反应。如 金属铜与混合酸反应的离子方程式为 3Cu+8Ht+2N03-3Cu2+2NO↑+4H0
导航 (3)利用离子方程式计算。 硝酸与硫酸的混合液与金属的反应,当金属足量时,不能用硝酸 与金属反应的化学方程式计算,应用离子方程式计算,因为生成 的硝酸盐中的 N𝐎𝟑 - 与硫酸电离出的 H+ 仍能继续与金属反应。如 金属铜与混合酸反应的离子方程式为 3Cu+8H+ +2N𝐎𝟑 - 3Cu2++2NO↑+4H2O

导期 ?思考发现 材料工 《本草纲目拾遗》记载:(硝酸)西洋人所造,性最猛, 能蚀五金。王怡堂先生云:其水至强,五金八石皆能穿滴,惟玻 璃可盛。 材料Ⅱ 某同学在实验室取出一瓶浓硝酸,发现溶液显黄色, 与教材中关于硝酸的描述出现偏差
导航 材料Ⅰ 《本草纲目拾遗》记载:(硝酸)西洋人所造,性最猛, 能蚀五金。王怡堂先生云:其水至强,五金八石皆能穿滴,惟玻 璃可盛。 材料Ⅱ 某同学在实验室取出一瓶浓硝酸,发现溶液显黄色, 与教材中关于硝酸的描述出现偏差