兰州石化职业技术学院石油化学工程系 第四章配位滴定法 二,EDTA与金属高子的配合物 EDTA分子具有两个氨氮原子和四个羧氧原子,都有孤 对电子,即有6个配位原子。因此,绝大多数的全属离子均 能与EDTA形成多个五元环,例如EDTA与Ca+、Fe3+的配合 物的结构如图所示。 12 CH. CH2 CH2 CH, CH2 CH2 C-CH2 O CH2 CH2 o CH, 首页 EDTA与Ca+、Fe3+的配合物的结构示意图 上页下页
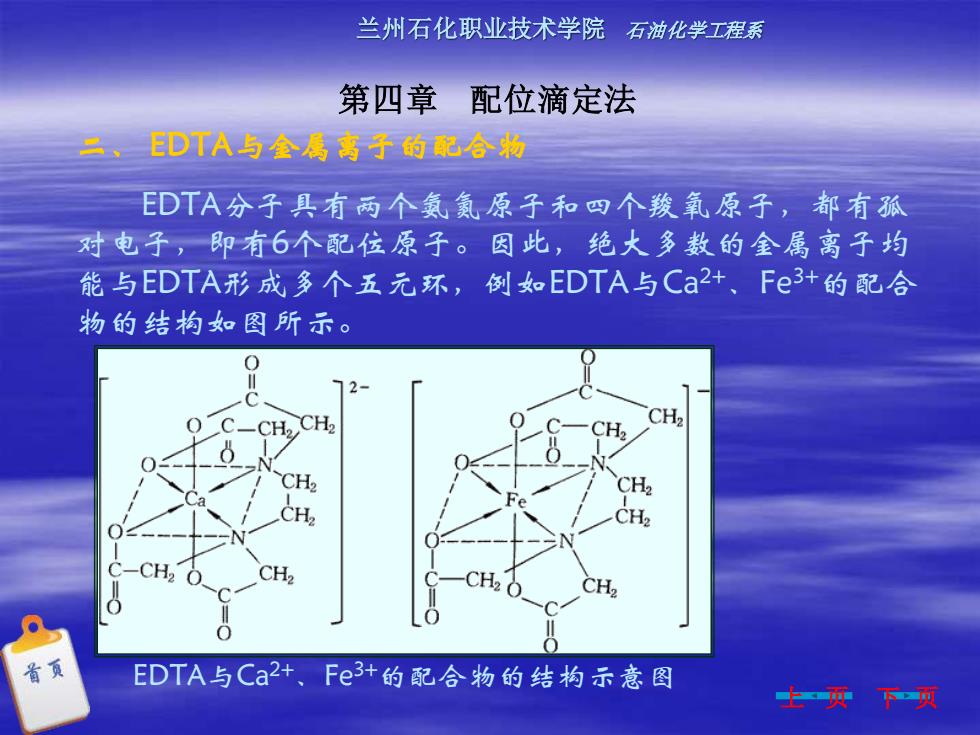
兰州石化职业技术学院 石油化学工程系 第四章 配位滴定法 上 页 下 页 二、 EDTA与金属离子的配合物 EDTA分子具有两个氨氮原子和四个羧氧原子,都有孤 对电子,即有6个配位原子。因此,绝大多数的金属离子均 能与EDTA形成多个五元环,例如EDTA与Ca2+、Fe3+的配合 物的结构如图所示。 EDTA与Ca2+、Fe3+的配合物的结构示意图

兰州石化职业技术学院石油化学工程系 第四章配位滴定法 从图中可以看出,EDTA与金属离子形成五个五元环:四个 门五元环及一个一M 五元环,具有这类环状 O-C-C-N M-C-C-N 结构的螯合物是很稳定的。 由于多数金属离子的配位数不超过6,所以EDTA与大多 数全属离子可形成1:1型的配合物,只有极少数全属离子, 如锆(V)和钼(I)等例外。 首页 上页下一页
兰州石化职业技术学院 石油化学工程系 第四章 配位滴定法 上 页 下 页 从图中可以看出,EDTA与金属离子形成五个五元环:四个 ┌─M─┐五元环及一个┌─M─┐五元环,具有这类环状 结构的螯合物是很稳定的。 由于多数金属离子的配位数不超过6,所以EDTA与大多 数金属离子可形成 1∶1 型的配合物,只有极少数金属离子, 如锆(Ⅳ)和钼(Ⅵ)等例外。 O-C-C-N M-C-C-N

兰州石化职业技术学院石油化学工程系 第四章配位滴定法 无色的金属离子与EDTA配位时,则形成无色的螯合物 有色的全属离子与EDTA配位时,一般则形成颜色更深的螯 合物。例如 NiY2- CuY2- CoY2- MnY2- CrY FeY- 蓝色 深蓝 紫红 紫红 深紫 黄色 综上所述,EDTA与绝大多数全属离子形成的螯合物具 有下列特点: ()计量关系简单,一般不存在逐级配位现象; (2)配合物十分稳定,且水溶性极好,使配位滴定 可以在水溶液中进行。 这些持点使EDTA滴定剂完全待合分析测定的要求,而 被广泛使用。 首页 上页 下页
兰州石化职业技术学院 石油化学工程系 第四章 配位滴定法 上 页 下 页 无色的金属离子与EDTA配位时,则形成无色的螯合物, 有色的金属离子与EDTA配位时,一般则形成颜色更深的螯 合物。例如: 综上所述,EDTA与绝大多数金属离子形成的螯合物具 有下列特点: (1) 计量关系简单,一般不存在逐级配位现象; (2) 配合物十分稳定,且水溶性极好,使配位滴定 可以在水溶液中进行。 这些特点使EDTA滴定剂完全符合分析测定的要求,而 被广泛使用

兰州石化职业技术学院石油化学工程系 第四章配位滴定法 配位解离平衡及影响因素 一、EDTA与金属离子的主反应及配合物的稳定常数 EDTA与金属离子大多形成1:1型的配合物,反应通式 如下: M+Y1-=MY4-8 书写时省略离子的电荷数,简写为 M+Y-MY 此反应为配位滴定的主反应。平衡时配合物的稳定常数为: [MY] [M][Y] 首页 上页下一页
兰州石化职业技术学院 石油化学工程系 第四章 配位滴定法 上 页 下 页 配位解离平衡及影响因素 一、 EDTA与金属离子的主反应及配合物的稳定常数 EDTA与金属离子大多形成1∶1型的配合物,反应通式 如下: 书写时省略离子的电荷数,简写为: 此反应为配位滴定的主反应。平衡时配合物的稳定常数为:
兰州石化职业技术学院石油化学工程系 第四章配位滴定法 EDTA与一些常见金属离子的配合物的稳定常数 (溶液离子强度=0.1molL1,温度20℃) 阳离子 lgKm 阳离子 lgKm 阳离子 1gK型 Nat 1.66 Ce3+ 15.98 Li+ 2.79 A13+ Cu2+ 16.3 18.80 Ba2+ Hg2+ 21.8 7.86 Co2+ 16.31 Sr2+ 23.2 8.73 Cd2+ 16.46 Thd+ Mg2+ Zn2+ Cr3+ 23.4 8.69 16.50 Ca2+ 10.69 Pb2+ 25.1 18.04 Fe3+ n2+ + UN+ 25.80 13.87 18.09 Fe2+ N12+ Bi3+ 27.94 14.32 18.62 首页 上页 下页
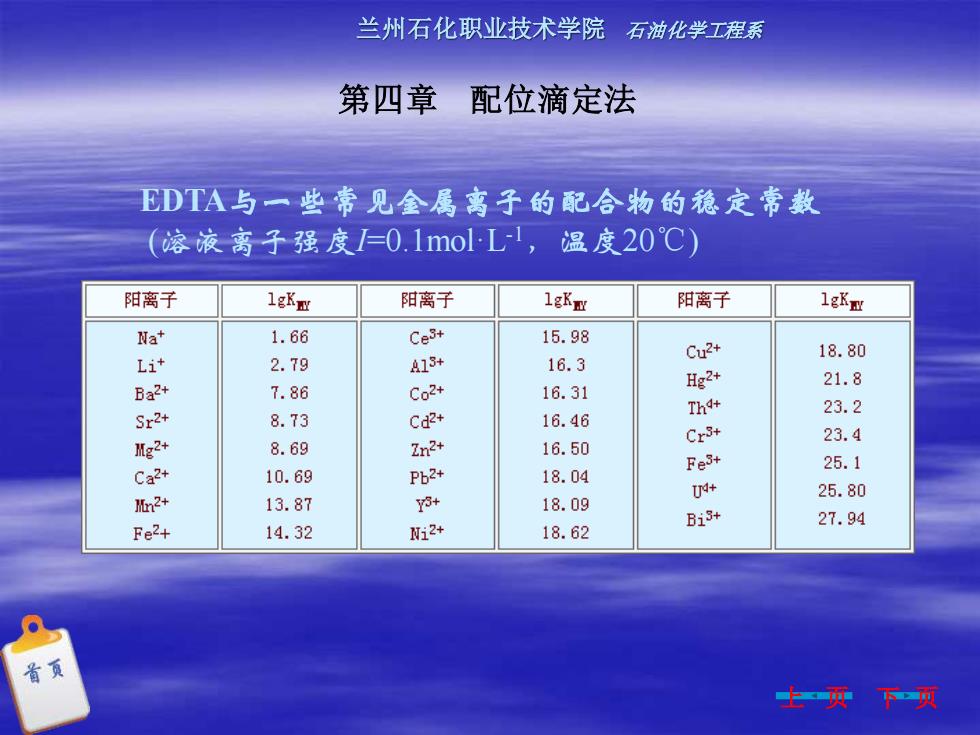
兰州石化职业技术学院 石油化学工程系 第四章 配位滴定法 上 页 下 页 EDTA与一些常见金属离子的配合物的稳定常数 (溶液离子强度I=0.1mol·L-1,温度20℃)