
第七章芳烃 学习要求: 1.掌握芳香烃及其衍生物的命名。 2.理解苯环的结构特征,能用价键理论声明苯的结构。 3.掌握苯及其同系物的化学性质。 4.熟悉苯环上亲电取代反应历程,能熟练应用取代基定位规律。 5.熟悉萘的结构与性质,了解几种多环芳烃。 6.掌握休克尔规则,会判断非苯芳烃。 芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。 芳香二字的来由最初是指从天然树脂(香精油)中提取而得、具有芳香气的 物质。 现代芳烃的概念是指具有芳香性的一类环状化合物,它们不一定具有香味, 也不一定含有苯环结构。 芳香烃具有其特征性质一芳香性(易取代,难加成,难氧化) 芳烃按其结构可分类如下: 「单环芳烃①c4c4ch◇c+C4 CHa 苯乙苯异丙苯苯乙烯 厂苯系芳烃 「联苯☐○O-⊙-O》 联苯 对三联苯 、多环芳烃了 解0Q了 (多苯代脂轻口c吃○ 非养芳经 )同力*晚 ·60
·60· 第七章 芳 烃 学习要求: 1.掌握芳香烃及其衍生物的命名。 2.理解苯环的结构特征,能用价键理论声明苯的结构。 3.掌握苯及其同系物的化学性质。 4.熟悉苯环上亲电取代反应历程,能熟练应用取代基定位规律。 5.熟悉萘的结构与性质,了解几种多环芳烃。 6.掌握休克尔规则,会判断非苯芳烃。 芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。 芳香二字的来由最初是指从天然树脂(香精油)中提取而得、具有芳香气的 物质。 现代芳烃的概念是指具有芳香性的一类环状化合物,它们不一定具有香味, 也不一定含有苯环结构。 芳香烃具有其特征性质——芳香性(易取代,难加成,难氧化)。 芳烃按其结构可分类如下: CH2CH3 CHCH3 CH=CH2 CH3 CH2 苯系芳烃 非苯芳烃 单环芳烃 多环芳烃 联苯 稠环芳烃 多苯代脂烃 苯 乙苯 异丙苯 苯乙烯 联苯 对三联苯 萘 蒽 二苯甲烷 环戊二烯 负离子 环庚三烯 正离子 薁

§7一1苯的结构 一、苯的凯库勒式 1865年凯库勒从苯的分子式CH。出发,根据苯的一元取代物只有一种(说明 六个氢原子是等同的事实,提出了苯的环状构造式。 ,简写为 H “苯的凯库物式结构 二、苯分子结构的价键观点 现代物理方法(射线法、光谱法、偶极距的测定)表明,苯分子是一个平 面正六边形构型,键角都是120°,碳碳键长都是0.1397m。图示如下: 0137m 正六边形结构 所有的原子共平面 C-C键长均为0.1397nm C-H键长均为0.110nm 所有键角都为120 理论解释: 1.杂化轨道理论解释 苯分子中的碳原子都是以s即杂化轨道成键的,故键角均为120°,所有原 子均在同一平面上。 未参与杂化的P轨道都垂直与碳环平面,彼此侧面重叠,形成一个封闭的 共轭体系,由于共轭效应使:电子高度离域,电子云完全平均化,故无单双键 之分。 00 0Q00 00 苯中的P轨道 P轨道的重叠 .61
·61· §7—1 苯的结构 一、 苯的凯库勒式 1865 年凯库勒从苯的分子式 C6H6出发,根据苯的一元取代物只有一种(说明 六个氢原子是等同的事实,提出了苯的环状构造式。 苯的凯库勒式结构 二、苯分子结构的价键观点 现代物理方法(射线法、光谱法、偶极距的测定)表明,苯分子是一个平 面正六边形构型,键角都是 120°,碳碳键长都是 0.1397nm。图示如下: 理论解释: 1.杂化轨道理论解释 苯分子中的碳原子都是以 sp 2杂化轨道成键的,故键角均为 120°,所有原 子均在同一平面上。 未参与杂化的 P 轨道都垂直与碳环平面,彼此侧面重叠,形成一个封闭的 共轭体系,由于共轭效应使π电子高度离域,电子云完全平均化,故无单双键 之分。 简写为 H H H H H H H H H H H H 所有的原子共平面 键长均为 键长均为 所有键角都为 C-C C-H 0.1397nm 0.110nm 120° 120° 120° 0.1397nm 0.1397nm 0.110nm 正六边形结构 苯中的P轨道 P轨道的重叠
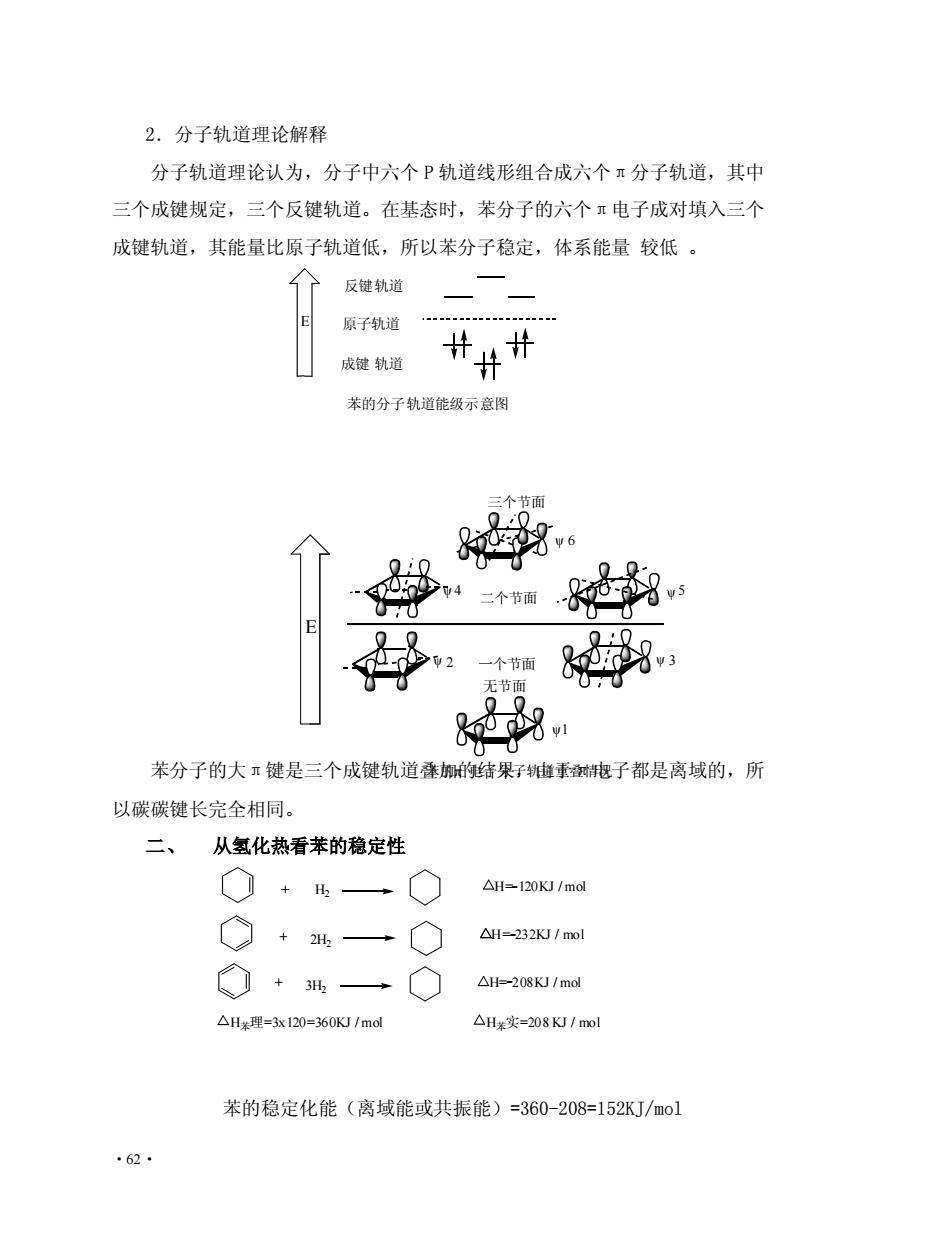
2.分子轨道理论解释 分子轨道理论认为,分子中六个P轨道线形组合成六个π分子轨道,其中 三个成键规定,三个反键轨道。在基态时,苯分子的六个电子成对填入三个 成键轨道,其能量比原子轨道低,所以苯分子稳定,体系能量较低。 反键轨道 原子轨道 成键轨道 苯的分子轨道能级示意图 4二个节面 无节面 和S 苯分子的大π键是三个成键轨道摩期的结果子重我子都是离域的,所 以碳碳键长完全相同。 二、从氢化热看苯的稳定性 O △H120KJ/mol +4一 △H=-232K1ml ○+一○ △H=-208KJ/mdl △H紫理=-3x120=360K)1md △H实=208K/mol 苯的稳定化能(离域能或共振能)=360-208=152KJ/mo1 ·62
·62· 2.分子轨道理论解释 分子轨道理论认为,分子中六个 P 轨道线形组合成六个π分子轨道,其中 三个成键规定,三个反键轨道。在基态时,苯分子的六个π电子成对填入三个 成键轨道,其能量比原子轨道低,所以苯分子稳定,体系能量 较低 。 苯分子的大π键是三个成键轨道叠加的结果,由于π电子都是离域的,所 以碳碳键长完全相同。 二、 从氢化热看苯的稳定性 苯的稳定化能(离域能或共振能)=360-208=152KJ/mol E 原子轨道 反键轨道 成键 轨道 苯的分子轨道能级示意图 H2 2H2 3H2 H= _ 120KJ / mol H= _ 232KJ / mol H= _ 208KJ / mol H苯理=3x120=360KJ / mol H苯实=208 KJ / mol E ψ ψ ψ ψ ψ2 ψ3 4 5 6 1 无节面 三个节面 二个节面 一个节面 苯的π 电子分子轨道重叠情况

三、苯的共振式和共振论的简介 1.基本要点: a.当一个分子、离子或游离基按照理论可以写出两个以上经典结构式时, 这些经典结构式构成了一个共振杂化体,共振杂化体接近实际分子。 ⊙→©→⑦→①→⊙ b.书写极限式时,必须严格遵守经典原子结构理论。原子核的相对位置不 能改变,只允许电子排布上有所差别。 0 → 00 00 00 CH.CH.CH.CH光CH9CH CH3 c.在所有极限式中,未共用的电子数必须相等。 CHCH-CH←一CH-CH丫dGdd4 一个未公用电子 一个未公用电子 三个未公用电子 d.分子的稳定程度可用共振能表示。 苯的共振能为150.4KJ/mol 2.共振论解释苯的结构 最重要的贡献结构 重要的贡献结构 □→□ §7一2单环芳烃的异构和命名 一、异构现象 1.烃基苯有烃基的异构 例如: CHCH地c地 63
·63· 三、 苯的共振式和共振论的简介 1.基本要点: a. 当一个分子、离子或游离基按照理论可以写出两个以上经典结构式时, 这些经典结构式构成了一个共振杂化体,共振杂化体接近实际分子。 b.书写极限式时,必须严格遵守经典原子结构理论。原子核的相对位置不 能改变,只允许电子排布上有所差别。 c.在所有极限式中,未共用的电子数必须相等。 d.分子的稳定程度可用共振能表示。 苯的共振能为 150.4 KJ/mol 2.共振论解释苯的结构 §7—2 单环芳烃的异构和命名 一、 异构现象 1.烃基苯有烃基的异构 例如: CH2CH2CH3 CH CH3 CH3 O C O O O C O O O C O O - - - - - - CH3CH2CH2CH3 CH3CHCH3 CH3 CH2CH=CH2 CH2=CHCH2 CH2CHCH2 一个未公用电子 一个未公用电子 三个未公用电子 + - + - 最重要的贡献结构 最不重要的贡献结构 兰色

2.二烃基苯有三中位置异构 例如: CC 3.三取代苯有三中位置异构 例如: .O 二、命名 1.基的概念 芳烃分子去掉一个氢原子所剩下的基团称为芳基(Ary1)用Ar表示。重要 的芳基有: 苯基,用Ph或中表示 2.一元取代苯的命名 a当苯环上连的是烷基(R-),NO,-X等基团时,则以苯环为母体,叫做 某基苯。 例如: CToroe 异丙基苯叔丁基苯硝基苯 氟苯 b当苯环上连有-C00H,-S0H,-NH,-OH,-CHO,-CH=CH或R较复杂时, 则把苯环作为取代基。例如: ·64
·64· 2.二烃基苯有三中位置异构 例如: 3.三取代苯有三中位置异构 例如: 二、 命名 1.基的概念 芳烃分子去掉一个氢原子所剩下的基团称为芳基(Aryl)用 Ar 表示。重要 的芳基有: 2.一元取代苯的命名 a 当苯环上连的是烷基(R-),-NO2,-X 等基团时,则以苯环为母体,叫做 某基苯。 例如: b 当苯环上连有-COOH,-SO3H,-NH2,-OH,-CHO,-CH=CH2或 R 较复杂时, 则把苯环作为取代基。例如: R R' R R R' R' R R' R R R'' R'' R'' R' R' CH2 (C6H5CH2 -) 苄基(苯甲基),用Bz表示 苯基, 用Ph或ф 表示 CH CH3 CH3 NO2 Cl 异丙基苯 叔丁基苯 硝基苯 氯苯