
第4章配合物反应机理和动力学 配体取代(交换反应) 两类 电子转移反应(氧化还原反应)Taube,Marcus 反应机理的研究 >研究对象:Co3+,Cr3+,N2+Pt2+等中心离子,简单配体 >研究的时标(time scale)范围: 100s(惰性化合物) 配体交换 ms(活性化合物) μs(电荷迁移和电子转移)
第4章 配合物反应机理和动力学 反应 机理的研究 ➢ 研究对象: Co3+ , Cr3+ , Ni2+ ,Pt2+等中心离子, 简单配体 ➢ 研究的时标(time scale )范围: 100s (惰性化合物) ms (活性化合物) s (电荷迁移和电子转移) 配体取代 (交换反应) 电子转移反应(氧化还原反应)Taube , Marcus 两类 配体交换

一.配位取代(substitution)反应 反应机理: 计量关系,速率方程 深层次的机理研究,影响反应速率的因素 中心离子的电子结构LFSE,HS,LS),价态,半径 离去基团(leaving group))(和M的作用) 进入基团(entering group)(有影响或者无影响)》 旁位基团(spectator ligands)(例如,对位效应) 空间效应(steric effects)
一.配位取代(substitution)反应 反应机理: ➢ 计量关系, 速率方程 ➢ 深层次的机理研究,影响反应速率的因素 中心离子 的电子结构(LFSE, HS, LS), 价态, 半径 离去基团(leaving group) ( 和M的作用) 进入基团(entering group) (有影响或者无影响) 旁位基团(spectator ligands) (例如, 对位效应) 空间效应(steric effects)
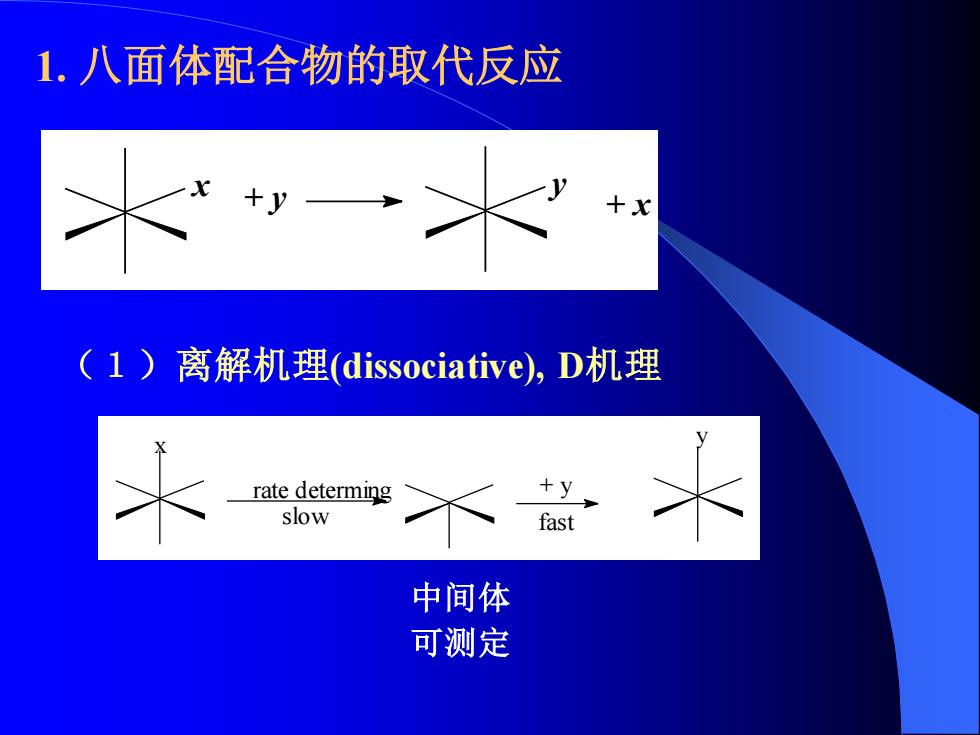
1.八面体配合物的取代反应 (1)离解机理(dissociative),D机理 rate determing +y slow fast 中间体 可测定
1. 八面体配合物的取代反应 + y y + x x (1)离解机理(dissociative), D机理 x rate determing slow + y y fast 中间体 可测定
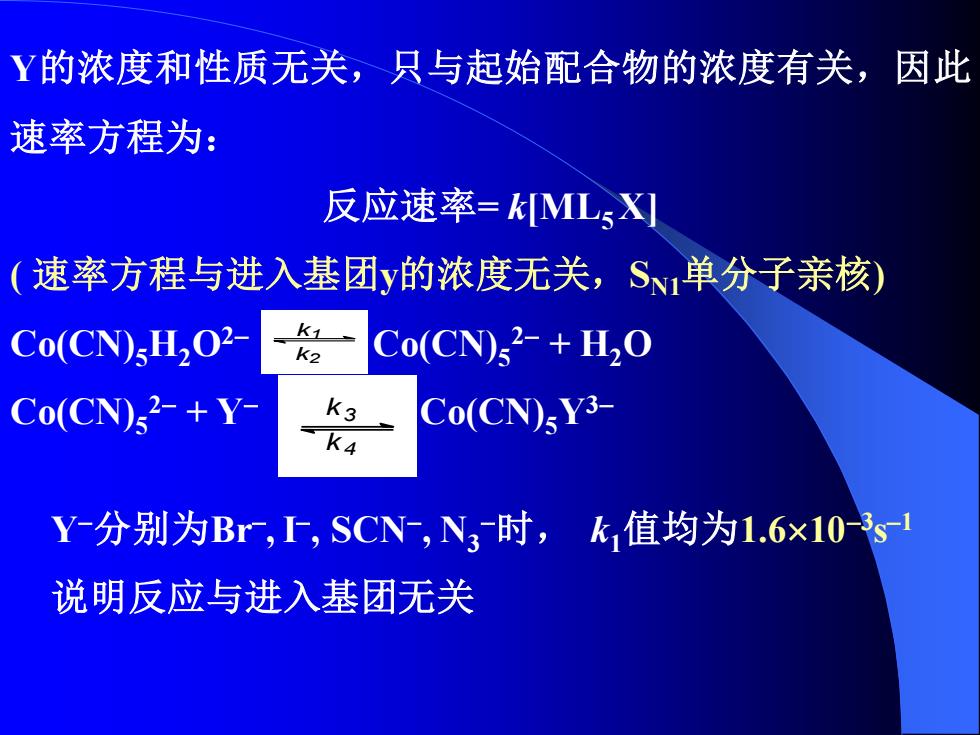
Y的浓度和性质无关,只与起始配合物的浓度有关,因此 速率方程为: 反应速率=kML5X] (速率方程与进入基团y的浓度无关,S、单分子亲核) Co(CN)sH2O2- 1 K2 Co(CN)2-+H2O Co(CN)2-+Y- K3 ≤K4 Co(CN)sY3- Y-分别为Br,SCN,N3时,k值均为1.6×103s 说明反应与进入基团无关
Y的浓度和性质无关,只与起始配合物的浓度有关,因此 速率方程为: 反应速率= k[ML5 X] ( 速率方程与进入基团y的浓度无关,SN1单分子亲核) Co(CN)5H2O2− Co(CN)5 2− + H2O Co(CN)5 2− + Y− Co(CN)5Y3− k1 k2 k3 k4 Y−分别为Br− , I− , SCN− , N3 −时, k1值均为1.610−3 s −1 说明反应与进入基团无关
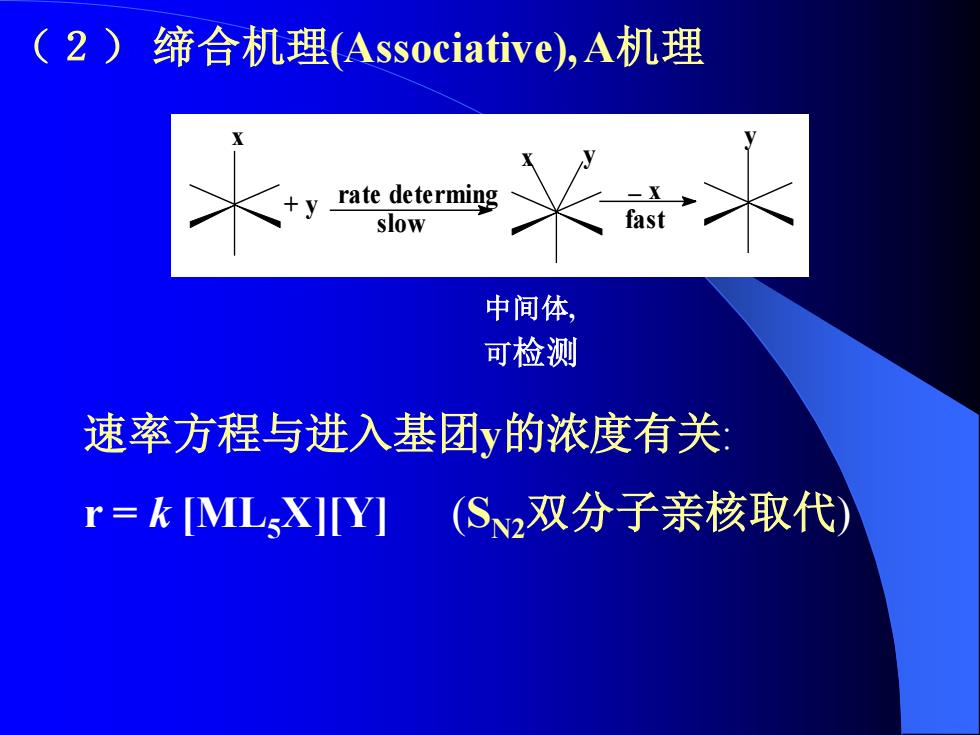
(2)缔合机理Associative),A机理 y rate determing slow 中间体, 可检测 速率方程与进入基团y的浓度有关: r=kMLX]Y](S2双分子亲核取代)
(2) 缔合机理(Associative), A机理 中间体, 可检测 x rate determing slow + y y fast x y _ x 速率方程与进入基团y的浓度有关: r = k [ML5X][Y] (SN2双分子亲核取代)