
绝不允许在实验室加热。夏天,打开浓氨水瓶盖之前,应先将氨水 瓶放在自来水流水下冷却后,再行开启。如不小心将酸或碱溅到 皮肤或眼内,应立即用水冲洗,然后用50g·L1碳酸氢钠溶液(酸 腐蚀时采用减50g·L1硼酸溶液(碱腐蚀时采用)冲洗,最后用 水冲洗。 (5)使用CCL4、乙醚、苯、丙酮、三氯甲烷等有机溶剂时,一定 要远离火焰和热源。使用完后将试剂瓶塞严,放在阴凉处保存。 低沸点的有机溶剂不能直接在火焰上或热源(煤气灯或电炉)上加 热,而应在水浴上加热。 (6)热、浓的HCO4遇有机物常易发生爆炸。如果试样为有 机物,应先用浓硝酸加热,使之与有机物发生反应,有机物被破坏 后,再加入HCO4。蒸发HCIO4所产生的烟雾易在通风橱中凝 聚,如经常使用HCO4的通风橱应定期用水冲洗,以免HCO4的 凝聚物与尘埃、有机物作用,引起燃烧或爆炸,造成事故。 (7)汞盐、砷化物、氰化物等剧毒物品,使用时应特别小心。 氰化物不能接触酸,因作用时产生剧毒的HCN!氰化物废液应倒 入碱性亚铁盐溶液中,使其转化为亚铁氰化铁盐,然后作废液处 理,严禁直接倒入下水道或废液缸中。 硫化氢气体有毒,涉及到有关疏化氢气体的操作时,一定要在 通风橱中进行。 (8)如发生烫伤,可在烫伤处抹上黄色的苦味酸溶液或烫伤 软膏。严重者应立即送医院治疗。实验室如发生火灾,应根据起 火的原因进行针对性灭火。酒清及其它可溶于水的液体着火时, 可用水灭火:汽油、乙醚等有机溶剂着火时,用砂土扑灭,此时绝对 不能用水,否则反而扩大燃烧面:导线或电器着火时,不能用水及 CO2灭火器,而应首先切断电源,用CCL4灭火器灭火,并根据火情 决定是否要向消防部门报告。 (9)实验室应保持室内整齐、干净。不能将毛刷、抹布扔在水 槽中:禁止将固体物、玻璃碎片等扔入水槽内,以免造成下水道堵
所产生的烟雾易在通风橱中凝 皮肤或眼内,应立即用水冲洗,然后用 腐蚀时采用)或 水冲洗。 使用 、乙醚、苯、丙酮、三氯甲烷等 有机溶剂时,一定 要远离火焰和热源。使用完后将试剂瓶塞严,放在阴凉处保存。 低沸点的有机溶剂不能直接在火焰上或热源(煤气灯或电炉)上加 热,而应在水浴上加热。 热、浓 的 遇有机物常易发生爆炸。如果试样为有 后,再加入 机物,应先用浓硝酸加热,使之与有机物发生反应,有机物被破坏 蒸发 聚,如经常使用 的通风橱应定期用水冲洗,以免 的 凝聚物与尘埃、有机物作用,引起燃烧或爆炸,造成事故。 氰化物废液应倒 )汞盐、砷化物、氰化物等剧毒物品,使用时应特别小心。 氰化物不能接触酸,因作用时产生剧毒的 入碱性亚铁盐溶液中,使其转化为亚铁氰化铁盐,然后作废液处 理,严禁直接倒入下水道或废液缸中。 硫化氢气体有毒,涉及到有关硫化氢气体的操作时,一定要在 通风橱中进行。 如发生烫伤,可在烫伤处抹上黄色的苦味酸溶液或烫伤 软膏。严重者应立即送医院治疗。实验室如发生火灾,应根据起 火的原因进行针对性灭火。酒清及其它可溶于水的液体着火时, 可用水灭火;汽油、乙醚等有机溶剂着火时,用砂土扑灭,此时绝对 不能用水,否则反而扩大燃烧面;导线或电器着火时,不能用水及 灭火器,而应首先切断电源,用 灭火器灭火,并根据火情 决定是否要向消防部门报告。 实验室应保持室内整齐、干净。不能将毛刷、抹布扔在水 槽中;禁止将固体物、玻璃碎片等扔入水槽内,以免造成下水道堵 绝不允许在实验室加热。夏天,打开浓氨水瓶盖之前,应先将氨水 瓶放在自来水流水下冷却后,再行开启。如不小心将酸或碱溅到 碳酸氢钠溶液(酸 硼酸溶液(碱腐蚀时采用)冲洗,最后用

塞。此类物质以及废纸、废屑应放入废纸箱或实验室规定存放的 地方。废酸、废碱应小心倒入废液缸,切勿倒入水槽内,以免腐蚀 下水管
塞。此类物质以及废纸、废屑应放入废纸箱或实验室规定存放的 地方。废酸、废碱应小心倒入废液缸,切勿倒入水槽内,以免腐蚀 下水管

第二章 常见离子的定性分析实验 §2-1定性分析基础知识 一、定性分析的任务及方法 定性分析的任务是鉴定物质中所含有的组分。对于无机定性 分析来说,这些组分通常表示为元素或离子,而在有机分析中所鉴 定的通常是元素、官能团或化合物。本章只讨论常见的无机离子 的定性分析。 无机定性分析实验的学习目的是使学生在掌握元素周期律的 基础上进一步熟悉常见离子的共性和个性,以便为选择和设计离 子的定性和定量分析方法提供依据。定性分析是理论与实际结合 很紧密的内容,通过学习可以进一步获得运用理论知识(特别是对 于平衡理论)解决实际问题的能力。定性分析的操作技术可以培 养学生细致认真的态度,提高实验操作的技能、技巧。因此对于定 性分析的学习不仅具有理论和实际应用价值,同时作为分析实验 课的一部分又有很大的教育意义。 无机物的定性分析主要有化学分析法和发射光谱法。化学分 析法由于设备简单、经济,方法灵活性大等优越性,仍为常用的方 法。化学分析法所依据的是物质的化学反应。如果化学反应是在 溶液中进行的,这种方法为湿法:如果反应是在固体之间进行的, 这种方法称为干法。焰色反应、熔珠试验、粉末研磨法等属于干法
常见离子的定性分析实验 定性分析基础知识 第二章 一、定性分析的任务及方法 定性分析的任务是鉴定物质中所含有的组分。对于无机定性 分析来说,这些组分通常表示为元素或离子,而在有机分析中所鉴 定的通常是元素、官能团或化合物。本章只讨论常见的无机离子 的定性分析。 无机定性分析实验的学习目的是使学生在掌握元素周期律的 基础上进一步熟悉常见离子的共性和个性,以便为选择和设计离 子的定性和定量分析方法提供依据。定性分析是理论与实际结合 很紧密的内容,通过学习可以进一步获得运用理论知识(特别是对 于平衡理论)解决实际问题的能力。定性分析的操作技术可以培 养学生细致认真的态度,提高实验操作的技能、技巧。因此对于定 性分析的学习不仅具有理论和实际应用价值,同时作为分析实验 课的一部分又有很大的教育意义。 无机物的定性分析主要有化学分析法和发射光谱法。化学分 析法由于设备简单、经济,方法灵活性大等优越性,仍为常用的方 法。化学分析法所依据的是物质的化学反应。如果化学反应是在 溶液中进行的,这种方法为湿法;如果反应是在固体之间进行的, 这种方法称为干法。焰色反应、熔珠试验、粉末研磨法等属于干法

分析。 根据分析时试样的用量、操作技术、被检出组分量的不同,可 以分为常量分析、微量分析和半微量分析。常量分析所用的试样 量为0.5~1g或20~30mL溶液,所用的仪器和操作与普通的化 学实验相同,如普通的试管、烧杯、漏斗等,使用过滤的方法分离沉 淀与溶液。这种方法操作比较简便、易于掌握,但是费时,药品消 耗量大。微量分析所用的试样量为常量分析的百分之一,即固体 数毫克,溶液数滴。使用的仪器为小巧而特殊的仪器。半微量分 析是介于上述二者之间,试样量为常量法的110~120,即固体 试样几十毫克,液体试样1一3mL,沉淀与溶液的分离使用离心 机。离子的检出以点滴反应为主。这种方法基本上保留了常量法 的优点,又有灵敏、快速、节约试剂等优点。本书在具体定性分析 实验中采用半微量定性分析法。 二、鉴定反应的灵敏度 鉴定反应的灵敏度通常用“检出限量”和“最低浓度”表示。 检出限量是指在一定条件下,利用某反应能检出离子的最小 质量,单位用g表示,符号以m表示。 最低浓度是指在一定条件下,被检出离子能得到肯定结果的 最低浓度。单位用gmL1表示。符号以PB表示。 例如用K2CO4鉴定Pb2+,当稀释至200000mL溶液中含有 1g(10g)Pb2+时,取一滴溶液相当于0.05mL)加入K2C04试 剂还能观察到黄色的PbCO,沉淀析出,那么可以根据所取试液 的体积与检出限量、最低浓度的关系表示鉴定反应的灵敏度。 最低浓度由下式得到: Aw器-5enL 因为稀释液一般以1mL相当于1g计,取一滴(相当于0.05mL) 则
沉淀析出,那么可以根据所取试液 表示。 表示。 ,当稀释至 分 析。 根据分析时试样的用量、操作技术、被检出组分量的不同,可 以分为常量分析、微量分析和半微量分析。常量分析所用的试样 量为 或 溶液,所用的仪器和操作与普通的化 学实验相同,如普通的试管、烧杯、漏斗等,使用过滤的方法分离沉 淀与溶液。这种方法操作比较简便、易于掌握,但是费时,药品消 耗量大。微量分析所用的试样量为常量分析的百分之一,即固体 数毫克,溶液数滴。使用的仪器为小巧而特殊的仪器。半微量分 析是介于上述二者之间,试样量为常量法的 试样几十毫克,液体试样 ,即固体 ,沉淀与溶液的分离使用离心 机。离子的检出以点滴反应为主。这种方法基本上保留了常量法 的优点,又有灵敏、快速、节约试剂等优点。本书在具体定性分析 实验中采用半微量定性分析法。 二、鉴定反应的灵敏度 鉴定反应的灵敏度通常用“检出限量”和“最低浓度”表示。 表示,符号以 检出限量是指在一定条件下,利用某反应能检出离子的最小 质量,单位用 表示。符号以 最低浓度是指在一定条件下,被检出离子能得到肯定结果的 最低浓度。单位用 例如用 鉴定 溶液中含有 时,取一滴溶液(相当于 加入 试 剂还能观察到黄色的 的体积与检出限量、最低浓度的关系表示鉴定反应的灵敏度。 最低浓度由下式得到: 因为稀释液一般以 相当于 计,取一滴(相当于 则
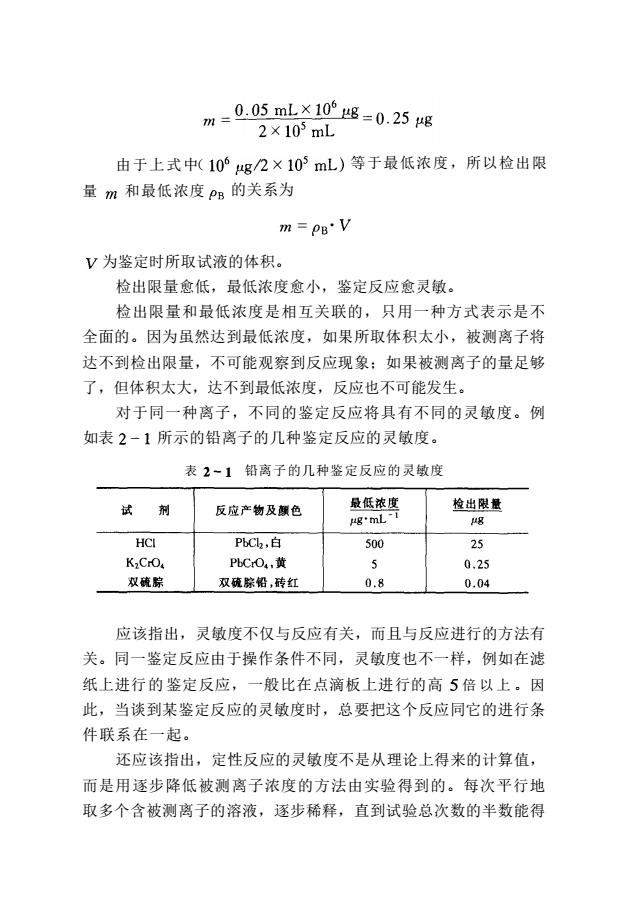
m-0-05mX10心2g=0.25g 2×103mL 由于上式中(10°g2×103mL)等于最低浓度,所以检出限 量m和最低浓度PB的关系为 m=PBV V为鉴定时所取试液的体积。 检出限量愈低,最低浓度愈小,鉴定反应愈灵敏。 检出限量和最低浓度是相互关联的,只用一种方式表示是不 全面的。因为虽然达到最低浓度,如果所取体积太小,被测离子将 达不到检出限量,不可能观察到反应现象:如果被测离子的量足够 了,但体积太大,达不到最低浓度,反应也不可能发生。 对于同一种离子,不同的鉴定反应将具有不同的灵敏度。例 如表2-1所示的铅离子的几种鉴定反应的灵敏度。 表2-1铅离子的几种鉴定反应的灵敏度 反应产物及颜色 最低浓度 检出限量 ug'mL g HCI PbCl,白 500 25 PbCrO,黄 0.25 双硫腙 双硫除铅,砖红 0.8 0.04 应该指出,灵敏度不仅与反应有关,而且与反应进行的方法有 关。同一鉴定反应由于操作条件不同,灵敏度也不一样,例如在滤 纸上进行的鉴定反应,一般比在点滴板上进行的高5倍以上。因 此,当谈到某鉴定反应的灵敏度时,总要把这个反应同它的进行条 件联系在一起。 还应该指出,定性反应的灵敏度不是从理论上得来的计算值, 而是用逐步降低被测离子浓度的方法由实验得到的。每次平行地 取多个含被测离子的溶液,逐步稀释,直到试验总次数的半数能得
如表 表 铅离子的几种鉴定反应的灵敏度 倍 以 上 。因 等于最低浓度,所以检出限 量 的关系为 由于上式中( 和最低浓度 为鉴定时所取试液的体积。 检出限量愈低,最低浓度愈小,鉴定反应愈灵敏。 检出限量和最低浓度是相互关联的,只用一种方式表示是不 全面的。因为虽然达到最低浓度,如果所取体积太小,被测离子将 达不到检出限量,不可能观察到反应现象;如果被测离子的量足够 了,但体积太大,达不到最低浓度,反应也不可能发生。 对于同一种离子,不同的鉴定反应将具有不同的灵敏度。例 所示的铅离子的几种鉴定反应的灵敏度。 的 鉴定反应,一般比在点滴板上进行的高 应该指出,灵敏度不仅与反应有关,而且与反应进行的方法有 关。同一鉴定反应由于操作条件不同,灵敏度也不一样,例如在滤 纸上进行 此,当谈到某鉴定反应的灵敏度时,总要把这个反应同它的进行条 件联系在一起。 还应该指出,定性反应的灵敏度不是从理论上得来的计算值, 而是用逐步降低被测离子浓度的方法由实验得到的。每次平行地 取多个含被测离子的溶液,逐步稀释,直到试验总次数的半数能得