3.1烯烃和炔烃的结构 3.1.1烯烃碳碳双键的组成 基态 激发态 sp2杂化态 2p1 2p 电子 2pL↑1 跃迁 杂化 2s → spL11 2s 1s1 ! 1s 1s赳 图3.1sp2杂化轨道形成过程示意图
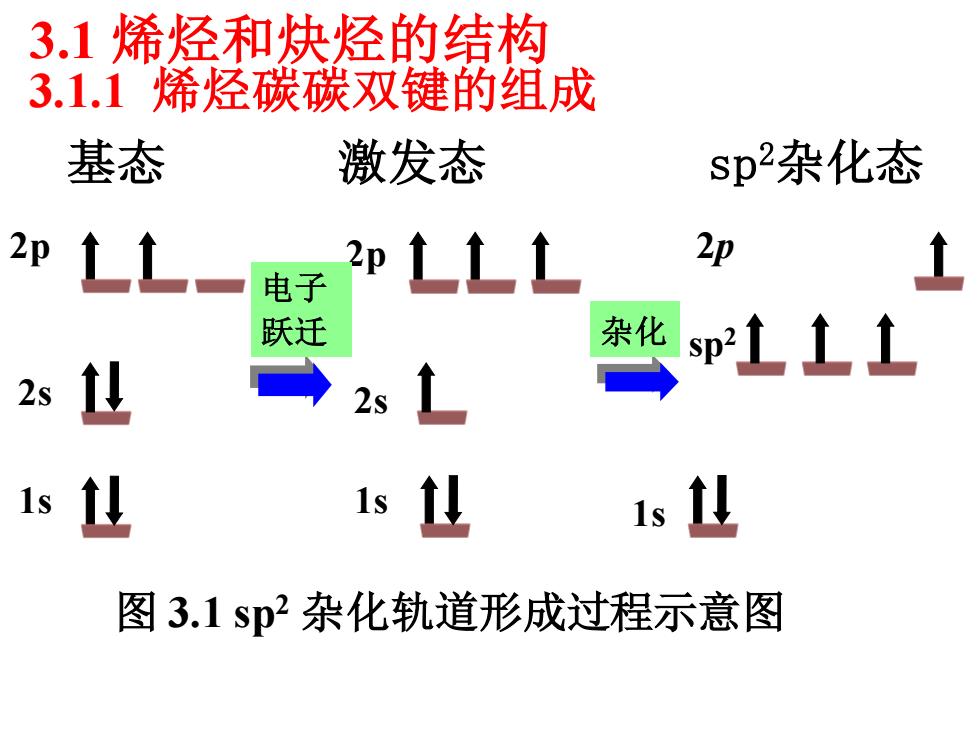
3.1 烯烃和炔烃的结构 3.1.1 烯烃碳碳双键的组成 2p 2s 1s 基态 激发态 sp2杂化态 1s 2p 2s 2p 1s sp2 电子 跃迁 杂化 图 3.1 sp2 杂化轨道形成过程示意图
每个sp2杂化轨道 含1/3s轨道成分, 含23p轨道成分。 图3.2一个sp2杂化轨道 三个sp杂化轨道在同 一平面上,成平面三角 形几何图形,其轨道间 对称轴的夹角为120°
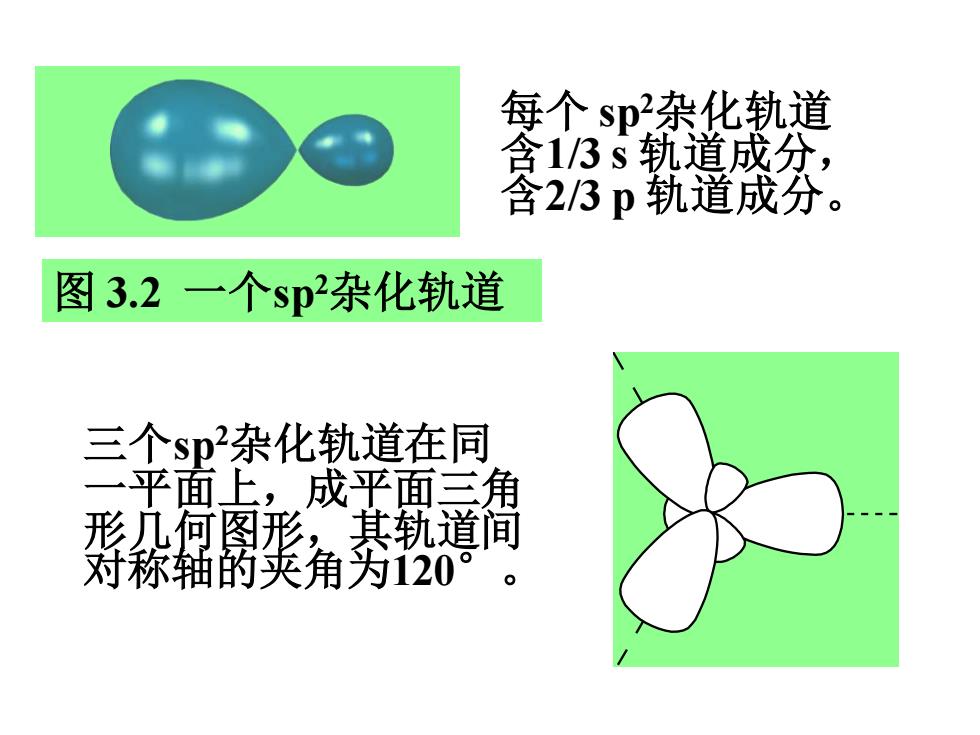
每个 sp2杂化轨道 含1/3 s 轨道成分, 含2/3 p 轨道成分。 图 3.2 一个sp2杂化轨道 三个sp2杂化轨道在同 一平面上,成平面三角 形几何图形,其轨道间 对称轴的夹角为120°

在乙烯分子中,每个碳原子都是s?杂化。 C一Cσ键的形成: sp2-sp2交盖 C一Ho键的形成: sp2-1s交盖 一个C-Co键和4个C一Ho键共处同一平面。 构成分子中2个碳4个氢共在一个平面,成平面形 分子。 H C-CH H 0.134nm H 189 H 图34乙烯的结构
在乙烯分子中,每个碳原子都是 sp2 杂化。 C-Hσ键的形成: sp2–sp C-Cσ键的形成: 2 交盖 sp2 -1s 交盖 一个C-Cσ键和4个C-Hσ键共处同一平面。 构成分子中2个碳4个氢共在一个平面 ,成平面形 分子。 图3.4 乙烯的结构 C C H H H H 0. 134 nm C H H H H 121 118 。 H 。 H H H C C
C一Cπ键的形成:垂直于sp2杂化轨道 所在平面且相互平行的2个p轨道进行侧面 交盖构成键。 在π键中,电子云分布在两个C原子 所处平面的上方和下方。 H H H H 图3.5乙烯分子中的键
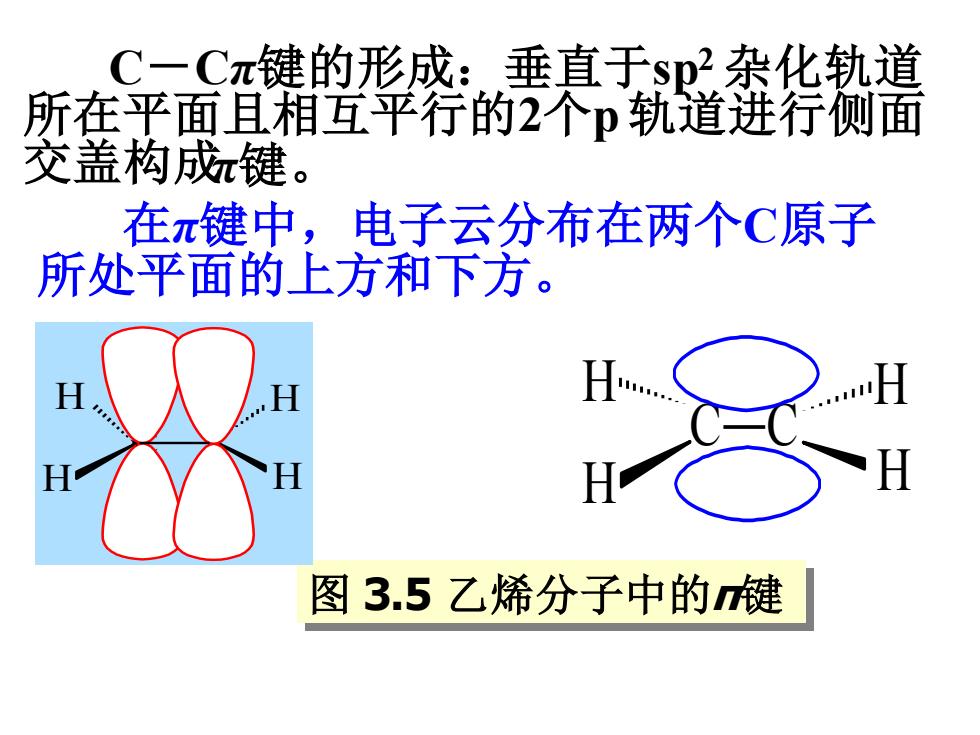
C-Cπ键的形成:垂直于sp2 杂化轨道 所在平面且相互平行的2个p 轨道进行侧面 交盖构成π键。 在π键中,电子云分布在两个C原子 所处平面的上方和下方。 图 3.5 乙烯分子中的π键 C C H H H H C H H H H

构成π键的P轨道上的电子裸露于分子平面, 碳原子对P轨道上的电子束缚力少,因此π键上 的电子有较大流动性,可极化性大,受外界试 剂影响容易极化,所以烯烃有较大的化学活性
构成π键的P轨道上的电子裸露于分子平面, 碳原子对P轨道上的电子束缚力少,因此π键上 的电子有较大流动性,可极化性大,受外界试 剂影响容易极化,所以烯烃有较大的化学活性