
第二节炔烃的化学性质 1、 炔烃的酸性 连在电 负性较 2、炔烃的亲电加成 强的原 子上的 3、硼氢化反应 氢 4、氧化 CC-H 5、炔烃的加氢和还原 10 碳碳π键(电子云 密度大,易发生亲 核较为暴露的 电反应》 sp杂化的碳
1、 炔烃的酸性 2、 炔烃的亲电加成 3、 硼氢化反应 4、 氧化 5、 炔烃的加氢和还原 第二节 炔烃的化学性质 C C H 碳碳π键(电子云 密度大,易发生亲 电反应) 核较为暴露的 sp杂化的碳 连在电 负性较 强的原 子上的 氢
第二节炔烃的化学性质 7.2.1炔烃的酸性 7.2.1.1 酸性 RC-H R3C-+H 碳氢键的断裂也可以看作是一种酸性电离, 所以将烃称为含碳酸 含碳酸的酸性强弱可用pka判别,pka越小,酸性越强。 烷烃(乙烷)〈烯烃(乙烯)≈氨〈末端炔烃(乙炔)〈乙醇〈水 pka 50 ~40 35 25 16 15.7 酸性逐渐增强 其共轭碱的碱性逐渐减弱
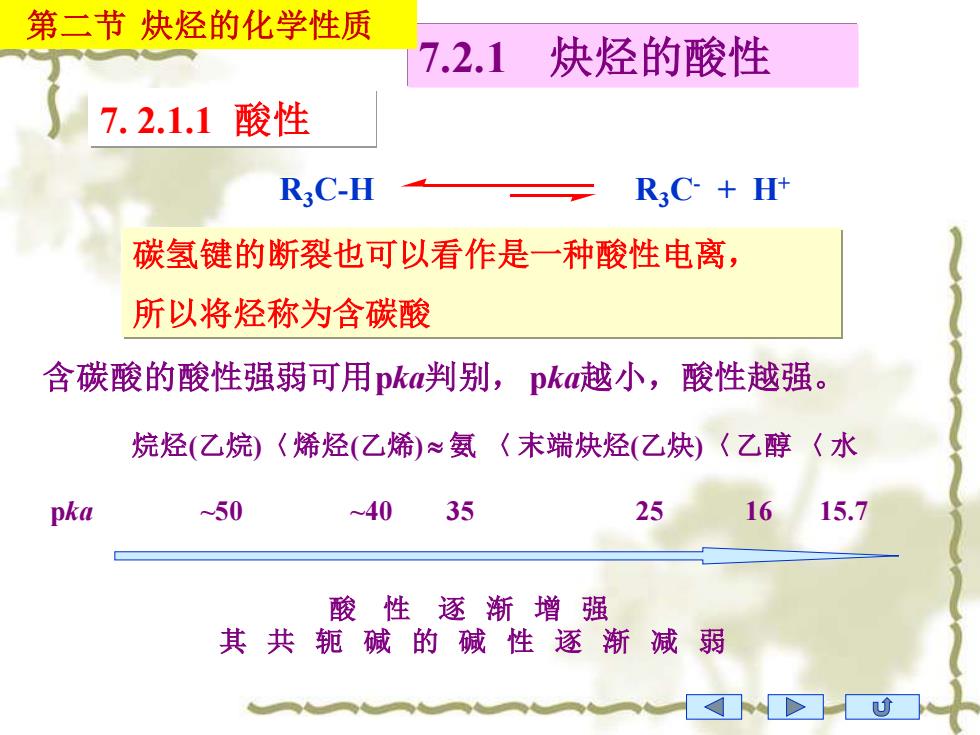
7.2.1 炔烃的酸性 R3C-H R3C- + H+ 碳氢键的断裂也可以看作是一种酸性电离, 所以将烃称为含碳酸 含碳酸的酸性强弱可用pka判别,pka越小,酸性越强。 烷烃(乙烷)〈烯烃(乙烯) 氨 〈 末端炔烃(乙炔)〈乙醇 〈 水 pka ~50 ~40 35 25 16 15.7 酸 性 逐 渐 增 强 其 共 轭 碱 的 碱 性 逐 渐 减 弱 7. 2.1.1 酸性 第二节 炔烃的化学性质
第二节炔烃的化学性质 7.2.1 炔烃的酸性 7.2.1.1 酸性 碳氢化合物中H的酸性顺序: C-H> sp ※ 三C—H炔氢的酸性 HC≡CH+NH →HC三C:+NH3(pK-25) HC三CH+Na HC≡CNa+Hh 生成的炔钠是一个亲核试剂 RC=CNa+RX RC≡CR' 用于制备高级炔烃
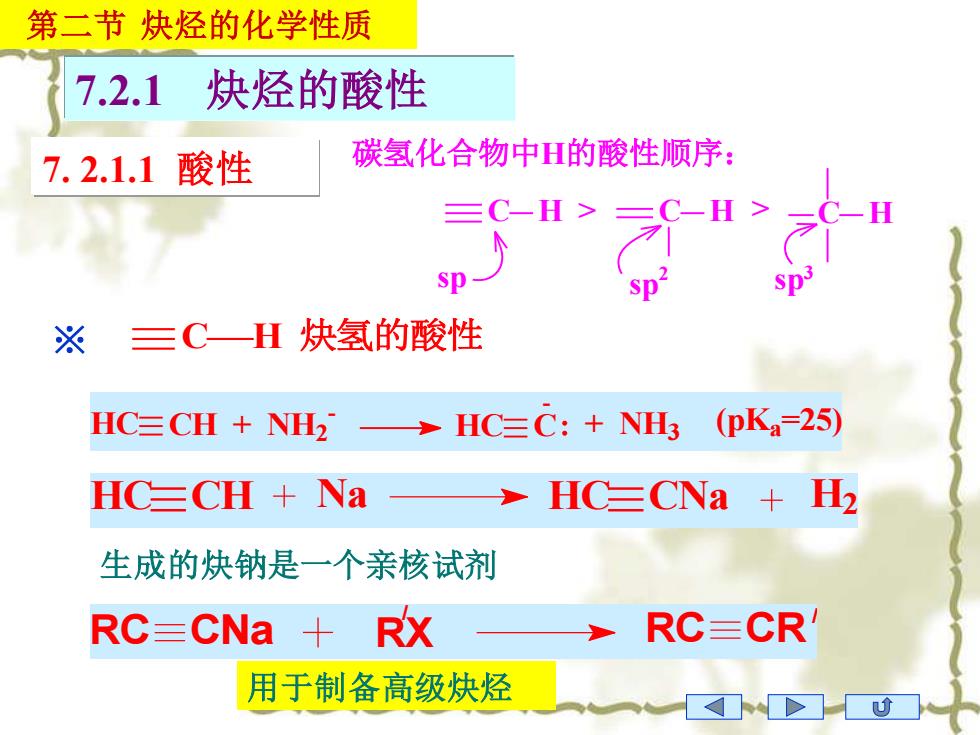
7.2.1 炔烃的酸性 第二节 炔烃的化学性质 HC CH + NH2 - HC C - + NH3 (pKa =25) 碳氢化合物中H的酸性顺序: C H > C H > C H sp sp 2 sp 3 HC CH Na HC CNa H2 生成的炔钠是一个亲核试剂 RC CNa RX / RC CR / 用于制备高级炔烃 ※ C H 炔氢的酸性 7. 2.1.1 酸性
第二节炔烃的化学性质 7.2.1炔烃的酸性 7.2.1.2炔化物的生成 RC=CH NaNH2 液氨 RC=CNa RC=CH+n-C4HoLi-RC=CLi n-C4H10 RC=CH C2H5MgBr-RC=CMgBr C2H6
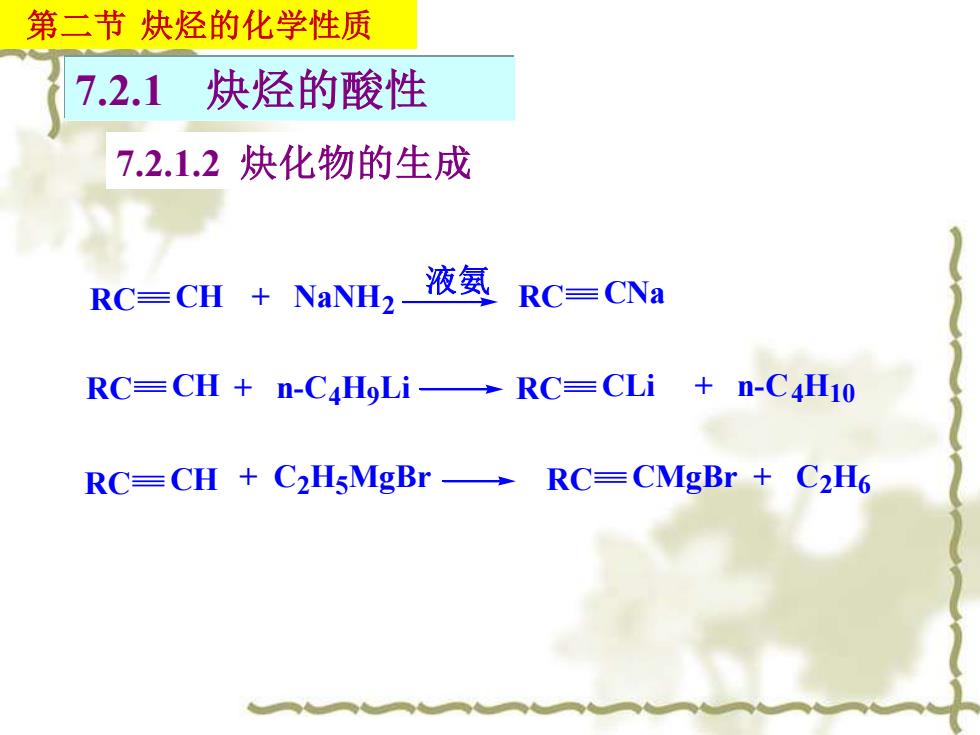
RC CH + NaNH2 液氨 RC CNa RC CH RC CH + n-C4H9Li + C2H5MgBr RC CLi + n-C4H10 RC CMgBr + C2H6 7.2.1 炔烃的酸性 第二节 炔烃的化学性质 7.2.1.2 炔化物的生成
第二节炔烃的化学性质 7.2.1炔烃的酸性 7.2.1.3过渡金属炔化物 NaNH2 R-C=C Na R-C=CH Ag (NH3)2NO3 R-C=CAg Cu (NH3)2CI R-C=CCu 鉴别
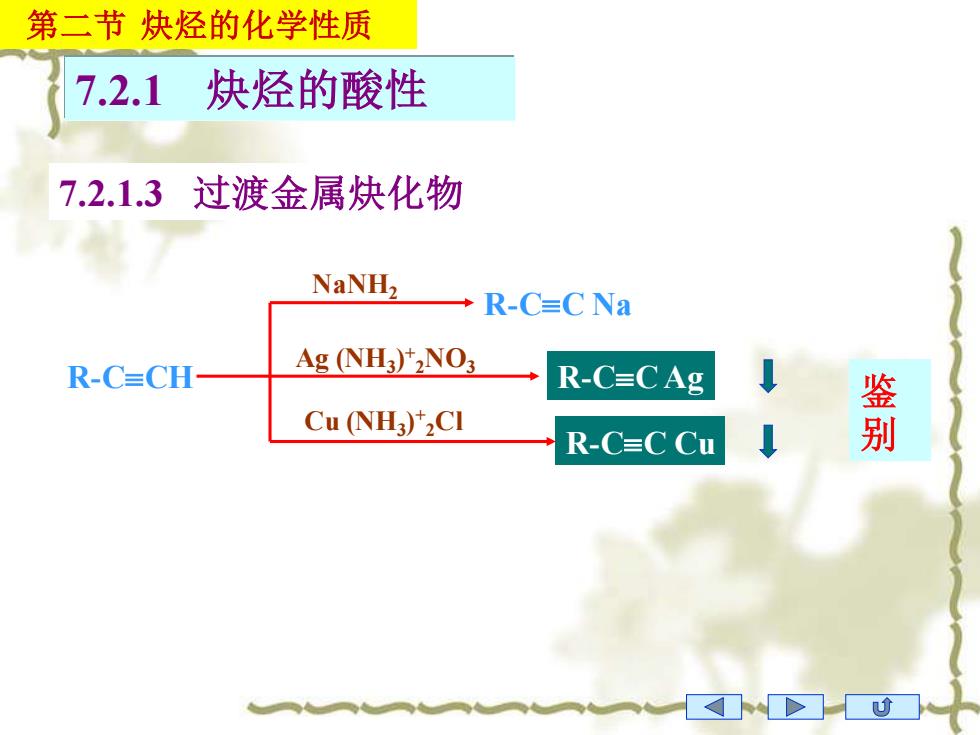
R-CCH R-CC Na R-CC Ag R-CC Cu NaNH2 Ag (NH3 ) + 2NO3 Cu (NH3 ) + 2Cl 鉴 别 7.2.1 炔烃的酸性 第二节 炔烃的化学性质 7.2.1.3 过渡金属炔化物