
§7.4基元反应的反应速率理论简介 反应速率的理论很多,但都不够完满。其中 研究较多,对部分反应较成熟的速率理论有两个: 简单碰撞理论一: 在分子运动论基础上, 以硬球碰撞为模型,也叫硬球碰撞理论。 过渡态理论 一在统计热力学、量子力学 基础上发展起来的速率理论

107 简单碰撞理论(1918)》 Leuis研究双分子、气相基元反应,得到了 与阿氏公式相似的公式。 (1)基本观点: a): 把分子看成刚球,无内部运动,分子接触碰撞 才有可能起反应。 实际分子接近时斥力加大,就改变方向使分子远 离,即完成一次碰撞。两分子所能达到的最小距 离称为碰撞直径(有效直径),碰撞直径稍大于 分子直径(或稍大于两分子的半径和)

108 b)只有活性分子碰撞才能反应。活性分子是 指高能量的分子,或称激烈碰撞才能反应,这 种能发生反应的激烈碰撞一-称作有效碰撞。 有效碰撞率(q):有效碰撞占总碰撞的分数 (碰撞分数),不发生反应的碰撞只传递能量。 ©)发生碰撞的两个分子沿质心连线方向上的相 对平动能超过一定值(E。)时才是有效碰撞。 Ec:临界能,或称阈能

109 不同的反应有不同阈能。相对平动能≥E时 才是有效碰撞。 两个分子的运动方向都在质心连线方向时为 迎头碰撞,这时体系总的相对平动能与质心连 线方向的相对平动能相同;否则应修正成质心 连线方向的相对平动能。碰撞后能否发生反 应,只取决于质心连线方向上的相对平动能是 否大于Ec
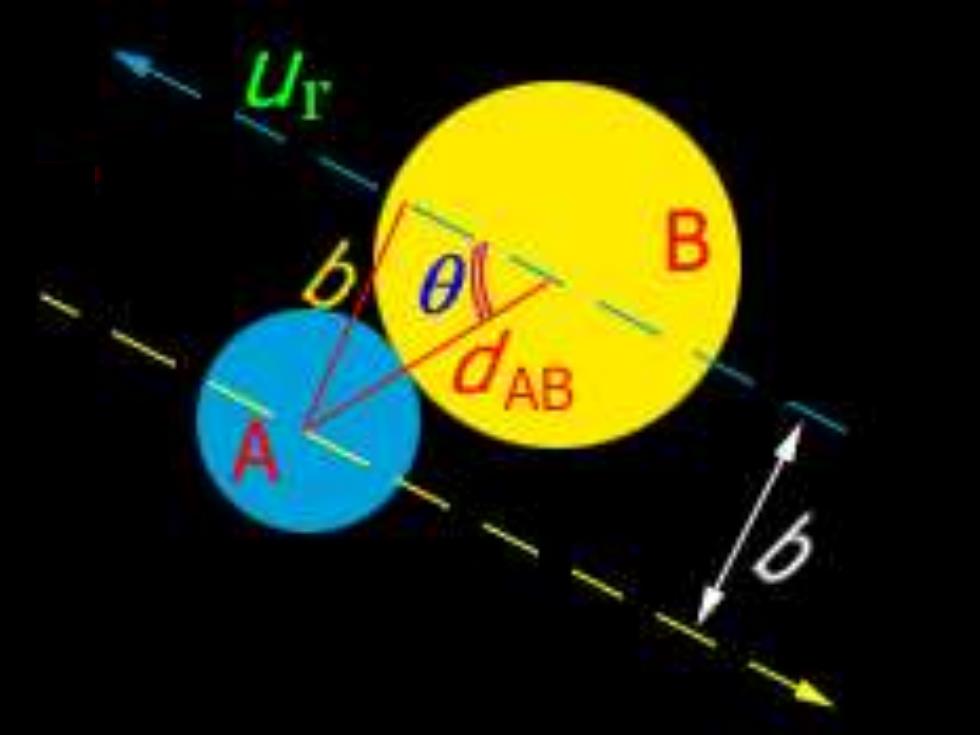
B AB