山东理大子2.势能面Potential energy surfaceGINLANNESIY OHTECHNOLOCYR:A远离BC分子,S: A、B、C三原子完全反应物:A+BC分离状态势能面势能凡势能相同D的点连成曲TABBC线等势能线Q:过渡状态P:C远离AB分子A.B.C产物:AB+C反应途径:R→Q→P
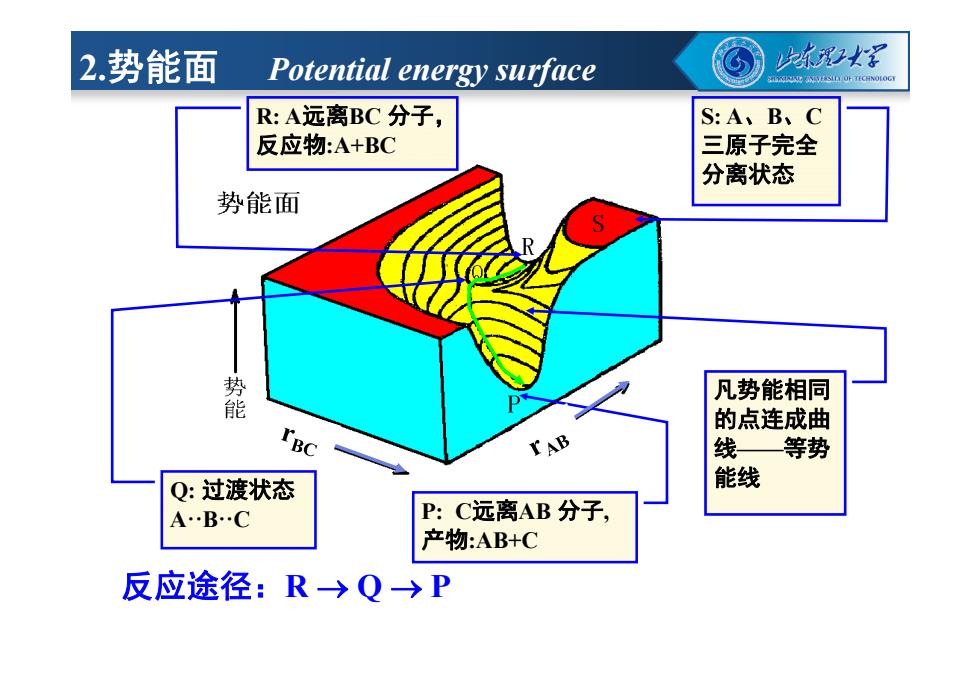
反应途径:R Q P 凡势能相同 的点连成曲 线——等势 能线 S: A、B、C 三原子完全 分离状态 R: A远离BC 分子, 反应物:A+BC P: C远离AB 分子, 产物:AB+C Q: 过渡状态 AꞏꞏBꞏꞏC 2.势能面 Potential energy surface

上东现大2.势能面Potential energy surfaceAEONNESINYOHTECHNOLOGY23456RSTAB65Q3IBC势能面投影图等势能线投影图上:越密则越陡,越稀则越坡
等势能线投影图上:越密则越陡,越稀则越坡, 2.势能面 Potential energy surface
山东理子2.势能面Potential energy surfaceAEONNESINYOHTECHNOLOGY势能[A...B...C]丰势垒&A+BCAB+CRPQ反应途径&,势垒:反应物与活化络合物之间的势能差;定义E,=L&,此即过渡态理论中的活化能
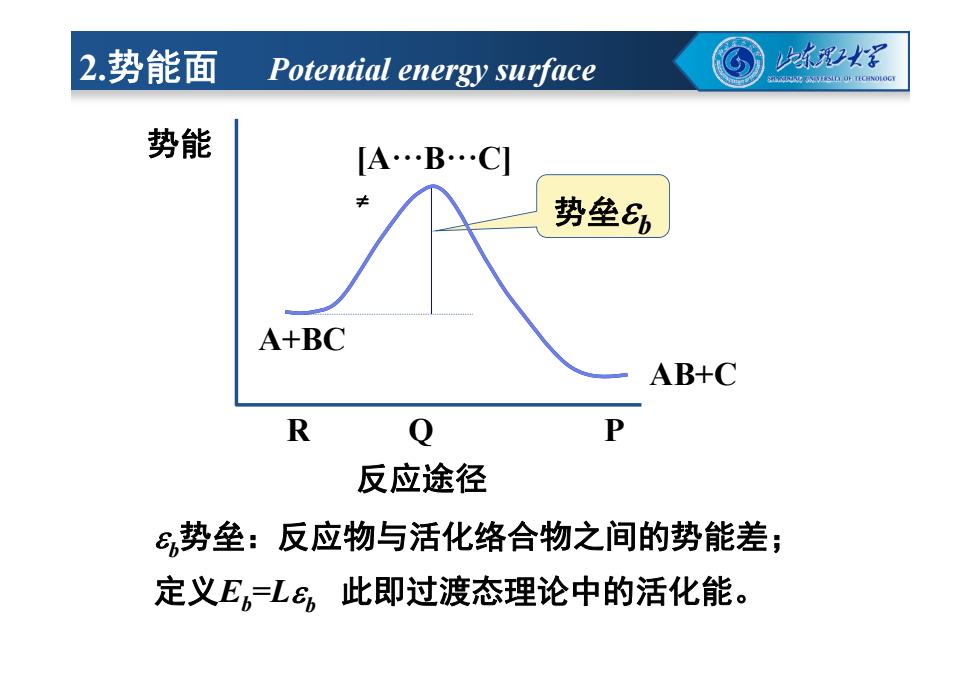
b势垒:反应物与活化络合物之间的势能差; 定义Eb=L b 此即过渡态理论中的活化能。 R Q P 势能 势垒 b A+BC AB+C 反应途径 [AꞏꞏꞏBꞏꞏꞏC] 2.势能面 Potential energy surface

山东理大子S12.2过渡态理论INNE NINESIINIOFTECHNOLOY3.由过渡态理论计算反应速率常数过渡态理论假设:>从反应物到生成物必须获得一定的能量,首先形成活化络合物;>活化络合物的浓度可从它与反应物达成热力学平衡的假设来计算;>一旦形成活化络合物,就向产物转化,这步是反应的速决步
3. 由过渡态理论计算反应速率常数 过渡态理论假设: 从反应物到生成物必须获得一定的能量,首先形成 活化络合物; 活化络合物的浓度可从它与反应物达成热力学平衡 的假设来计算; 一旦形成活化络合物,就向产物转化,这步是反应 的速决步。 §12.2 过渡态理论 3. 由过渡态理论计算反应速率常数

山东子S12.2过渡态理论NALNINEASIIIOFTECHNOLOGT3.由过渡态理论计算反应速率常数设某基元反应为A+B-C-→A-B+CA+B-C_K_[A...B...C]"→A-B+C经推导得反应的速率常数计算公式为AHS(A,se(ck= (c)"explexpRTR若用压力表示,标准态是100kPa,速率常数为Ase(pA,He(pek-年()expexpRRT
§12.2 过渡态理论 3. 由过渡态理论计算反应速率常数 c ABC A B C ABC K 设某基元反应为 ABC ABC 1 rm r m B exp exp k T n Sc Hc k c h R RT 若用压力表示,标准态是100 kPa,速率常数为 1 B rm r m exp exp n kT p Sp Hp k h RT R RT 经推导得反应的速率常数计算公式为