
这是因为按SN2历程进行反应,因空间位阻较大, 不利于亲核试剂从背后进攻中心碳原子,反应难 以进行。若按SN1历程进行反应,虽然生成的中 间体是稳定性很小的伯碳正离子,反应速率较慢, 但因伯碳正离子可重排为稳定的叔碳正离子,故 得到的是重排产物。 醇的亲核取代反应要比卤代烷困难,其原因在 于醇羟基的碱性较强,是个不好的离去基团。 碱性 :HO>X
这是因为按SN2历程进行反应,因空间位阻较大, 不利于亲核试剂从背后进攻中心碳原子,反应难 以进行。若按SN1历程进行反应,虽然生成的中 间体是稳定性很小的伯碳正离子,反应速率较慢, 但因伯碳正离子可重排为稳定的叔碳正离子,故 得到的是重排产物。 醇的亲核取代反应要比卤代烷困难,其原因在 于醇羟基的碱性较强,是个不好的离去基团。 碱 性: HO > X

实验表明:强酸的负离子,如C-《一s0,0、x等是较 好的离去基团;而H0、0、NH等则是不好的离去基团。 因此,醇的亲核取代反应需在酸催化下进行,或将醇羟 基先转化为好的离去基团,以利于反应的进行。 CH.CH,GHCCmCH.CHCHCH.CH CH.CH.CHCH.CH, NaBr OH OTs Br (=CH-Cs02) 侵
实验表明:强酸的负离子,如 CH3 SO2O 、 X 等是较 好的离去基团;而 HO 、RO 、NH2 等则是不好的离去基团。 因此,醇的亲核取代反应需在酸催化下进行,或将醇羟 基先转化为好的离去基团,以利于反应的进行。 CH3CH2CHCH2CH3 OH TsCl CH3CH2CHCH2CH3 OTs NaBr (CH3 ) 2 SO CH3CH2CHCH2CH3 Br 吡 啶 Ts = CH3 SO2
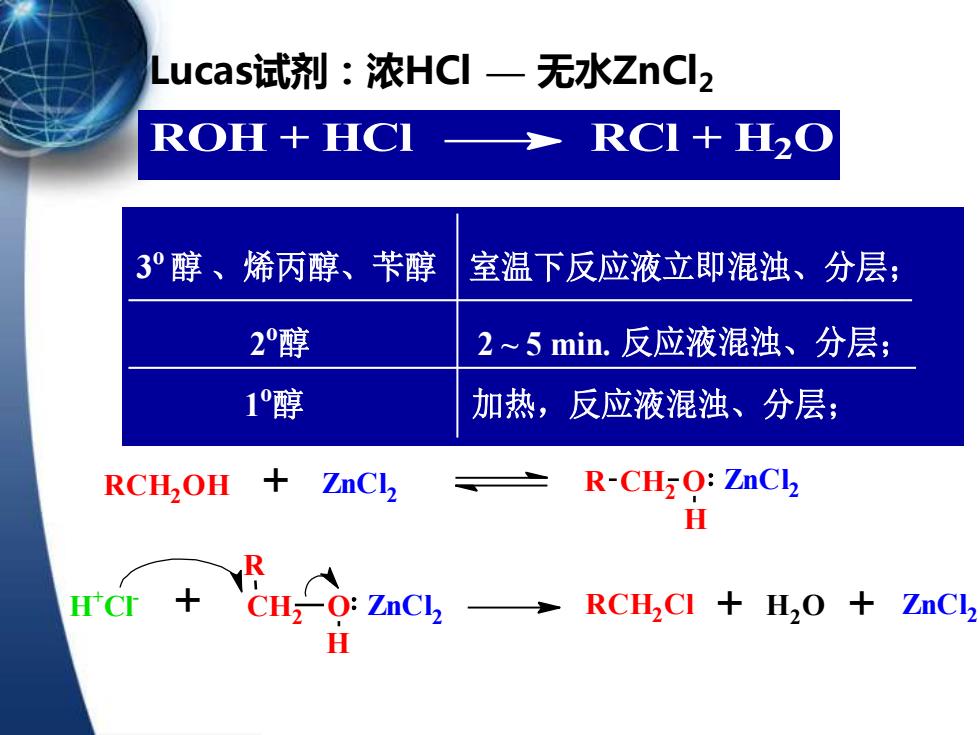
Lucas试剂:浓HCl一无水ZnCl2 ROH+HCI RCI+H2O 3°醇、烯丙醇、苄醇 室温下反应液立即混浊、分层; 2醇 2~5min.反应液混浊、分层; 1醇 加热,反应液混浊、分层; RCH,OH+ ZnCl, R-CH-O:ZnCl H H'cr CH,0:ZnC→ RCH2CI H2O ZnCl, H
3 o 醇 、烯丙醇、苄醇 室温下反应液立即混浊、分层; 2 o 醇 2 ~ 5 min. 反应液混浊、分层; 1 o 醇 加热,反应液混浊、分层; Lucas试剂:浓HCl — 无水ZnCl2 ROH + HCl RCl + H2 O RCH2 O H + ZnCl2 R C H2 O H ZnCl2 H + Cl- + R C H2 O H ZnCl2 RCH2 Cl H2 O ZnCl + + 2

②与PX3作用: 醇与三卤化磷反应,得到不发生重排反应的卤代烃,该 法用于制备溴代烃或碘代烃。 3ROH PBr3 3RBr P(OH) 6ROH 312 2P->6RI 2H3PO 三氯化磷有时会得到副产物磷酸酯,用二氯亚砜较好
② 与PX3作用: 三氯化磷有时会得到副产物磷酸酯,用二氯亚砜较好。 3ROH + PBr3 3RBr P(OH) + 3 6ROH 3I2 + + 2P 6R I + 2H3 PO4 醇与三卤化磷反应,得到不发生重排反应的卤代烃,该 法用于制备溴代烃或碘代烃
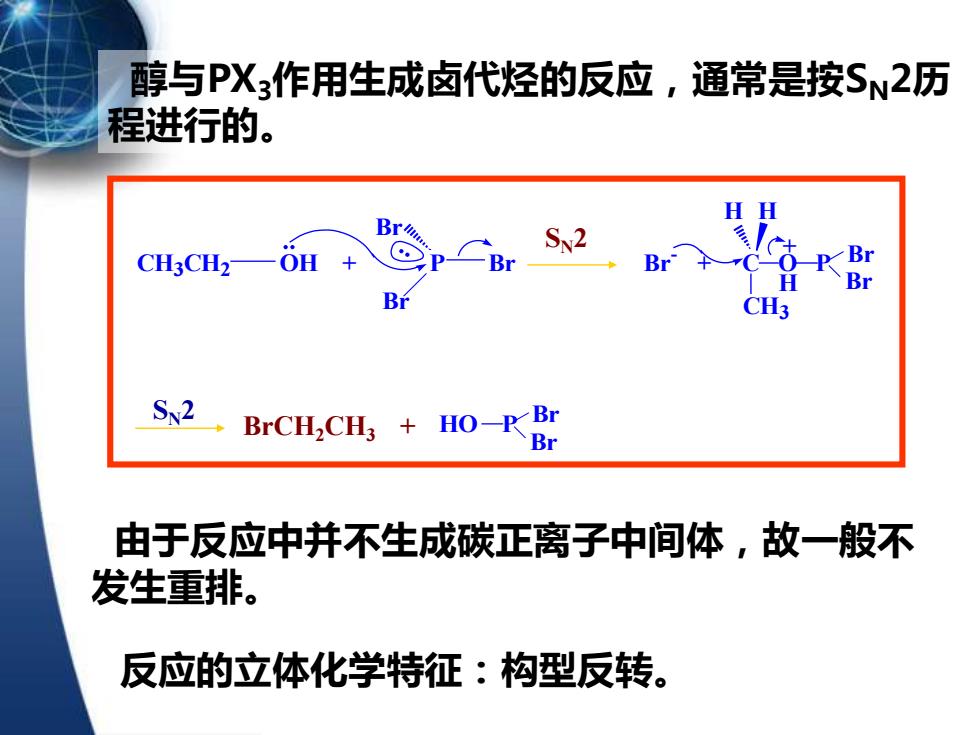
醇与PX3作用生成卤代烃的反应,通常是按SN2历 程进行的。 H Br CH3CH2—( Br Br Br CH3 Sx2 BrCH2CH HO-KBE r 由于反应中并不生成碳正离子中间体,故一般不 发生重排。 反应的立体化学特征:构型反转
醇与PX3作用生成卤代烃的反应,通常是按SN2历 程进行的。 由于反应中并不生成碳正离子中间体,故一般不 发生重排。 反应的立体化学特征:构型反转。 SN2 SN2 Br Br BrCH HO P 2CH3 + CH3CH2 OH + P Br Br Br Br - + C O P H CH3 Br Br H H +