
物理性质特点是存在分子间的氢键作用 为什么醇具有较高的沸点? (分子间氢键缔合) 醇分子中烃基对氢键缔合有阻碍作用。 多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5C 197℃ 290℃
物理性质 特点是存在分子间的氢键作用 为什么醇具有较高的沸点? (分子间氢键缔合) 醇分子中烃基对氢键缔合有阻碍作用。 多元醇,分子中两个以上位置可形成氢键。 乙醇 乙二醇 丙三醇 78.5 o C 197 o C 290 o C O H R O R H O H R H O R
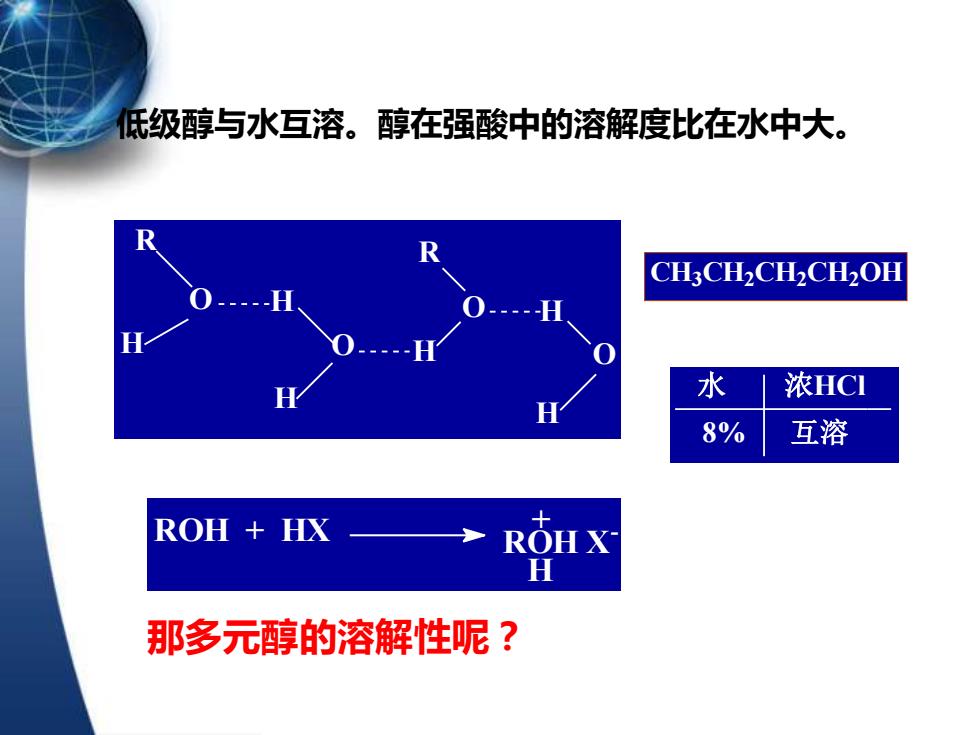
低级醇与水互溶。醇在强酸中的溶解度比在水中大。 CH3CH2CH2CH2OH 水 浓HC】 8% 互溶 ROH HX ROHX H 那多元醇的溶解性呢?
R O H H O H H O R H O H ROH + HX ROH X - H + CH3CH2CH2CH2OH 水 浓HCl 8% 互溶 低级醇与水互溶。醇在强酸中的溶解度比在水中大。 那多元醇的溶解性呢?
醇化物(结晶醇) 低级醇与一些无机盐形成的结晶状分子化合物称之为结晶 醇,也称之为醇化物。 MgCL2●6CH3OH CaCl2●4C2HsOH 注意 结晶醇不溶于有机 工业乙醚常杂有 溶剂而溶于水。利 许多无机盐 用这一性质,可以 少量乙醇,加入 CaCl,可使醇从 不能作为醇 使醇和其它有机溶 乙醚中沉淀下来。 的干燥剂。 剂分开,或从反应 物中除去醇类
醇化物(结晶醇) 低级醇与一些无机盐形成的结晶状分子化合物称之为结晶 醇,也称之为醇化物。 MgCl2• 6CH3OH CaCl2 • 4C2H5OH 注意 许多无机盐 不能作为醇 的干燥剂。 结晶醇不溶于有机 溶剂而溶于水。利 用这一性质,可以 使醇和其它有机溶 剂分开,或从反应 物中除去醇类。 工业乙醚常杂有 少量乙醇,加入 CaCl2可使醇从 乙醚中沉淀下来
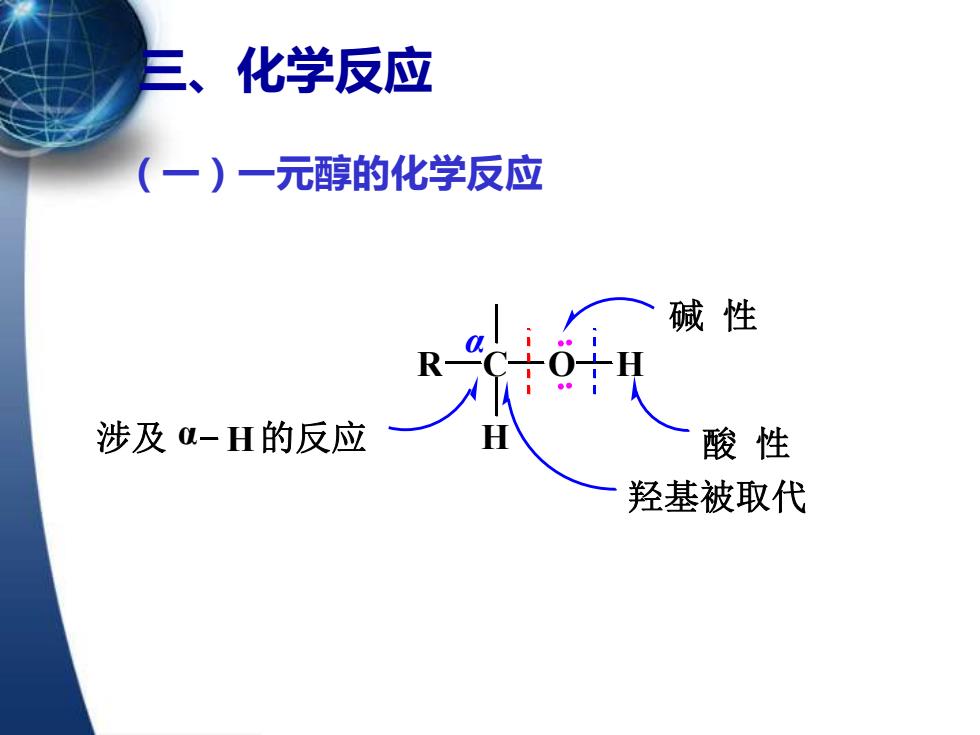
化学反应 (一)一元醇的化学反应 碱性 涉及-H的反应 酸性 羟基被取代
三、化学反应 R C O H H : : 碱 性 酸 性 α 羟基被取代 涉及 α H的反应 (一)一元醇的化学反应

1.醇中氧氢键(O-H)断裂的反应 酸性:与碱金属反应 C2H5OH+Na C2H5ONa + 2H2 3 (CH3)CHOH Al (CH3)2CHO 3AI 1+12 R-ONa H2O NaOH ROH (生成的醇钠可以被水破坏,说明醇羟基中的氢不如水分子 中的氢活泼,醇是比水更弱的酸,甘共扳碱(R-ONa)的 碱性比NaOH强) 苯:乙醇:水 =74.1:18.5:7.4(64.9) C2HOH+NaOH C2HONa +H2O
1. 醇中氧氢键(O-H)断裂的反应 2 1 2 1 3 (CH3) 2CHOH + Al (CH3 ) 2 CHO 3 Al + 1 C2H5OH + Na C2H5ONa + H2 H2 酸性:与碱金属反应 R-ONa + H2 O NaOH + ROH (生成的醇钠可以被水破坏,说明醇羟基中的氢不如水分子 中的氢活泼,醇是比水更弱的酸,其共轭碱(R-ONa)的 碱性比NaOH强) C2H5OH + NaOH C2H5ONa +H2O 苯乙醇水 =74.118.57.4(64.9)