
二、烷烃的构造异构 烷烃同系列中,甲烷、乙烷、丙烷只有 一种结合方式,没有异构现象,从丁烷起就 有同分异构现象。 CH3-CH2-CH2-CH3 CH3-CH-CH3 CH3 前者称为正丁烷,后者称为异丁烷。显然,正丁烷 和异丁烷是同分异构体。这种由分子中各原子的不同连 接方式和次序而引起的同分异构现象叫做构造异构。他 们的不同是碳原子间相连形成的碳链发生了变化,因此 又叫做碳链异构
烷烃同系列中,甲烷、乙烷、丙烷只有 一种结合方式,没有异构现象,从丁烷起就 有同分异构现象。 二、烷烃的构造异构 CH3 CH2 CH2 CH3 CH3 CH CH3 CH3 前者称为正丁烷,后者称为异丁烷。显然,正丁烷 和异丁烷是同分异构体。这种由分子中各原子的不同连 接方式和次序而引起的同分异构现象叫做构造异构。他 们的不同是碳原子间相连形成的碳链发生了变化,因此 又叫做碳链异构
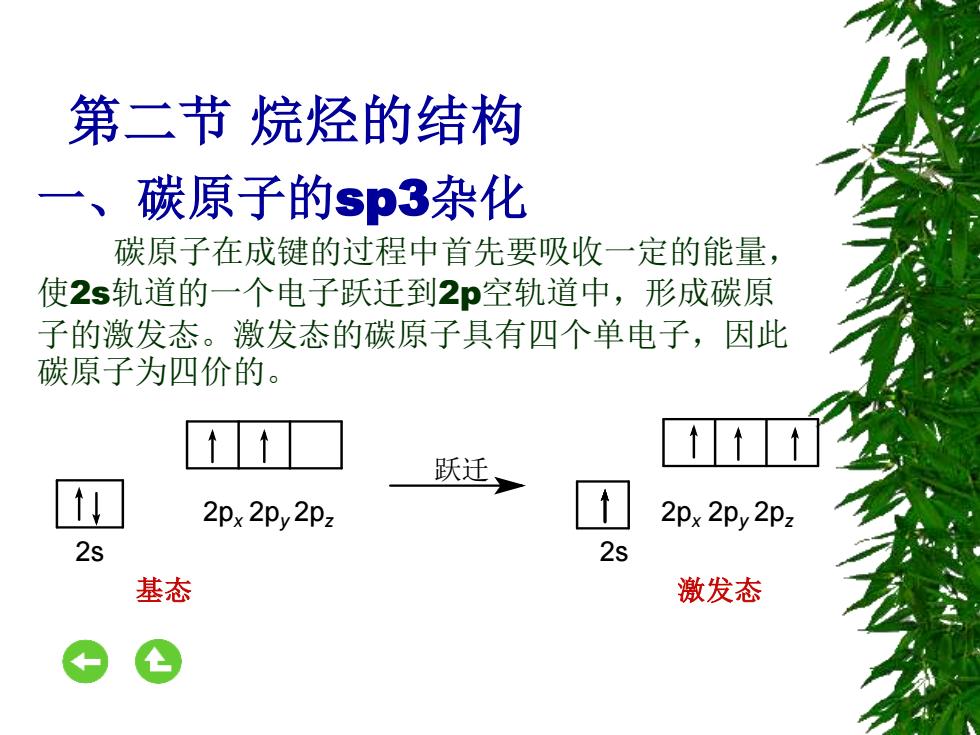
第二节烷烃的结构 一、碳原子的sp3杂化 碳原子在成键的过程中首先要吸收一定的能量, 使2s轨道的一个电子跃迁到2p空轨道中,形成碳原 子的激发态。激发态的碳原子具有四个单电子,因此 碳原子为四价的。 跃迁 2px 2py 2pz 2px 2py 2pz 2s 2s 基态 激发态
第二节 烷烃的结构 一、碳原子的sp3杂化 碳原子在成键的过程中首先要吸收一定的能量, 使2s轨道的一个电子跃迁到2p空轨道中,形成碳原 子的激发态。激发态的碳原子具有四个单电子,因此 碳原子为四价的。 跃迁 2px 2py 2pz 2px 2py 2pz 2s 2s 基态 激发态
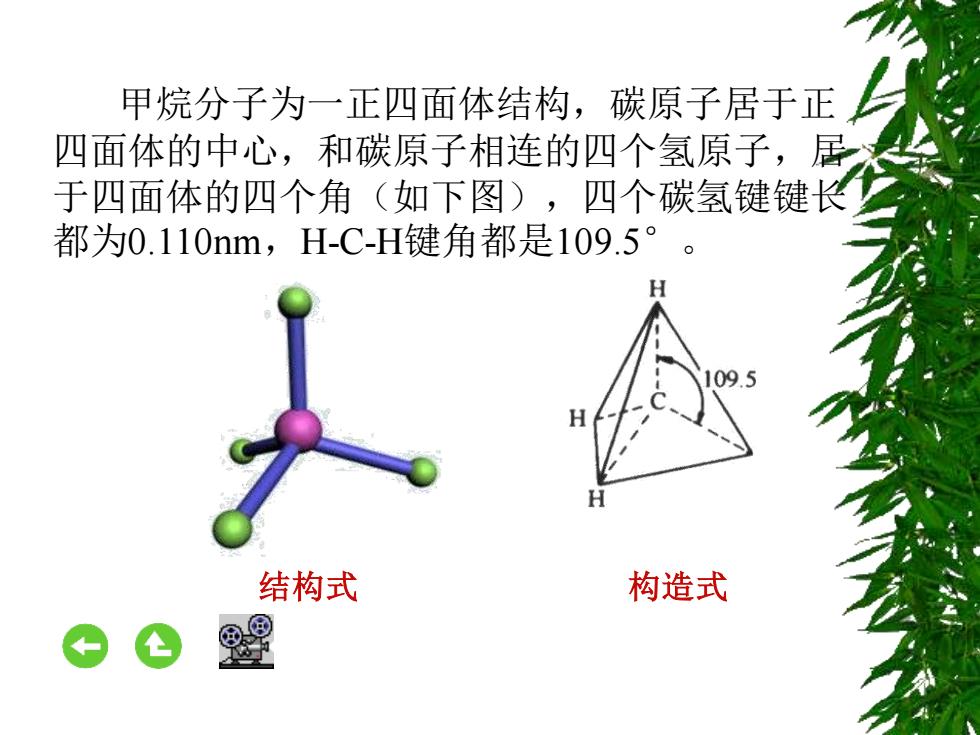
甲烷分子为一正四面体结构,碳原子居于正 四面体的中心,和碳原子相连的四个氢原子,居 于四面体的四个角(如下图),四个碳氢键键长 都为0.110nm,H-C-H键角都是109.5 H 结构式 构造式
甲烷分子为一正四面体结构,碳原子居于正 四面体的中心,和碳原子相连的四个氢原子,居 于四面体的四个角(如下图),四个碳氢键键长 都为0.110nm,H-C-H键角都是109.5° 。 结构式 构造式

Sp3杂化轨道构型
Sp3杂化轨道构型
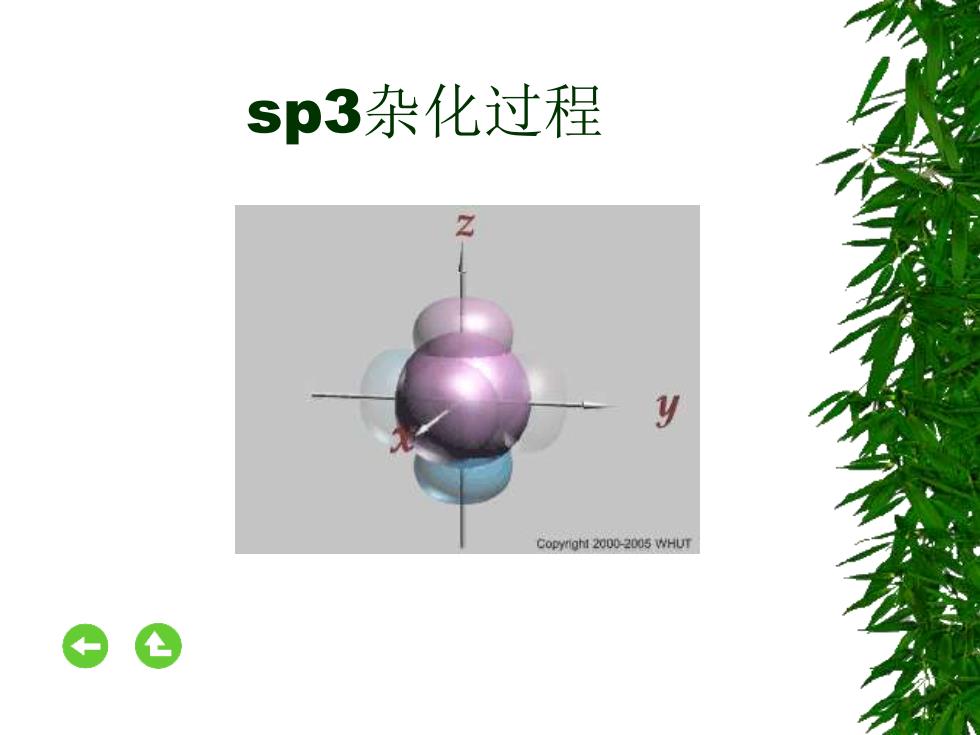
sp3杂化过程 y Copynght 2000-2005 WHUT
sp3杂化过程