
PRL,100,073003(2008),J.Mauritsson,K.J.Schafer
PRL, 100, 073003 (2008), J. Mauritsson,K. J. Schafer

1.3原子结构 原子(Atom) 原子核+核外电子 原子核 质子+中子 质子 质子数(亿)=原子序数=电子数 正电荷 中子 中子数()中子质量≈质子质量 无电荷 原子质量(A) 质子质量+中子质量 同位素: Z相同,N不同的原子 原子量: 元素(原子序数相同)中各同位素 的原子质量的平均值。 电子 质量约1/1836质子或1/1839中子 负电荷 波粒 轨道非固定,几率最大的分布构成电子云层 绕核运动 速度1/101/100光速
1.3 原子结构 原子(Atom) 原子核+核外电子 原子核 质子+中子 质子 质子数(Z)=原子序数=电子数 正电荷 中子 中子数(N) 中子质量≈质子质量 无电荷 原子质量(A) 质子质量+中子质量 同位素: Z相同,N不同的原子 原子量: 元素(原子序数相同)中各同位素 的原子质量的平均值。 电子 质量约1/1836质子或1/1839中子 负电荷 波-粒 轨道非固定,几率最大的分布构成电子云层 绕核运动 速度1/10 1/100光速
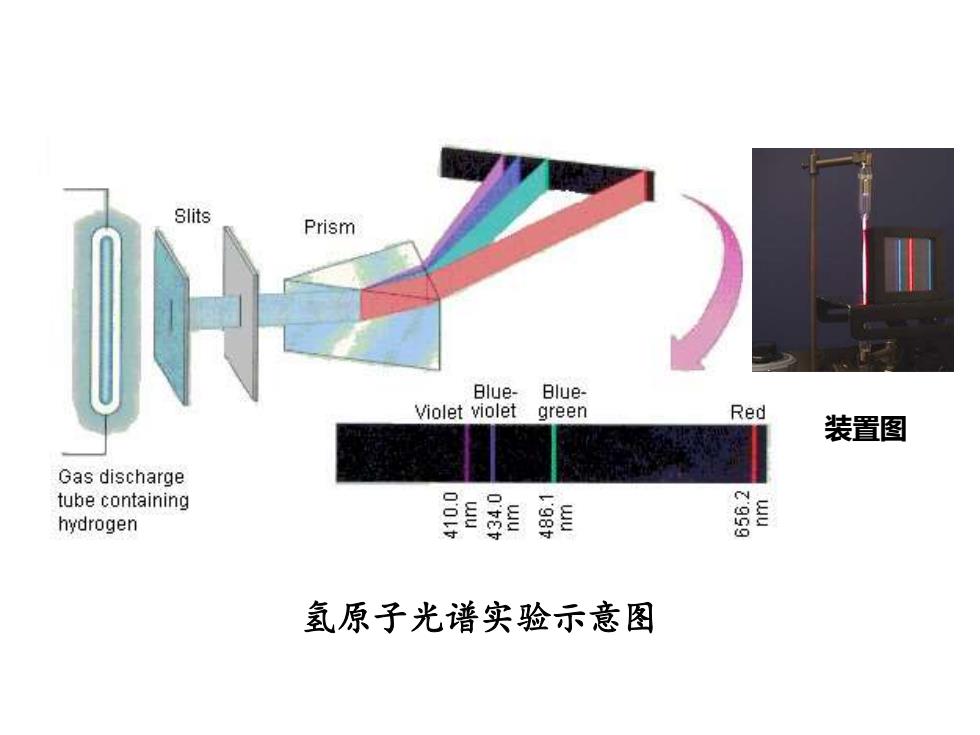
Slits Prism Blue-Blue- Violet violet green Red 装置图 Gas discharge tube containing hydrogen 目 目 氢原子光谱实验示意图
氢原子光谱实验示意图 装置图
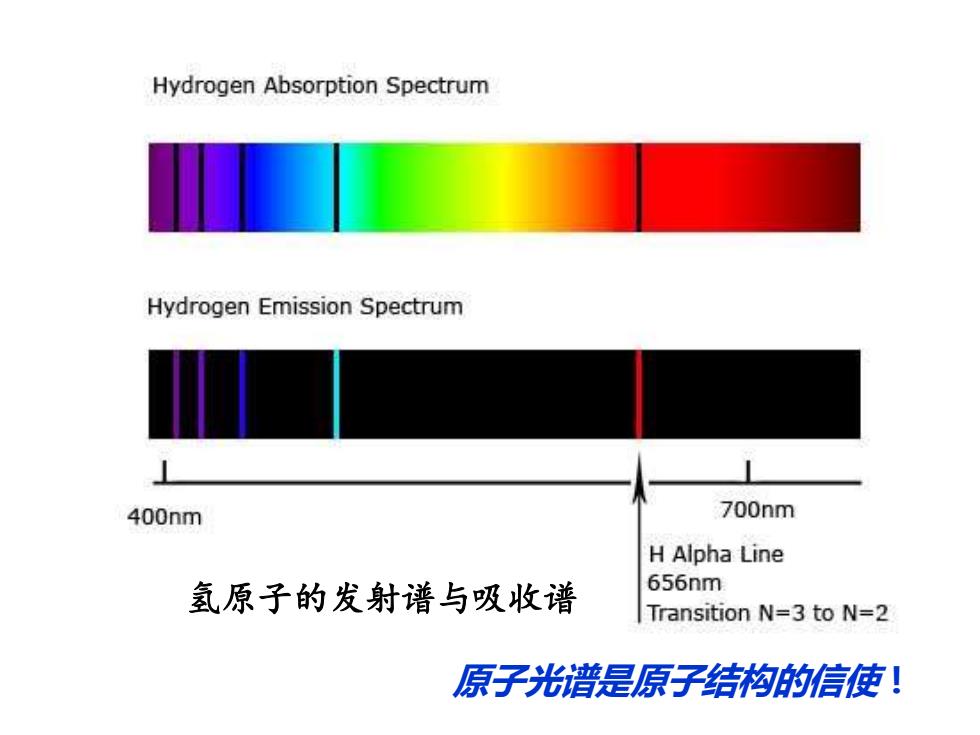
Hydrogen Absorption Spectrum Hydrogen Emission Spectrum 400nm 700nm H Alpha Line 氢原子的发射谱与吸收谱 656nm Transition N=3 to N=2 原子光谱是原子结构的信使!
氢原子的发射谱与吸收谱 原子光谱是原子结构的信使!
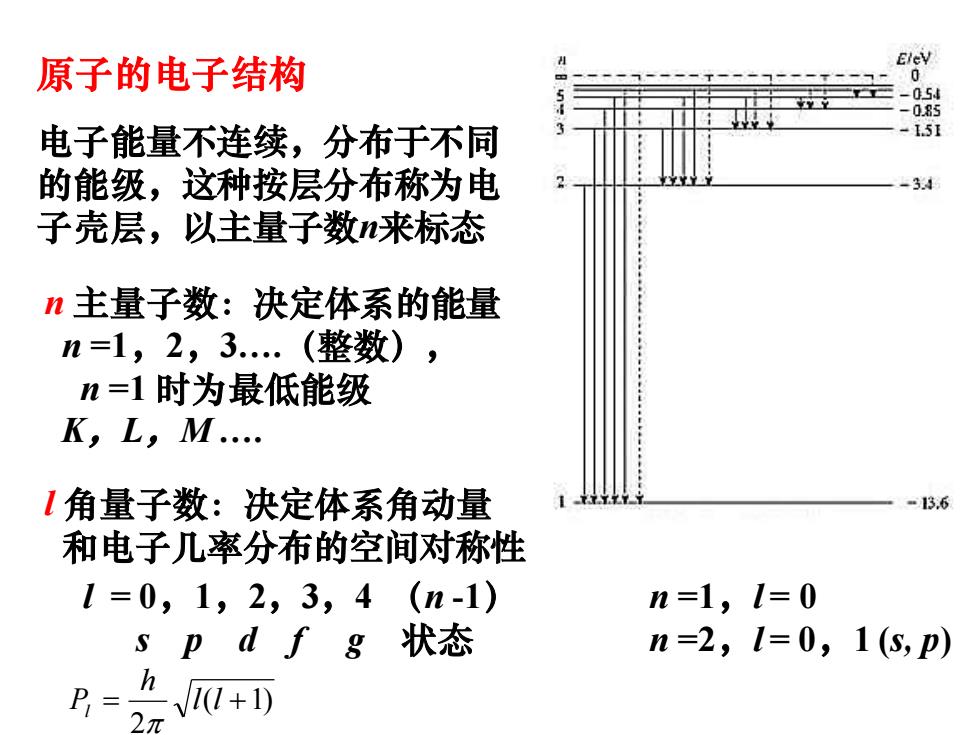
原子的电子结构 0 -054 -085 电子能量不连续,分布于不同 的能级,这种按层分布称为电 3.4 子壳层,以主量子数n来标态 n主量子数:决定体系的能量 n=1,2,3.(整数), n=1时为最低能级 K,L,M. 1角量子数:决定体系角动量 -13,6 和电子几率分布的空间对称性 1=0,1,2,3,4(n-1) n=1,l=0 s pd fg状态 n=2,l=0,1(s,p) P1= 、0+0 2π
电子能量不连续,分布于不同 的能级,这种按层分布称为电 子壳层,以主量子数n来标态 n 主量子数:决定体系的能量 n =1,2,3.(整数), n =1 时为最低能级 K,L,M . ( 1) 2 = l l + h Pl l 角量子数:决定体系角动量 和电子几率分布的空间对称性 l = 0,1,2,3,4 (n -1) n =1,l = 0 s p d f g 状态 n =2,l = 0,1 (s, p) 原子的电子结构