
4.17),这是由于苯环的大π键与羧基可以形成ππ共轭体系,羧基的吸电子共 轭效应,使环上的电子云向羧基偏移,减弱了氢氧键的极性,氢的解离能力降低, 故酸性比甲酸弱。 二元羧酸含有两个羧基,第一步解离时受到另一个羧基吸电子诱导效应的影 响,解离比一元羧酸要容易,第二步解离时受到己经解离的羧基给电子诱导效应 的影响,其解离比一元羧酸要难,K>K。>K。两个羧基距离越近,影响越大。 二元羧酸的电离常数见表9-1。 综上所述,羧酸的酸性强弱顺序如下: 二元羧酸>甲酸>苯甲酸>其他饱和一元羧酸 一元羧酸具有一定的酸性,其酸性比盐酸、硫酸等无机强酸的酸性要弱,但 比碳酸和酚类的酸性强。羧酸与其他有关化合物的酸性强弱顺序如下: HsO.HCI RCOOH HCO,>O HO>RO 所以羧酸可以与NaOH、NaCO、NaHCO3发生反应,常用与NaHCO反应 放出CO2气体来鉴别羧酸。 R-COOH+NaOH R-COONa+H20 R-CO0H+Na,CO3→R-C0ONa+CO2↑+H,0 R-COOH+NaHCO,→R-COONa+CO,↑+H0 ②H0 4-CH-O .COO.CCHCOOHOOC-COOHC.COOH (二)搬基上羟基的取代反应 羧酸分子中羧基上的羟基被卤素、酰氧基、烷氧基和氨基取代,生成相应的 酰卤、酸酐、酯和酰胺等羧酸衍生物。羧酸分子中去掉羟基剩余的部分(RC-) 称为酰基。 1.酰卤的生成羧基中的羟基被卤素取代后的产物称为酰卤。酰氯是常见的 酰卤,它可由羧酸与三氯化磷、五氯化磷或亚硫酰氯反应生成
4.17),这是由于苯环的大 π 键与羧基可以形成 π-π 共轭体系,羧基的吸电子共 轭效应,使环上的电子云向羧基偏移,减弱了氢氧键的极性,氢的解离能力降低, 故酸性比甲酸弱。 二元羧酸含有两个羧基,第一步解离时受到另一个羧基吸电子诱导效应的影 响,解离比一元羧酸要容易,第二步解离时受到已经解离的羧基给电子诱导效应 的影响,其解离比一元羧酸要难,Ka1>Ka >Ka2。两个羧基距离越近,影响越大。 二元羧酸的电离常数见表 9-1。 综上所述,羧酸的酸性强弱顺序如下: 二元羧酸>甲酸>苯甲酸>其他饱和一元羧酸 一元羧酸具有一定的酸性,其酸性比盐酸、硫酸等无机强酸的酸性要弱,但 比碳酸和酚类的酸性强。羧酸与其他有关化合物的酸性强弱顺序如下: H2SO4、HCl > RCOOH > H2CO3 > > > OH H2O ROH 所以羧酸可以与 NaOH、Na2CO3、NaHCO3 发生反应,常用与 NaHCO3 反应 放出 CO2 气体来鉴别羧酸。 R COOH + NaOH R COONa + H2O R R COOH + Na2CO3 R COONa + CO2 R COOH + NaHCO3 COONa + CO2 + H2O + H2O 课堂互动 试将下列各组化合物按酸性由强到弱顺序排列 (1)①CH3COOH,②H2O,③CH3CH2OH,④C6H5OH,⑤NH3,⑥H2CO3 (2)①CH3COOH,②HCOOH,③(CH3)2CH-COOH,④HOOC-COOH,⑤ C6H5COOH (二)羧基上羟基的取代反应 羧酸分子中羧基上的羟基被卤素、酰氧基、烷氧基和氨基取代,生成相应的 酰卤、酸酐、酯和酰胺等羧酸衍生物。羧酸分子中去掉羟基剩余的部分( = R C O ) 称为酰基。 1.酰卤的生成 羧基中的羟基被卤素取代后的产物称为酰卤。酰氯是常见的 酰卤,它可由羧酸与三氯化磷、五氯化磷或亚硫酰氯反应生成
0 0 R-C-OH PCI -R-e-CI+HgPOs 三氯化磷 酰氯 亚磷酸 -l rCR8c+OC,IGt 五氯化磷 酰氯三氯氧磷 R8OH SOChR8CI+s0.1+HCI 0 亚疏酰氯 酰氯 (氯化亚飘) 制备酰氯常用的方法是亚硫酰氯与羧酸反应,因该反应生成的副产物都是气 体,在反应中随时逸出,可得到较纯净的酰氯。酰氯很活泼,它是一类具有高度 反应活性的化合物,广泛用于药物和有机合成中。 2.酸酐的生成羧酸在脱水剂(如P2O)作用下加热,2个羧基间失去一分子 水,生成酸酐。 R-8OH+HO-R 酸酐 具有4个或5个碳原子的二元酸(如丁二酸、戊二酸、邻苯二甲酸等)加热, 分子内脱水,形成较稳定的五元环或六元环的环状酸酐(环酐)。如: CH2-C-OH 6 t-8 丁二酸 丁二酸酐 0 邻苯二甲酸 邻苯二甲酸酐 3.酯的生成在少量酸(如浓硫酸)的催化作用下,羧酸可与醇反应生成酯 该反应称为酯化反应。有机酸和醇的酯化反应速度极慢,必须在酸的催化及加热 下进行。 0 ,浓Hs0R-&0R+0 0 R2oH+RoH△ 羧酸 醇
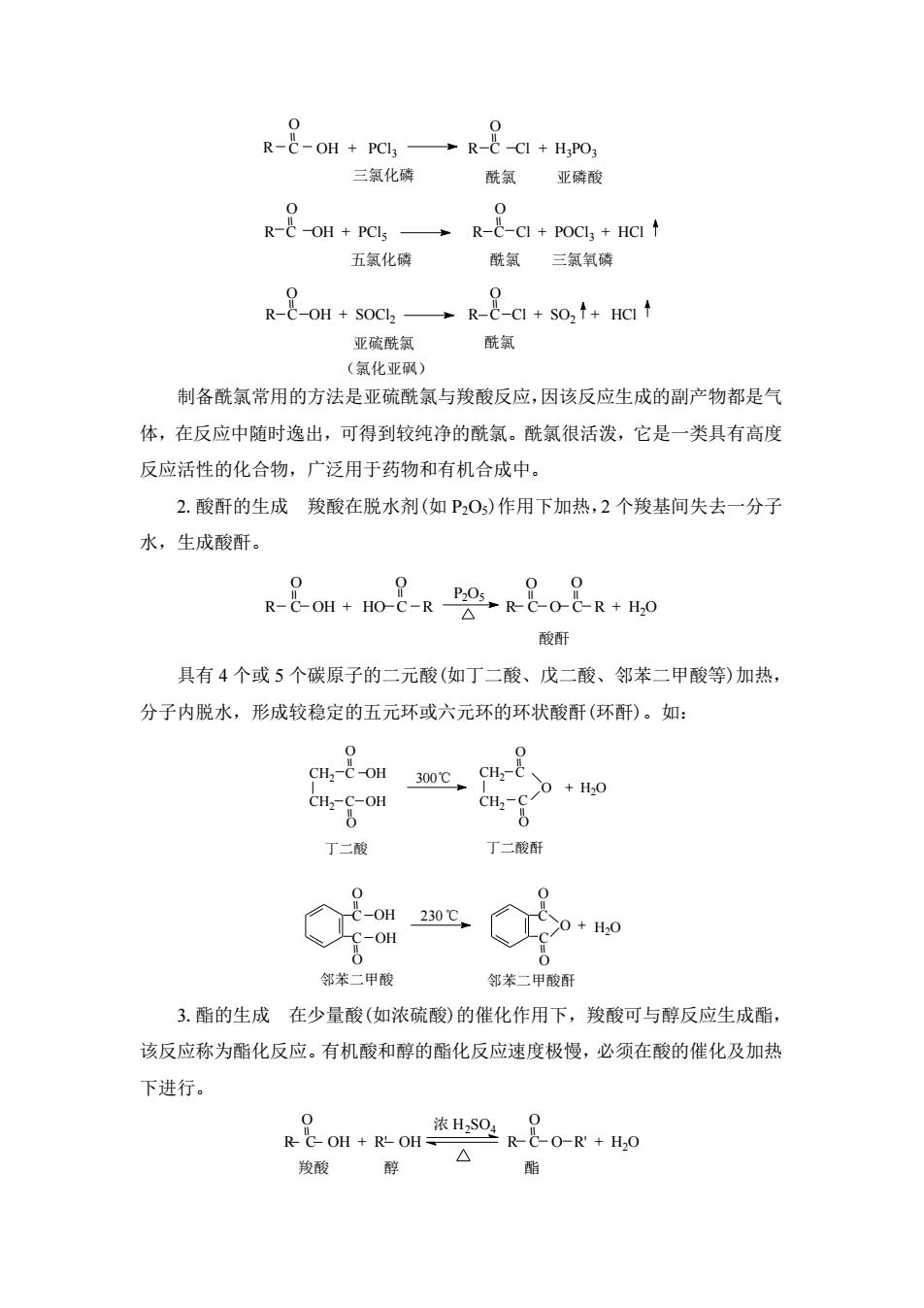
三氯化磷 酰氯 亚磷酸 五氯化磷 酰氯 三氯氧磷 亚硫酰氯 (氯化亚砜) 酰氯 R C OH + PCl3 R C Cl + H3PO3 = = O O = = O O R C OH + PCl5 R C Cl + POCl3 + HCl = = O O R C OH + SOCl2 R C Cl + SO2 + HCl 制备酰氯常用的方法是亚硫酰氯与羧酸反应,因该反应生成的副产物都是气 体,在反应中随时逸出,可得到较纯净的酰氯。酰氯很活泼,它是一类具有高度 反应活性的化合物,广泛用于药物和有机合成中。 2.酸酐的生成 羧酸在脱水剂(如 P2O5)作用下加热,2 个羧基间失去一分子 水,生成酸酐。 酸酐 R C OH + HO C R R C O C R + H2O = = P2O5 = = O O O O 具有 4 个或 5 个碳原子的二元酸(如丁二酸、戊二酸、邻苯二甲酸等)加热, 分子内脱水,形成较稳定的五元环或六元环的环状酸酐(环酐)。如: 丁二酸 丁二酸酐 CH2 C OH = = = = CH2 C OH O O CH2 C CH2 C O O O 300℃ + H2O 邻苯二甲酸 邻苯二甲酸酐 = = = = C C O O O O C C OH OH O + H2O 230℃ 3.酯的生成 在少量酸(如浓硫酸)的催化作用下,羧酸可与醇反应生成酯, 该反应称为酯化反应。有机酸和醇的酯化反应速度极慢,必须在酸的催化及加热 下进行。 羧酸 醇 酯 = O R C OH + R' OH R C O R' + H2O = 浓 H O 2SO4