
后酒子大学 Shihezi University 当反应达到平衡时, g°+ .059V, 0.059V, 01=02 lg- -1g 乃 Aped Agedz 两边同乘以2,和的最小公倍数n,则 n=nl a %=n/b 整理后得 品.ka 三 gK n(p°-p) 0.059V 口式中为氧化还原反应平衡常数。其大小反映了氧化还原反 应进行的程度。 口上式表明,氧化还原反应的平衡常数与两电对的标准电极电 位及电子转移数有关
n n / a 1 = n2 = n / b 1 2 1 2 a b θ θ Red Ox 1 2 a b Ox Red n( - ) lg lgK 0.059V a a a a ϕ ϕ = = 两边同乘以n11和n22的最小公倍数n,则 整理后得 � 式中K为氧化还原反应平衡常数 为氧化还原反应平衡常数。其大小反映了氧化还原反 。其大小反映了氧化还原反 应进行的程度。 应进行的程度。 � 上式表明,氧化还原反应的平衡常数与两电对的标准电极电 上式表明,氧化还原反应的平衡常数与两电对的标准电极电 位及电子转移数有关。 位及电子转移数有关。 ϕ1 = ϕ2 = 当反应达到平衡时, 当反应达到平衡时, 1 1 θ Ox 1 1 Red 0 059V lg . a n a ϕ + 2 2 θ Ox 2 2 Red 0 059V lg . a n a = ϕ +

后酒子大 Shihezi University 条件平衡常数K 若考虑溶液中各种副反应的影响,以相应的条件电位代替标 准电极电位,相应的活度也应以总浓度代替,即 东s-leK-noe2 0.059V 条件平衡常数·能更好地反映实际情况下反应进行的程度
条件平衡常数Kˊ 若考虑溶液中各种副反应的影响,以相应的条件电位代替标 若考虑溶液中各种副反应的影响,以相应的条件电位代替标 准电极电位,相应的活度也应以总浓度代替, 准电极电位,相应的活度也应以总浓度代替, 即 1 2 1 2 a b θ θ Red Ox 1 2 a b Ox Red n( - ) lg lgK 0.059V c c c c ϕ ϕ = = ˊ ˊ ˊ 条件平衡常数Kˊ能更好地反映实际情况下反应进行的程度。 能更好地反映实际情况下反应进行的程度
后调子大学 Shihezi University 三。化学计量点时反应进行的程度 根据滴定分析误差要求,一般在化学计量点时反应完全程度至 少应达到99.9%以上,未反应物应小于0.1%。 aOx bRed2 aRed+bOx2 lgK =lg ,(99.9%2(99.9% COx Red, (0.16)2(0.1%° ≈lg103a10b=3(a+b) a-leK-noo】 b mo-) 0.059V 3(a+b) 0.059V
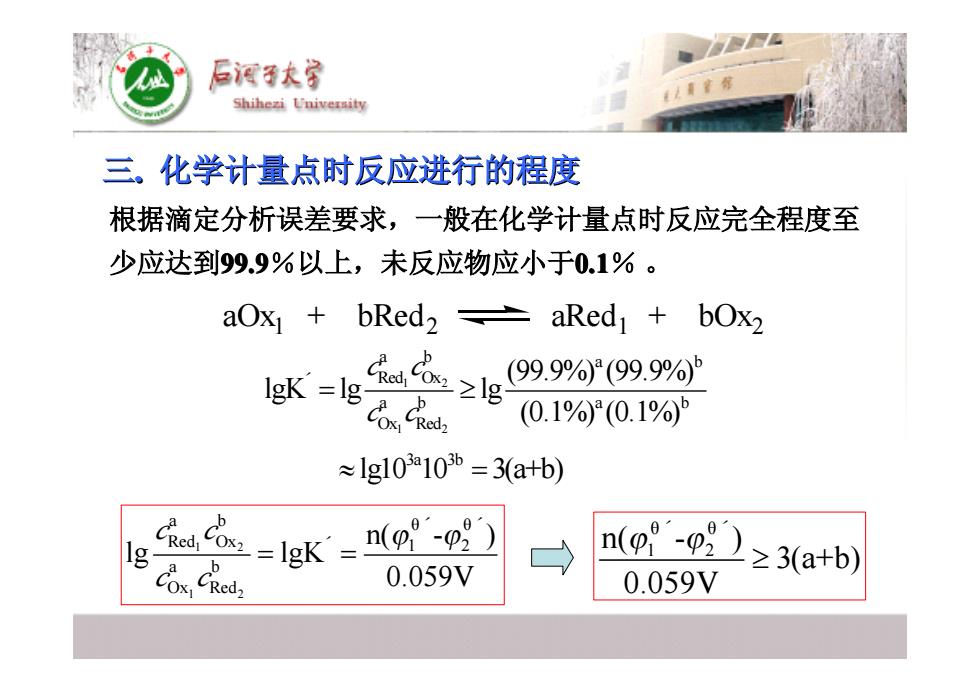
三. 化学计量点时反应进行的程度 化学计量点时反应进行的程度 根据滴定分析误差要求,一般在化学计量点时反应完全程度至 根据滴定分析误差要求,一般在化学计量点时反应完全程度至 少应达到99.9%以上,未反应物应小于 %以上,未反应物应小于0.1% 。 1 2 1 2 a b a b Red Ox a b a b Ox Red 3a 3b (99.9%) (99.9%) lgK lg lg (0.1%) (0.1%) lg10 10 3(a+b) c c c c = ≥ ≈ = ˊ aOx1 + bRed2 aRed1 + bOx2 θ θ 1 2 n( - ) 3(a+b) 0.059V ϕ ϕ ≥ ˊ ˊ 1 2 1 2 a b θ θ Red Ox 1 2 a b Ox Red n( - ) lg lgK 0.059V c c c c ϕ ϕ = = ˊ ˊ ˊ

后酒子大 Shihezi University aOx+bRed2± aRed+bOx2 n(p-p)≥3(a+b) 0.059V 讨论: 1)%=属=1,则=b-1,=1,gF≥6,△中0"≥0.35V 2)m12,%=1,则=1,b-2,-2,g≥9,△中0≥0.27V 3)属=属=2,则需=b-1,-2,g≥6,△中9≥018V
讨论: 1)n11=n22=1,则a=b=1,n=1, lg K′ ≥ 6,∆φθ′ θ′ ≥ 0.35 V 2)n11=2,n22=1,则a=1,b=2,n=2, lg K′ ≥ 9,∆φθ′ θ′ ≥ 0.27 V 3)n11=n22=2,则a=b=1,n=2,lg K′ ≥ 6,∆φθ′ θ′ ≥ 0.18 V θ θ 1 2 n( - ) 3(a+b) 0.059V ϕ ϕ ≥ ˊ ˊ aOx1 + bRed2 aRed1 + bOx2

后酒子大学 Shihezi University 例:若两个电对在反应中转移的电子数分别为2和3,为使反应 完全程度达9.9%,则两电对的条件电极电位差值至少为() A、0.12V B、0.15V C、0.27V D、0.72V B n() 3(a+b) 0.059V 计算表明,无论什么类型的氧化还原反应,若仅考虑反应的完 全程度,一般认为△中·≥0.36V就能满足滴定分析的要求。 P225例7-8
计算表明,无论什么类型的氧化还原反应,若仅考虑反应的完 计算表明,无论什么类型的氧化还原反应,若仅考虑反应的完 全程度,一般认为 全程度,一般认为△φӨӨˊ≥0.36V就能满足滴定分析的要求。 就能满足滴定分析的要求。 P225 例7-8 例:若两个电对在反应中转移的电子数分别为 例:若两个电对在反应中转移的电子数分别为2和3,为使反应 完全程度达99.9%,则两电对的条件电极电位差值至少为 ,则两电对的条件电极电位差值至少为( ) ( ) ( ) ( ) ( ) ( ) ( ) ( ) A、0.12V B 0.12V B 0.12V B 0.12V B 0.12V B 0.12V B 0.12V B 0.12V B、0.15V C 0.15V C 0.15V C 0.15V C 0.15V C 0.15V C 0.15V C 0.15V C、0.27 V D 0.27 V D 0.27 V D 0.27 V D 0.27 V D 0.27 V D 0.27 V D 0.27 V D、0.72V B θ θ 1 2 n( - ) 3(a+b) 0.059V ϕ ϕ ≥ ˊ ˊ