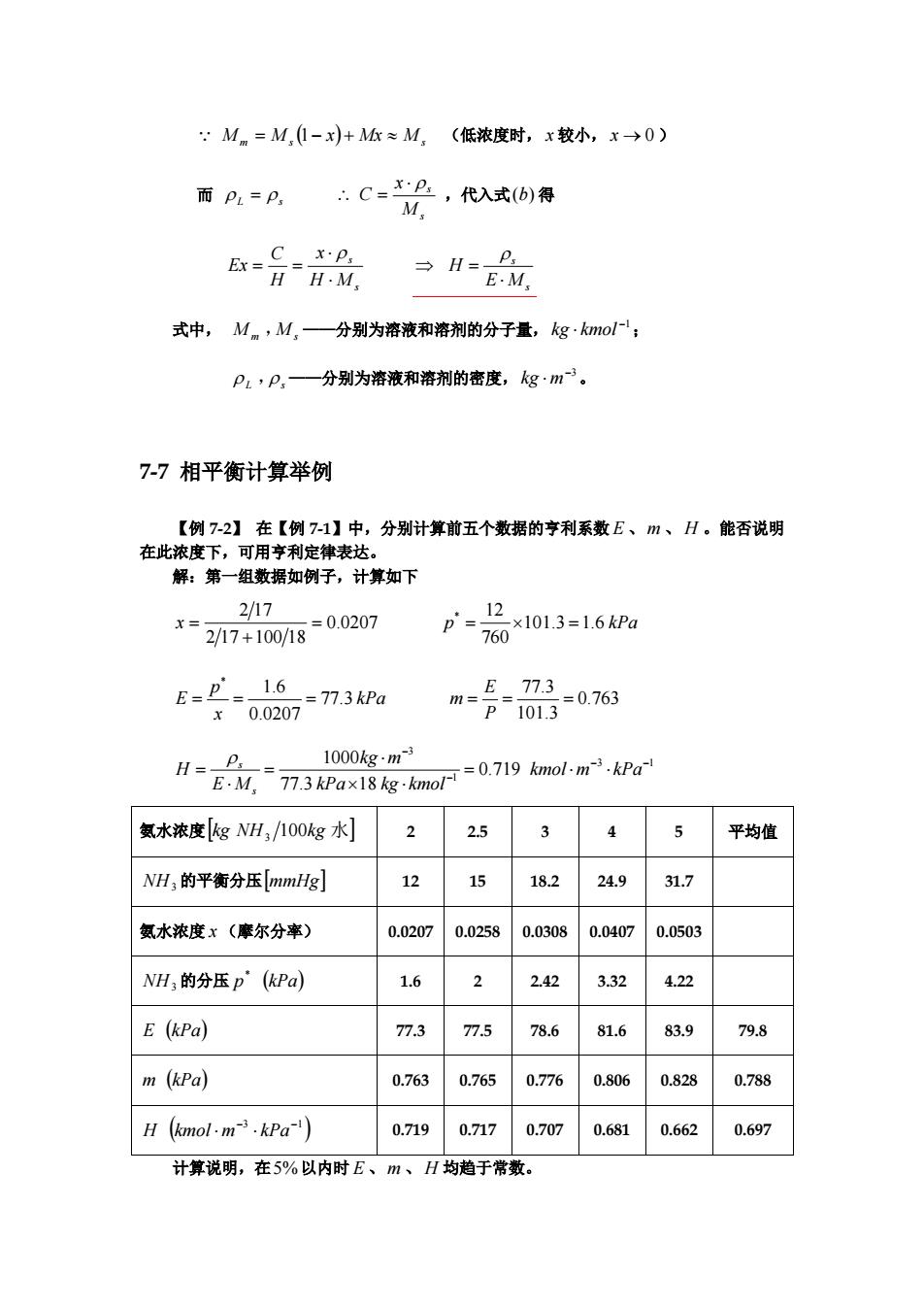
Q M m = M s ( ) 1− x + Mx ≈ M s (低浓度时, x 较小, x → 0 ) 而 ρ L = ρ s s s M x C ⋅ ρ ∴ = ,代入式(b) 得 s s H M x H C Ex ⋅ ⋅ = = ρ s s E M H ⋅ = ρ ⇒ 式中, M m ,M s ——分别为溶液和溶剂的分子量, ;−1 kg ⋅ kmol ρ L ,ρ s ——分别为溶液和溶剂的密度, 。−3 kg ⋅ m 7-7 相平衡计算举例 【例 7-2】 在【例 7-1】中,分别计算前五个数据的亨利系数 、 m 、 。能否说明 在此浓度下,可用亨利定律表达。 E H 解:第一组数据如例子,计算如下 0.0207 2 17 100 18 2 17 = + x = p 101.3 1.6 kPa 760 * 12 = × = kPa x p E 77.3 0.0207 1.6 * = = = 0.763 101.3 77.3 = = = P E m 3 1 1 3 0.719 77.3 18 1000 − − − − = ⋅ ⋅ × ⋅ ⋅ = ⋅ = kmol m kPa kPa kg kmol kg m E M H s ρ s 氨水浓度[kg NH 100kg 水] 3 2 2.5 3 4 5 平均值 NH3 的平衡分压[ ] mmHg 12 15 18.2 24.9 31.7 氨水浓度 x (摩尔分率) 0.0207 0.0258 0.0308 0.0407 0.0503 NH3 的分压 p ( ) kPa * 1.6 2 2.42 3.32 4.22 E ( ) kPa 77.3 77.5 78.6 81.6 83.9 79.8 m ( ) kPa 0.763 0.765 0.776 0.806 0.828 0.788 ( ) −3 −1 H kmol ⋅ m ⋅ kPa 0.719 0.717 0.707 0.681 0.662 0.697 计算说明,在5%以内时 E 、 m 、 H 均趋于常数
Q M m = M s ( ) 1− x + Mx ≈ M s (低浓度时, x 较小, x → 0 ) 而 ρ L = ρ s s s M x C ⋅ ρ ∴ = ,代入式(b) 得 s s H M x H C Ex ⋅ ⋅ = = ρ s s E M H ⋅ = ρ ⇒ 式中, M m ,M s ——分别为溶液和溶剂的分子量, ;−1 kg ⋅ kmol ρ L ,ρ s ——分别为溶液和溶剂的密度, 。−3 kg ⋅ m 7-7 相平衡计算举例 【例 7-2】 在【例 7-1】中,分别计算前五个数据的亨利系数 、 m 、 。能否说明 在此浓度下,可用亨利定律表达。 E H 解:第一组数据如例子,计算如下 0.0207 2 17 100 18 2 17 = + x = p 101.3 1.6 kPa 760 * 12 = × = kPa x p E 77.3 0.0207 1.6 * = = = 0.763 101.3 77.3 = = = P E m 3 1 1 3 0.719 77.3 18 1000 − − − − = ⋅ ⋅ × ⋅ ⋅ = ⋅ = kmol m kPa kPa kg kmol kg m E M H s ρ s 氨水浓度[kg NH 100kg 水] 3 2 2.5 3 4 5 平均值 NH3 的平衡分压[ ] mmHg 12 15 18.2 24.9 31.7 氨水浓度 x (摩尔分率) 0.0207 0.0258 0.0308 0.0407 0.0503 NH3 的分压 p ( ) kPa * 1.6 2 2.42 3.32 4.22 E ( ) kPa 77.3 77.5 78.6 81.6 83.9 79.8 m ( ) kPa 0.763 0.765 0.776 0.806 0.828 0.788 ( ) −3 −1 H kmol ⋅ m ⋅ kPa 0.719 0.717 0.707 0.681 0.662 0.697 计算说明,在5%以内时 E 、 m 、 H 均趋于常数

§3 传质系数与速率方程 7-8 分子扩散与费克定律 (1)分子扩散——流体内某一组分存在浓度差时,则由于分子运动使组分从浓度高处传 递至浓度低处,这种现象称为分子扩散。 (2)费克定律——单位时间通过单位面积物质的扩散量与浓度梯度成正比。 dZ dC J A A ∝ , 写成等式: dZ dC J D A A = − AB 式中, J A ——质量通量 −2 −1 kmol ⋅ m ⋅s dZ dCA ——浓度梯度 4 3 − m ⇒ kmol ⋅ m m kmol DAB —— A 在 B 中的扩散系数 2 −1 m ⋅s 对于气体扩散: = = − = = RT p V n C dZ dC N J D A A A A A A Q dZ dp RT D N A ∴ A = − ∫ ∫ = − i A p p A Z A dp RT D N dZ 0 ( ) A A i p p RT D ⇒ N ⋅ Z = − ( ) A A i p p RTZ D ∴ N = − , Gk RTZ D 令 = —— kG 称为传质系数 ( ) A G A i ∴ N = k p − p 同理,对于液相扩散有: ( ) , A L Ci CA N = k − = Z D k L (3)单相传质的滞流“膜模型
§3 传质系数与速率方程 7-8 分子扩散与费克定律 (1)分子扩散——流体内某一组分存在浓度差时,则由于分子运动使组分从浓度高处传 递至浓度低处,这种现象称为分子扩散。 (2)费克定律——单位时间通过单位面积物质的扩散量与浓度梯度成正比。 dZ dC J A A ∝ , 写成等式: dZ dC J D A A = − AB 式中, J A ——质量通量 −2 −1 kmol ⋅ m ⋅s dZ dCA ——浓度梯度 4 3 − m ⇒ kmol ⋅ m m kmol DAB —— A 在 B 中的扩散系数 2 −1 m ⋅s 对于气体扩散: = = − = = RT p V n C dZ dC N J D A A A A A A Q dZ dp RT D N A ∴ A = − ∫ ∫ = − i A p p A Z A dp RT D N dZ 0 ( ) A A i p p RT D ⇒ N ⋅ Z = − ( ) A A i p p RTZ D ∴ N = − , Gk RTZ D 令 = —— kG 称为传质系数 ( ) A G A i ∴ N = k p − p 同理,对于液相扩散有: ( ) , A L Ci CA N = k − = Z D k L (3)单相传质的滞流“膜模型

图 7-7 单相传质示意图 如图 7-7 所示,萘片的扩散传质,即气相传质,可写成: ( ) G A A A G A A k p p N k p p 1 1 2 1 2 − = − = (传质阻力) (传质推动力) 液相传质可写成: ( ) L A A A L A A k C C N k C C 1 1 2 1 2 − = − = 7-9 两相间传质的“双膜”模型 为了解决多相传质问题,路易斯—惠特曼(Lewis-Whitman)将固体溶解理论引入传 质过程,二十年代提出了双膜模型,其要点如下。 1.两相间有物质传递时,相界面两侧各有一层极薄的静止膜,传递阻力都集中在这里。 这实际上是继承了“滞流膜”模型的观点。例如气—液相间的传质,如图 7-8 所示,气相侧 和液相侧的传质通量分别为: ( ) G A i AG G A i k p p N k p p 1 − = − = .(a) ( ) L i A AL L i A k C C N k C C 1 − = − = .(b) 式中, kG ——以分压差为推动力表示的气相传质分系数, ; −1 −2 −1 kmol ⋅s ⋅ m ⋅ kPa L k ——以浓度差为推动力表示的液相传质分系数, ;−1 m ⋅s A i p 、p ——分别为气相湍流主体和气—液界面上的溶质气体分压, kPa ; CA 、Ci ——分别为液相湍流主体和气—液界面上溶质的液相浓度, 。−3 kmol ⋅ m
图 7-7 单相传质示意图 如图 7-7 所示,萘片的扩散传质,即气相传质,可写成: ( ) G A A A G A A k p p N k p p 1 1 2 1 2 − = − = (传质阻力) (传质推动力) 液相传质可写成: ( ) L A A A L A A k C C N k C C 1 1 2 1 2 − = − = 7-9 两相间传质的“双膜”模型 为了解决多相传质问题,路易斯—惠特曼(Lewis-Whitman)将固体溶解理论引入传 质过程,二十年代提出了双膜模型,其要点如下。 1.两相间有物质传递时,相界面两侧各有一层极薄的静止膜,传递阻力都集中在这里。 这实际上是继承了“滞流膜”模型的观点。例如气—液相间的传质,如图 7-8 所示,气相侧 和液相侧的传质通量分别为: ( ) G A i AG G A i k p p N k p p 1 − = − = .(a) ( ) L i A AL L i A k C C N k C C 1 − = − = .(b) 式中, kG ——以分压差为推动力表示的气相传质分系数, ; −1 −2 −1 kmol ⋅s ⋅ m ⋅ kPa L k ——以浓度差为推动力表示的液相传质分系数, ;−1 m ⋅s A i p 、p ——分别为气相湍流主体和气—液界面上的溶质气体分压, kPa ; CA 、Ci ——分别为液相湍流主体和气—液界面上溶质的液相浓度, 。−3 kmol ⋅ m