
第二类导体又称离子导体,如电解质溶液、熔融电解质等第二类导体的特点是:A.正、负离子作反向移动而导电B.导电过程中有化学反应发生C.温度升高,电阻下降,导电能力增强D.导电总量分别由正、负离子分担等,也属于离子固体电解质,如AgBr、Pbl,导体,1但它导电的机理比较复杂,导电能力不高本章以讨论电解质水溶液为主
第二类导体又称离子导体,如电解质溶液、熔 融电解质等 第二类导体的特点是: A. 正、负离子作反向移动而导电 B. 导电过程中有化学反应发生 C. 温度升高,电阻下降,导电能力增强 D. 导电总量分别由正、负离子分担 *固体电解质,如 等,也属于离子 导体,但它导电的机理比较复杂,导电能力不高, 本章以讨论电解质水溶液为主。 AgBr PbI 、 2

正极、负极、电势高的极称为正极,电流从正极正极:流向负极。电势低的极称为负极,电子从负极负极:流向正极
正极、负极、 电势低的极称为负极,电子从负极 流向正极。 负极: 电势高的极称为正极,电流从正极 流向负极。 正极:

阴极、阳极发生还原作用的极称为阴极阴极:在原电池中,阴极是正极;在(Cathode)电解池中,阴极是负极。发生氧化作用的极称为阳极阳极:在原电池中,阳极是负极;在(Anode)电解池中,阳极是正极
阴极、阳极 阴极: 发生还原作用的极称为阴极。 (Cathode) 阳极: 发生氧化作用的极称为阳极。 (Anode) 在原电池中,阴极是正极;在 电解池中,阴极是负极。 在原电池中,阳极是负极;在 电解池中,阳极是正极
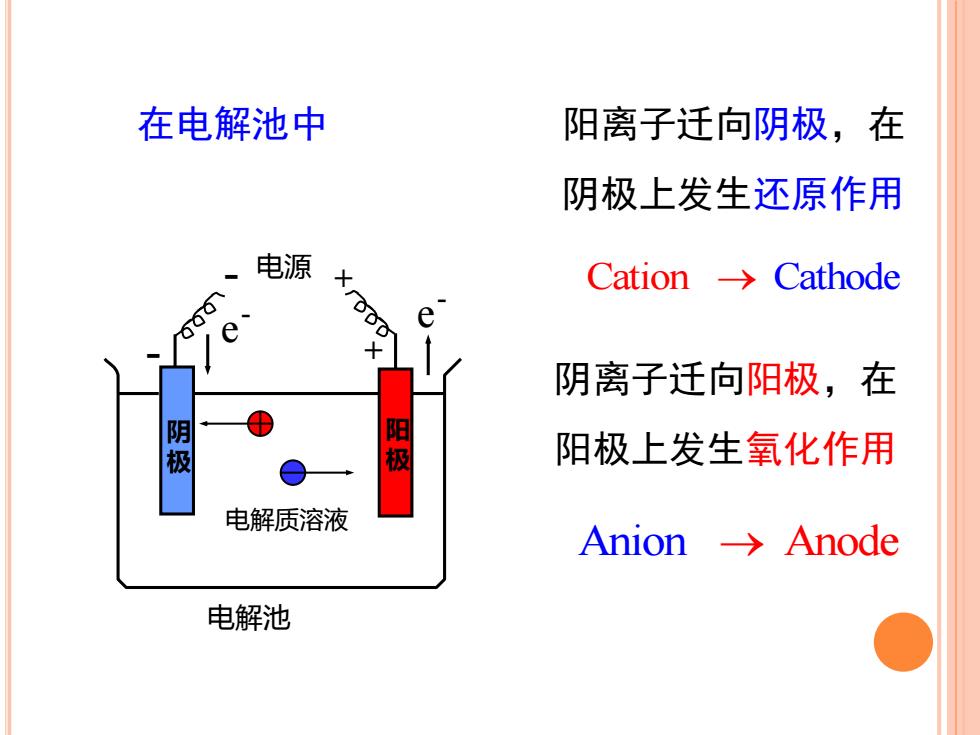
在电解池中阳离子迁向阴极,在阴极上发生还原作用电源Cation → Cathode+100eQe阴离子迁向阳极,在阳极阴极阳极上发生氧化作用电解质溶液Anion→> Anode电解池
电解质溶液 阳离子迁向阴极,在 阴极上发生还原作用 Anion → Anode - 电源 + 电解池 + 阳 极 - e - e - 阴 极 Cation → Cathode 阴离子迁向阳极,在 阳极上发生氧化作用 在电解池中
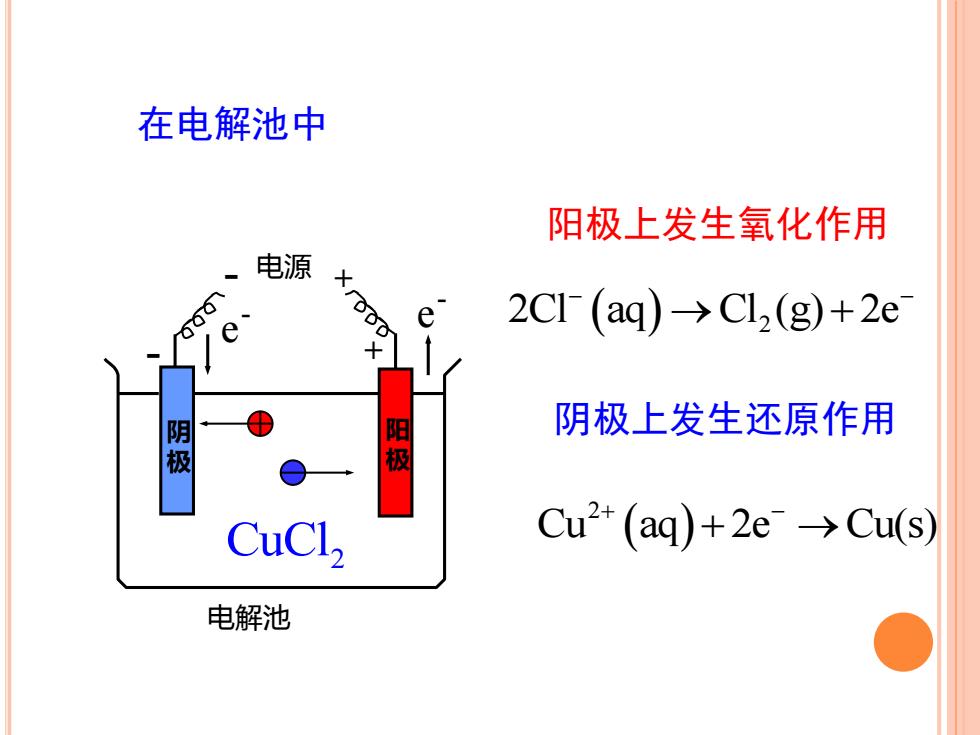
在电解池中阳极上发生氧化作用电源+10072CI- (aq) →Cl2(g)+2eee阴极上发生还原作用阳极阴极Cu2+ (aq)+2e- →Cu(s)CuCl,电解池
阳极上发生氧化作用 阴极上发生还原作用 在电解池中 - 电源 + 电解池 + 阳 极 - e - e - 阴 极 CuCl2 2Cl aq Cl (g) 2e ( ) 2 − − → + ( ) 2 Cu aq 2e Cu(s) + − + →