。确定孤对电子数和分子空间构型 LP=0分子的空间构型=电子对的空间构型 Example B BeH2 VP=22+2)-2 H-Be-H LP=0 :F BF3 VP-2333 LP=0 CH VP- (4+4)=4 LP=0 HT H PC1s VP= (5+5)=5 P=0 人个水水 SF6 26+6)=6 LP=0 SF. 6 上页下页 节首 节尾
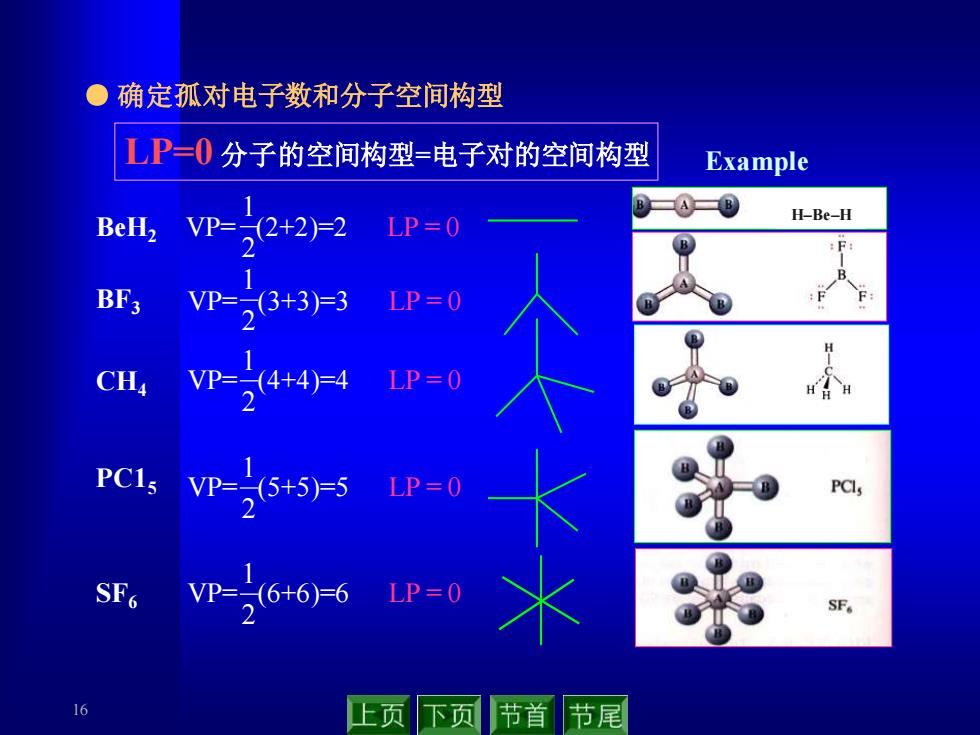
16 ● 确定孤对电子数和分子空间构型 LP=0 分子的空间构型=电子对的空间构型 BeH2 BF3 CH4 PC15 SF6 VP= (2+2)=2 LP = 0 2 1 VP= (3+3)=3 LP = 0 2 1 VP= (4+4)=4 LP = 0 2 1 VP= (5+5)=5 LP = 0 2 1 VP= (6+6)=6 LP = 0 2 1 Example H–Be–H
LP≠O分子的空间构型≠电子对的空间构型使价层电子对斥力最小 Total Electron-pair Bonding Nonbonding Molecular electron pairs geometry pairs pairs geometry Example 2 2 0 ®® 0=c=0 Linear Linear 3 Trigonal planar Trigonal plana oo 上页下页节首节尾
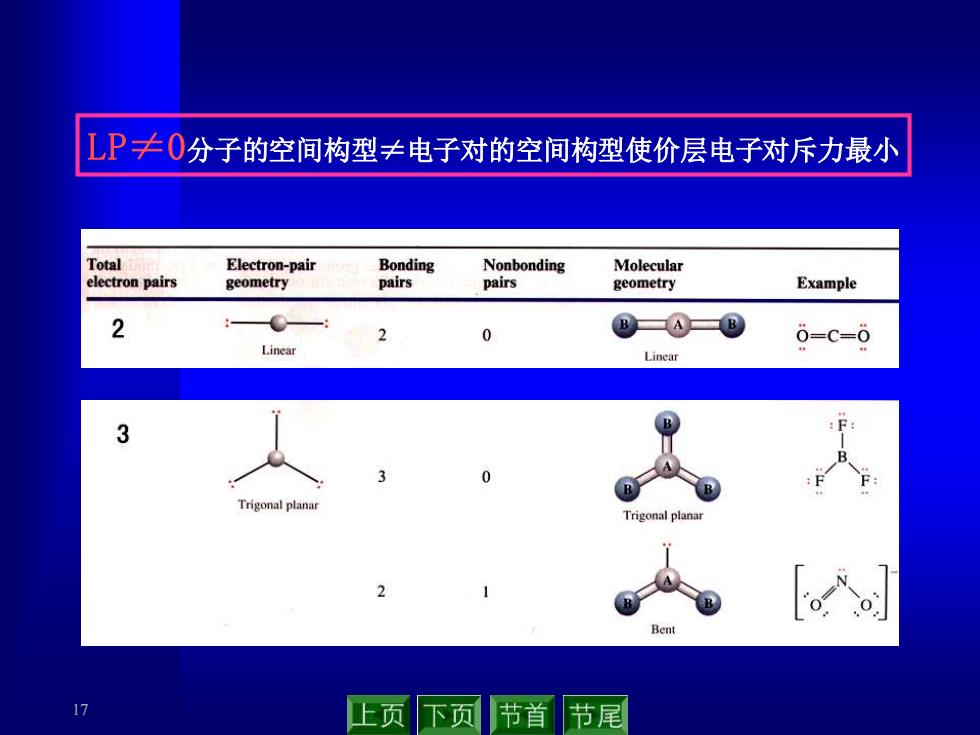
17 LP≠0分子的空间构型≠电子对的空间构型使价层电子对斥力最小

Total Electron-pair Bonding Nonbonding Molecular electron pairs geometry pairs pairs geometry Example 4 0 H H Tetrahedral Tetrahedral 3 H AH Trigonal pyramidal Bent 18 上页下页节首节尾
18
Total Electron-pair Bonding Nonbonding Molecular electron pairs geometry pairs pairs geometry Example 5 PCls Trigonal bipyramidal Trigonal bipyramida Seesaw 孤对电子优先代替平 伏位置上的原子和相关 CIF, 键对电子 T-shaped 19 上下页节首节尾
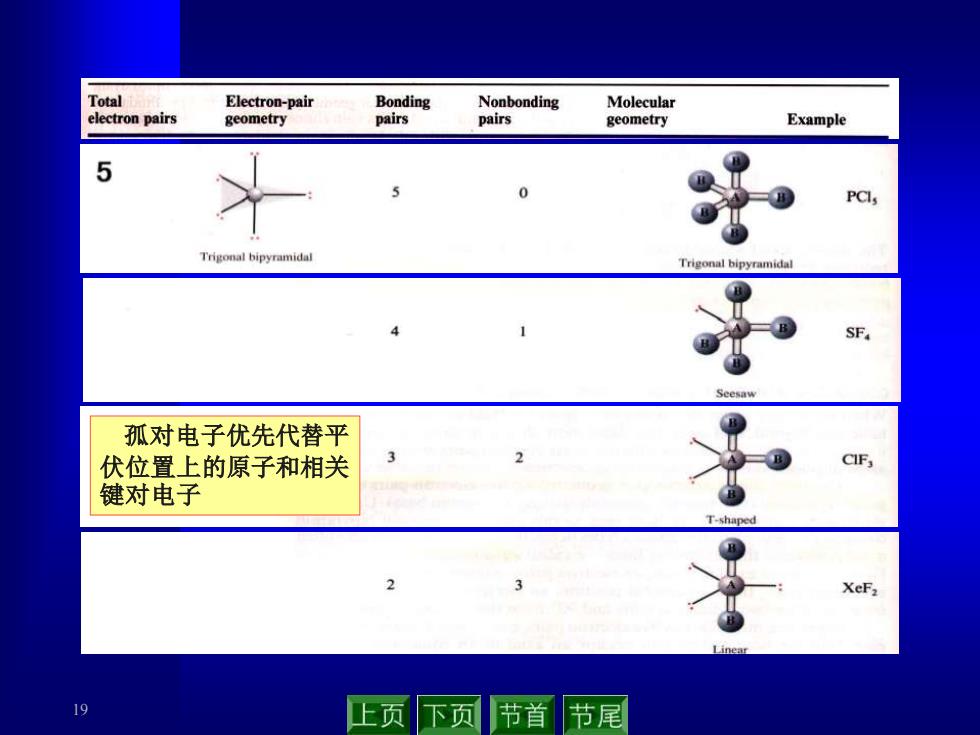
19 孤对电子优先代替平 伏位置上的原子和相关 键对电子
Total Electron-pair Bonding Nonbonding Molecular electron pairs geometry pairs pairs geometry Example 6 SF& Octahedral Octahedral 第二对孤对电子 优先代替第一对孤 BrFs 对电子反位的原子 和相关键对电子 Square pyramidal XeF, Square planar 20 上页下页节首节尾
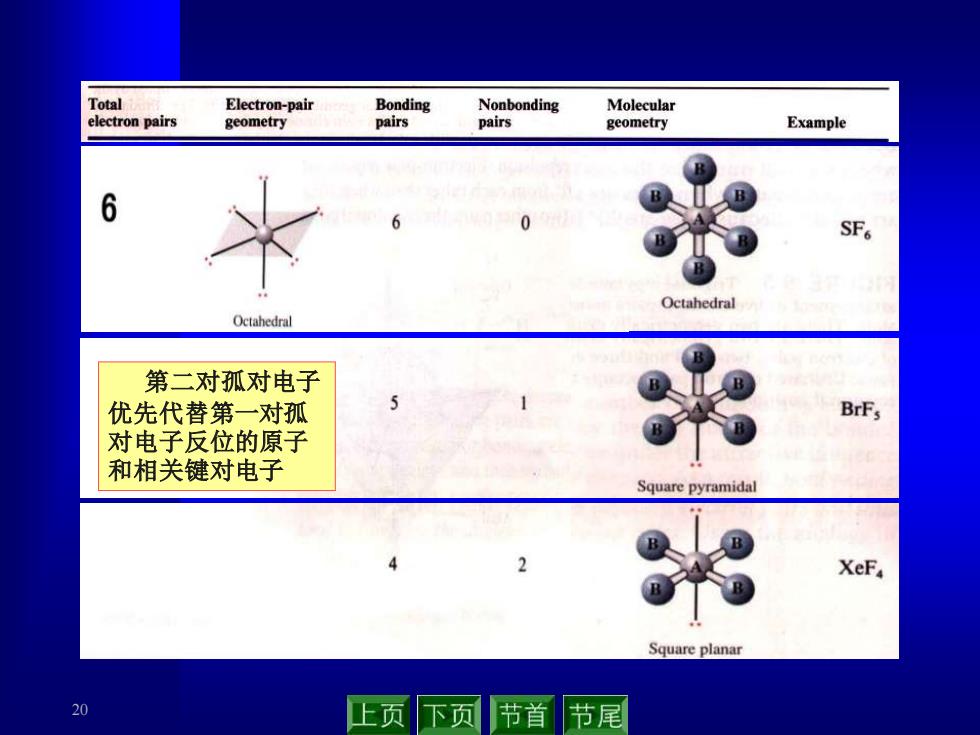
20 第二对孤对电子 优先代替第一对孤 对电子反位的原子 和相关键对电子