
2.1.2已明确了的化学键类型 〔离子配 键 电价键一离子键 电价配键 离子偶极配键 配键 电子对键 极性键. 共价配键 (单、双、叁键) 非极性键 双原子 化 共价键 单电子键 三电子键 共价键 多原子 共轭π键 .4 共价键 多中心键 . 金属键 6 上页下页 节首节尾
6 化 学 键 共价键 金属键 离 子 配 键 离子偶极配键 离子键 电价配键 配键 双原子 共价键 多原子 共价键 电子对键 (单、双、叁键) 单电子键 三电子键 共轭 π 键 多中心键 极 性 键 共价配键 非极性键 2.1.2 已明确了的化学键类型 电价键

2.2共价键的概念与路易斯结构式 (covalent bond theory 2.2,1共价键的相关概念 Lewis G.N.在1916年假定化学键所涉及的每 对电子处于两个相邻原子之间为其共享,用八一B表示 双键和叁键相应于两对或三对共享电子.分子的稳定性是因为共享电 子对服从“八隅律”(octet rule), single covalent bond 共享电子对 共价键 double covalent bond 记住有关术语和概念】 triple covalent bond The bond polarity in the hydrogen halide 配位共价键coordination covalent bond Chemical H-I H-Br H-CI H-F 极性共价键polar covalent bond bond 非极性共价键non polar covalent bond Electronicgrativ ity 0.46 0.76 0.96 1.78 电正性原子electropositive atom diffe re nce Bonding polarity Increasing in turn 电负性原子electronegative atom 节尾
7 2.2.1 共价键的相关概念 2.2 共价键的概念与路易斯结构式 (covalent bond theory ) Lewis G. N. 在1916年假定化学键所涉及的每一 对电子处于两个相邻原子之间为其共享,用A—B表示 .双键和叁键相应于两对或三对共享电子. 分子的稳定性是因为共享电 子对服从“八隅律”(octet rule). 配位共价键coordination covalent bond 非极性共价键non polar covalent bond 极性共价键polar covalent bond 电负性原子electronegative atom 电正性原子electropositive atom 共享电子对——共价键 single covalent bond double covalent bond triple covalent bond The bond polarity in the hydrogen halide Chemical bond H – I H – Br H – Cl H – F Electronicgrativity 0.46 0.76 0.96 1.78 difference Bonding polarity Increasing in turn 记住有关术语和概念!

22.2路易斯结构式 路易斯用元素符号之间的小黑点表示分子中各原子的键合关 系,代表一对键电子的一对小黑点亦可用“一”代替。路易斯结 构式能够简洁地表达单质和化合物的成键状况,其基本书写步骤 空下微原子的键合关系写出元奏符井将相郎原子用单键连接在 大多数情况下,原子间的键合关系是已知的,例如,NO,中的 键合关系不是N一OO,而是O一N一O.有时还可作出某些有 根据的猜测。 2.将各原子的价电子数相加,算出可供利用的价电子总数.如果 被表达的物种带有正电荷,价电子总数应减去正电荷数:如果 被表达的物种带有负电荷,价电子总数应加上负电荷数, 3.扣除与共价单键相应的电子数(单键数×2)后,将剩余的价电 子分配给每个原子,使其占有适当数目的非键合电子。对第2 周期元素而言,非键合电子数与键合电子数之和往往能使每 个原子满足八隅律· 4.如果剩余的电子不够安排,可将一些单键改为双键或叁键 上页下页 节首 节尾
8 2.2.2 路易斯结构式 路易斯用元素符号之间的小黑点表示分子中各原子的键合关 系,代表一对键电子的一对小黑点亦可用“-”代替。路易斯结 构式能够简洁地表达单质和化合物的成键状况,其基本书写步骤 如下: 1. 按原子的键合关系写出元素符号并将相邻原子用单键连接. 在 大多数情况下,原子间的键合关系是已知的,例如, NO2中的 键合关系不是N—O—O,而是O—N—O.有时还可作出某些有 根据的猜测. 2. 将各原子的价电子数相加, 算出可供利用的价电子总数. 如果 被表达的物种带有正电荷, 价电子总数应减去正电荷数; 如果 被表达的物种带有负电荷, 价电子总数应加上负电荷数. 3. 扣除与共价单键相应的电子数(单键数×2)后,将剩余的价电 子分配给每个原子, 使其占有适当数目的非键合电子。对第2 周期元素而言, 非键合电子数与键合电子数之和往往能使每 个原子满足八隅律. 4. 如果剩余的电子不够安排,可将一些单键改为双键或叁键
Que 写出氯酸根离子CO3的路易斯结构式 C1原子的电负性小于0原子,意味着不存在O一O之间的键 合.合理的排布应该如下所示: C10离子中价电子总数等于26(四个原子的价电子数相加再加1), 扣除3个单键的6个电子,余下的20个电子以孤对方式分配给四个原 子,使它们均满足八隅律的要求 下页 节首 节尾
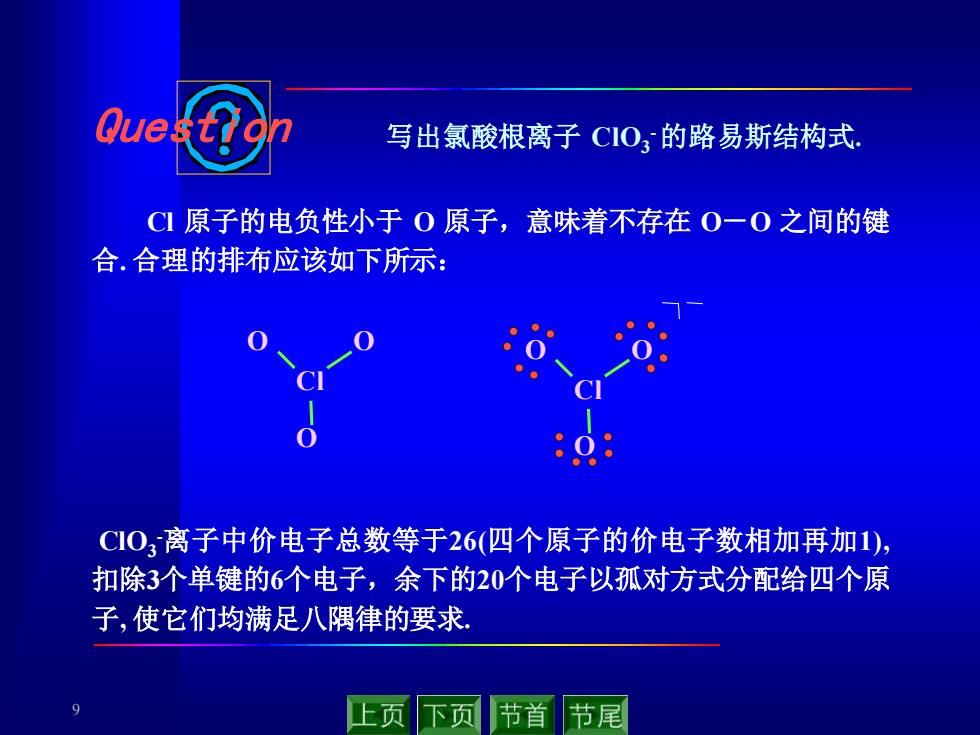
9 Question 写出氯酸根离子 ClO3 -的路易斯结构式. Cl 原子的电负性小于 O 原子,意味着不存在 O-O 之间的键 合. 合理的排布应该如下所示: ClO3 -离子中价电子总数等于26(四个原子的价电子数相加再加1), 扣除3个单键的6个电子,余下的20个电子以孤对方式分配给四个原 子, 使它们均满足八隅律的要求. Cl O O O Cl O O O

Que 写出NO离子的路易斯结构式 NO+离子只可能有一种排布方式,见下图最左边一个: N-O N汉* :+N+ N≡O:7 NO离子中价电子总数等于10(两个原子的价电子数相加后减 1),扣除1个单键的2个电子,余下的8个电子无论按上图中第 二个那样以孤对方式分配给两个原子,还是按上图中第三或第四 个那样将N一O单键改为双键,都不能使两个原子同时满足八隅 律的要求.这一要求只有将单键改为叁键才能满足, 10 上页 下页 节首 节尾
10 Question 写出 NO+ 离子的路易斯结构式. NO+ 离子只可能有一种排布方式,见下图最左边一个: NO+ 离子中价电子总数等于10 (两个原子的价电子数相加后减 1),扣除 1 个单键的 2 个电子, 余下的 8 个电子无论按上图中第 二个那样以孤对方式分配给两个原子,还是按上图中第三或第四 个那样将 N-O 单 键改为双键,都不能使两个原子同时满足八隅 律的要求. 这一要求只有将单键改为叁键才能满足. N O N O + + N O + N O + N O