第一节配合物的组成、命名和异构现象 些金属离子的配位数 配位数 金属离子 实例 2 Ag、Cut、Au [AgNH3)2]H、 [Cu(CN)2] 4 Cu2+、Zn2+、Cd2+、Hg2+、A13+、[Hgl4]2-、 Sn2+、Pb2+、Co2+、Ni2+、Pt2+、[Zn(CN)4]2-、 Fe3+、Fe2+ [Pt(NH)2CI2] 6 Cr3+、AI3+、Pt4+、Fe3+、Fe2+、 [PtCl6]2、 Co3+、Co2+、Ni2+、Pb4+ [Cr(NH3)4C2]、 [Fe(CN)6]3-、 [NiNH3)6]2+、 [Co(NH)(HO)CL]
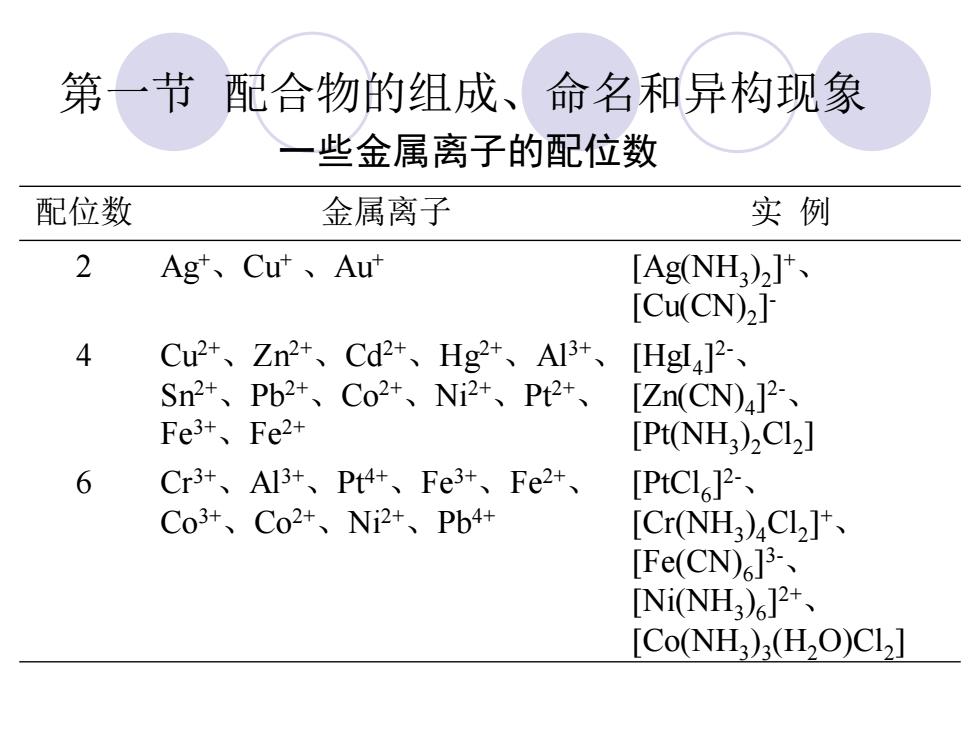
第一节 配合物的组成、命名和异构现象 一些金属离子的配位数 配位数 金属离子 实 例 2 Ag+ 、Cu+ 、Au+ [Ag(NH3 ) 2 ] + 、 [Cu(CN)2 ] - 4 Cu2+ 、Zn2+ 、Cd2+ 、Hg2+ 、Al3+ 、 Sn2+ 、Pb2+ 、Co2+ 、Ni2+ 、Pt2+ 、 Fe3+ 、Fe2+ [HgI4 ] 2-、 [Zn(CN)4 ] 2-、 [Pt(NH3 ) 2Cl2 ] 6 Cr3+ 、Al3+ 、Pt4+ 、Fe3+ 、Fe2+ 、 Co3+ 、Co2+ 、Ni2+ 、Pb4+ [PtCl6 ] 2-、 [Cr(NH3 ) 4Cl2 ] + 、 [Fe(CN)6 ] 3-、 [Ni(NH3 ) 6 ] 2+ 、 [Co(NH3 ) 3 (H2O)Cl2 ]

第一节配合物的组成、命名和异构现象 5.配离子的电荷 配离子的电荷数等于中心原子和配体总电荷的 代数和: 例1. [CuNH3)4]2+ 配离子电荷数=1×(+2)+4×0=+2。 例2.Hgl4]2 配离子的电荷数=1×(+2)十4×(-1)=-2。 外层离子的电荷总数和配离子的电荷总数相等, 而符号相反,所以由外层离子的电荷可以推断 出配离子的电荷及中心原子的氧化值
第一节 配合物的组成、命名和异构现象 5. 配离子的电荷 • 配离子的电荷数等于中心原子和配体总电荷的 代数和: 例1. [Cu(NH3 )4 ] 2+ 配离子电荷数=1×(+2)+4×0=+2。 例2. [HgI4 ] 2- 配离子的电荷数=1×(+2)+4×(-1)=-2。 ⚫ 外层离子的电荷总数和配离子的电荷总数相等, 而符号相反,所以由外层离子的电荷可以推断 出配离子的电荷及中心原子的氧化值

第一节配合物的组成、命名和异构现象 二、配合物的命名 1. 配位化合物的命名:阴离子在前、阳离子在后 配阳离子: “某化某”、“氢氧化某”、 “某酸某” [Fe(en)3]Cl3、[AgNH3)2]OH、[CuNH3)4]SO4 配阴离子: “某酸”、“某酸某” H2[PtCl]NH4[Co(NH2)4NH3)2]
第一节 配合物的组成、命名和异构现象 二、配合物的命名 1. 配位化合物的命名:阴离子在前、阳离子在后 • 配阳离子: “某化某”、 “氢氧化某”、“某酸某” [Fe(en)3 ]Cl3、[Ag(NH3 )2 ]OH、[Cu(NH3 )4 ]SO4 • 配阴离子: “某酸”、 “某酸某” H2 [PtCl6 ]、NH4 [Co(NH2 )4 (NH3 )2 ]

第一节配合物的组成、命名和异构现象 2.配离子及配位分子的命名: 配体数-配体名称“合”中心原子名称(氧化值) 配体数目用二、三、四等数字表示 复杂的配体名称写在圆括号中,以免混淆 不同配体之间以中圆点“.”分开 配体数 配体名称合中心原子(氧化态值) 以二、 不同 以罗马数 三、四 配体 字Ⅱ、Ⅲ、 “。 表示 V表示 分开
第一节 配合物的组成、命名和异构现象 2. 配离子及配位分子的命名: 配体数-配体名称-“合”-中心原子名称(氧化值) • 配体数目用二、三、四等数字表示 • 复杂的配体名称写在圆括号中,以免混淆 • 不同配体之间以中圆点“·”分开 配体数 配体名称 合 中心原子(氧化态值) 以二、 三、四 表示 不同 配体 “•” 分开 以罗马数 字Ⅱ、Ⅲ、 Ⅳ表示

第一节配合物的组成、命名和异构现象 3. 配体命名顺序: ①先无机配体,后有机配体; ② 先离子,后分子; ③ 按配位原子元素符号字母序; ④ 配位原子相同,原子数目少的配体在前(先简单, 后复杂); 配位原子、配体原子数目相同,按配位原子连 接的原子的元素符号字母序; 配体化学式相同,按配位原子元素符号字母序
第一节 配合物的组成、命名和异构现象 3. 配体命名顺序: ① 先无机配体,后有机配体; ② 先离子,后分子; ③ 按配位原子元素符号字母序; ④ 配位原子相同,原子数目少的配体在前(先简单, 后复杂); ⑤ 配位原子、配体原子数目相同,按配位原子连 接的原子的元素符号字母序; ⑥ 配体化学式相同,按配位原子元素符号字母序