
第三章、 热力学第二定律 不可能把热从低 温物体传到高温 物体,而不引起 其它变化 The Second Law of Thermodynamics 1
1 第三章 热力学第二定律 不可能把热从低 温物体传到高温 物体,而不引起 其它变化

第三章 热力学第二定律 §3.1 自发变化的共同特征 §3.2 热力学第二定律 §3.3 Carnot定理 §3.4 熵的概念 §3.5 Clausius不等式与熵增加原理 §3.6 热力学基本方程与T-S图 §3.7 熵变的计算 §3.8 熵和能量退降 §3.9 热力学第二定律的本质和熵的统计意义 2
2 第三章 热力学第二定律 §3.1 自发变化的共同特征 §3.2 热力学第二定律 §3.3 Carnot定理 §3.4 熵的概念 §3.5 Clausius不等式与熵增加原理 §3.6 热力学基本方程与T-S图 §3.7 熵变的计算 §3.8 熵和能量退降 §3.9 热力学第二定律的本质和熵的统计意义

第三章 热力学第二定律 §3.10 Helmholtzi和Gibbs自由能 §3.11 变化的方向与平衡条件 §3.12 △G的计算示例 §3.13 几个热力学函数间的关系 §3.14 热力学第三定律及规定熵 *§3.15 绝对零度不能到达的原理 *§3.16 不可逆过程热力学简介 *§3.17 信息熵浅释 3
3 第三章 热力学第二定律 §3.10 Helmholtz和Gibbs自由能 §3.11 变化的方向与平衡条件 §3.13 几个热力学函数间的关系 §3.12 G 的计算示例 §3.14 热力学第三定律及规定熵 *§3.15 绝对零度不能到达的原理 *§3.16 不可逆过程热力学简介 *§3.17 信息熵浅释

§3.1 自发变化的共同特征—不可逆性 自发变化某种变化有自动发生的趋势,一旦发生就 无需借助外力,可自动进行,这种变化称为自发变化。 自发变化的共同特征一不可逆性任何自发变化的逆过 程是不能自动进行的,且为热方学不可逆过程。例如: (1)焦耳热功当量中功自动转变成热; (2)气体向真空膨胀; (3)热量从高温物体传入低温物体; (4)浓度不等的溶液混合均匀;(⑤)锌片与硫酸铜的置换反应等 它们的逆过程都不能自动进行。当借助外力,系统 恢复原状后,会给环境留下不可磨灭的影响。 4
4 §3.1 自发变化的共同特征——不可逆性 自发变化 某种变化有自动发生的趋势,一旦发生就 无需借助外力,可自动进行,这种变化称为自发变化。 自发变化的共同特征—不可逆性 任何自发变化的逆过 程是不能自动进行的,且为热力学不可逆过程。例如: (1)焦耳热功当量中功自动转变成热; (2)气体向真空膨胀; (3)热量从高温物体传入低温物体; (4)浓度不等的溶液混合均匀;(5)锌片与硫酸铜的置换反应等 它们的逆过程都不能自动进行。当借助外力,系统 恢复原状后,会给环境留下不可磨灭的影响
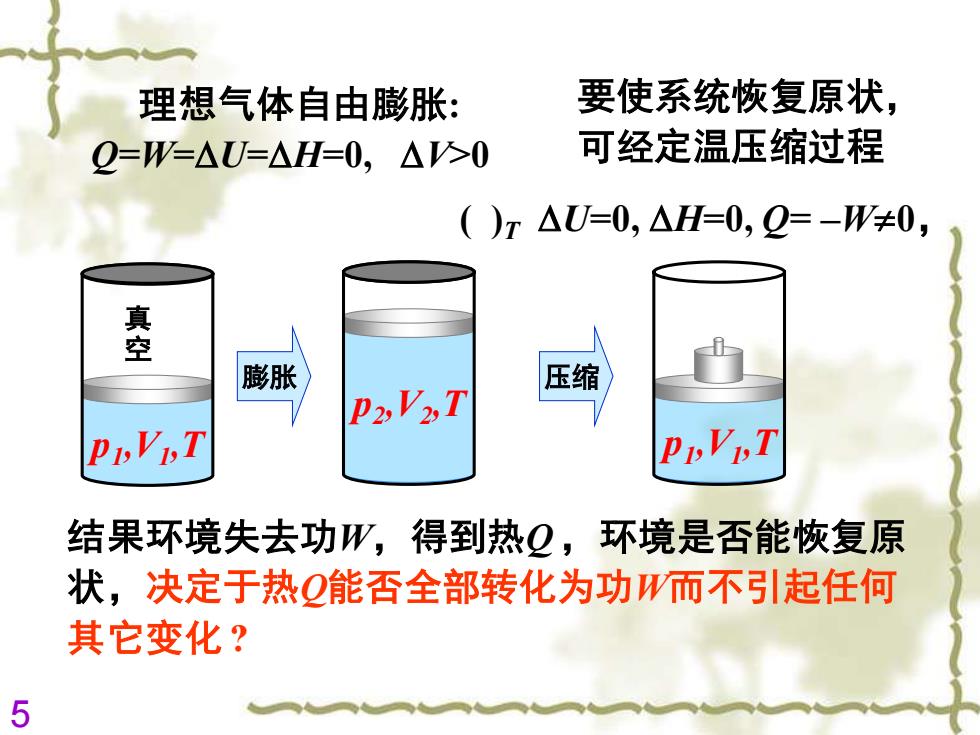
理想气体自由膨胀: 要使系统恢复原状, Q=W=△U=△H=0,△>0 可经定温压缩过程 ()T△U=0,△H=0,Q=-W≠0, 空 膨胀 压缩 P2V2T 结果环境失去功W,得到热Q,环境是否能恢复原 状,决定于热O能否全部转化为功W而不引起任何 其它变化? 5
5 理想气体自由膨胀: Q=W=U=H=0, V>0 结果环境失去功W,得到热Q ,环境是否能恢复原 状,决定于热Q能否全部转化为功W而不引起任何 其它变化 ? 要使系统恢复原状, 可经定温压缩过程 真 空 p1 ,V1 ,T p2 ,V2 ,T p1 ,V1 ,T ( )T U=0, H=0, Q= –W0, 膨胀 压缩