原子半径 Ba 镧系元素的原子半径随原 子序数的变化如左图所示。 一方面,镧系元素原子半径 从La的187.7pm到Lu的173.4 0A网 pm,共缩小了14.3pm,平均 每两个相邻元素之间缩小 14.3/14≈1pm。尽管平均相差 囡 只有1个pm,但其累积效应(共 14pm)是很显著的。 Hf. 另一方面,原子半径不是 5759616365676971 单调地减小,而是一条两峰一 原子序数 谷的曲线
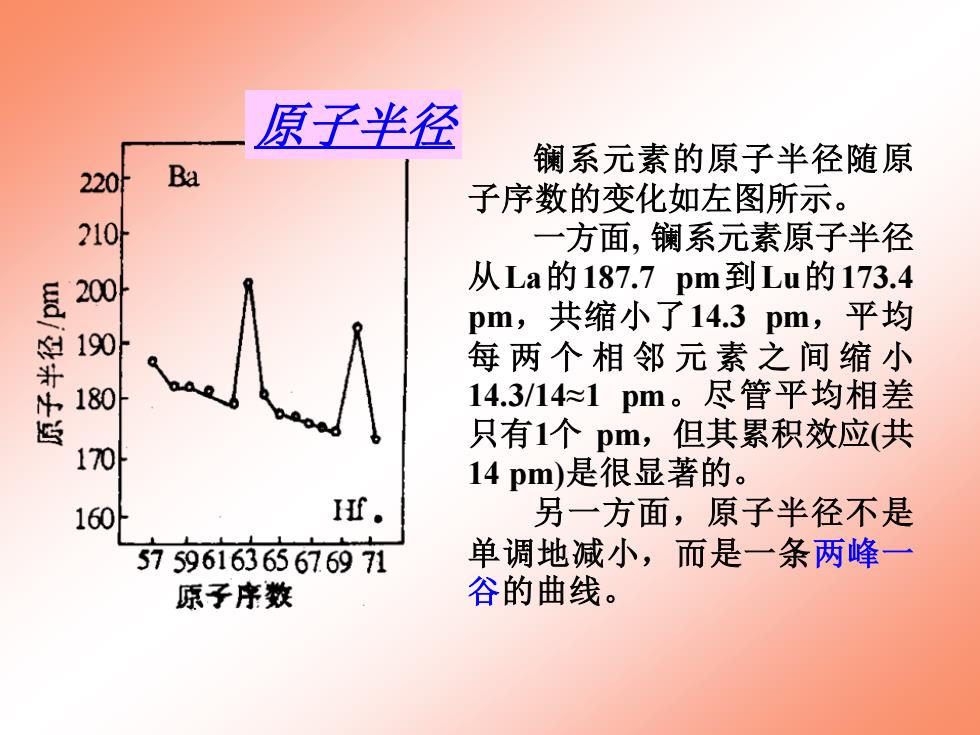
镧系元素的原子半径随原 子序数的变化如左图所示。 一方面, 镧系元素原子半径 从La的187.7 pm到Lu的173.4 pm,共缩小了14.3 pm,平均 每 两 个 相 邻 元 素 之 间 缩 小 14.3/14≈1 pm。尽管平均相差 只有1个 pm,但其累积效应(共 14 pm)是很显著的。 另一方面,原子半径不是 单调地减小,而是一条两峰一 谷的曲线。 原子半径
离子半径 110 Sm" 离子半径 镧系元素+3价离子从f0的La3+到f4的 L3+,依次增加4f电子(与原子的电子排布 且00 不一样),因而随着原子序数的增加离子的 Tm" 半径依次单调减小(没有峰谷现象),收缩的 程度比原子半径更大,由La3+的106.1pm到 90 Lu3+的84.8pm,共缩小了21.3pm,平均每 。Tb“ 两个相邻元素间缩小了21.3/141.5pm。 80 57剪6i6的6$67的7 离子半径的变化,在具有P的中点Gd3+钆处, 微有不连续性,这可由其相邻离子半径的差值的大小可以看出: Pm3+Sm3+ Eu3+Gd3+Tb3+Dy3+ rpm97.996.4 95.093.892.390.8 △(pm) 1.5 1.4 1.2 1.5 1.5 这是由于G3+具有半满稳定结构,屏蔽稍大,半径略有增大之故。 Y3+的半径为89.3pm,落在Ho3+和Er3+之间,故钇常与重稀 土共生,而Sc3+的半径为73.29pm,远小于镧系离子的半径,故 钪一般不和稀土共生
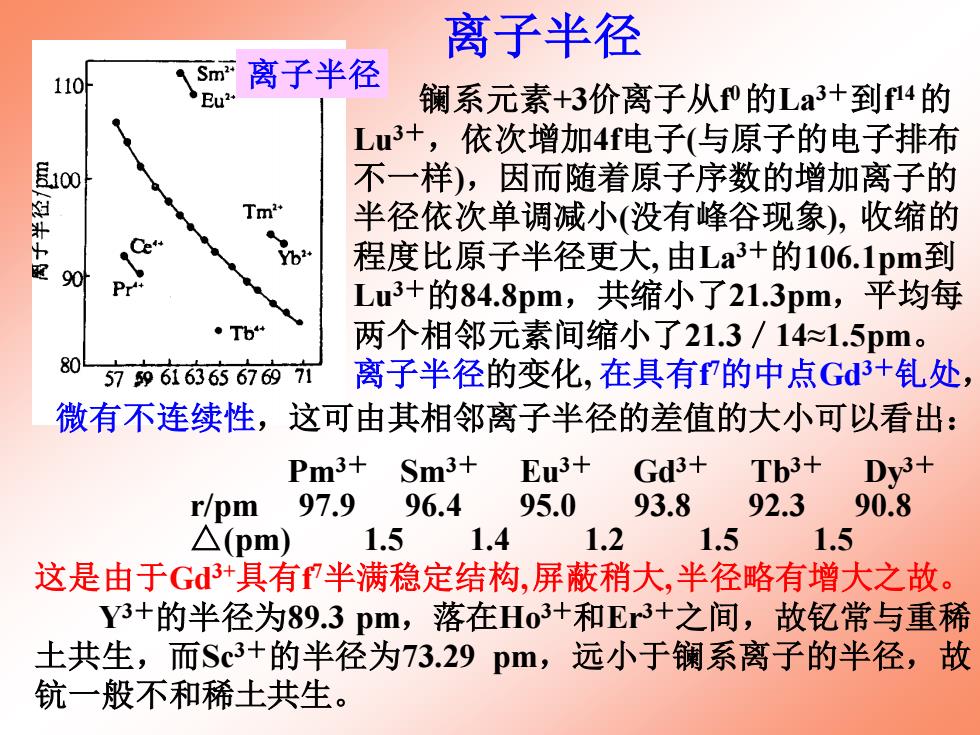
离子半径 Pm3+ Sm3+ Eu3+ Gd3+ Tb3+ Dy3+ r/pm 97.9 96.4 95.0 93.8 92.3 90.8 △(pm) 1.5 1.4 1.2 1.5 1.5 这是由于Gd3+具有f 7半满稳定结构,屏蔽稍大,半径略有增大之故。 Y3+的半径为89.3 pm,落在Ho3+和Er3+之间,故钇常与重稀 土共生,而Sc3+的半径为73.29 pm,远小于镧系离子的半径,故 钪一般不和稀土共生。 镧系元素+3价离子从f 0 的La3+到f 14 的 Lu3+,依次增加4f电子(与原子的电子排布 不一样),因而随着原子序数的增加离子的 半径依次单调减小(没有峰谷现象), 收缩的 程度比原子半径更大, 由La3+的106.1pm到 Lu3+的84.8pm,共缩小了21.3pm,平均每 两个相邻元素间缩小了21.3/14≈1.5pm。 离子半径的变化, 在具有f 7的中点Gd3+钆处, 微有不连续性,这可由其相邻离子半径的差值的大小可以看出: 离子半径

10.1.4Ln3+离子的碱度及镧系离子的分离 某种金属离子吸引电子或阴离子的能力被称为该金属 离子的“相对碱度”。孔力越强,碱度越弱。 碱度的强弱可用金属离子的离子势φ(=Z)来量度, 离子势值越人大(即半径小,电荷高则碱度越弱。 对于镧系电荷相同的离子,随着原子序数增加,离子半 径减小,离子势逐渐增大,离子的碱度减弱。 利用L3+离子半径的微小差别,亦即碱度的微小差别, 可以对镧系离子进行分离:
某种金属离子吸引电子或阴离子的能力被称为该金属 离子的“相对碱度” 。引力越强,碱度越弱。 碱度的强弱可用金属离子的离子势φ(=Z/r)来量度, 离子势值越大(即半径小,电荷高)则碱度越弱。 对于镧系电荷相同的离子, 随着原子序数增加,离子半 径减小,离子势逐渐增大,离子的碱度减弱。 利用Ln3+离子半径的微小差别, 亦即碱度的微小差别, 可以对镧系离子进行分离: 10.1.4 Ln3+离子的碱度及镧系离子的分离
镧系元豪的碱性、Ln(OH),开始沉淀的pH 值及溶度积和溶解度(8K LrOH) 如:Ln3+水 Ln(OH),开始沉淀时的pH值 离子 中=Zr t.Ln(OH) 溶解度 解生成Ln(OHD3 硝酸盐 氯化物 硫酸盐 醋酸盐 (×10 mol.dm) 沉淀的趋势随原 La 283 7.82 8.03 7.41 7.93 1.0×10-19 7.8 子序数的增加 2.84 7.60 7.41 7.35 7.77 1.5×100 48 296 (即碱度减弱)而 7.35 7.05 7.17 7.66 27×102 5.4 d 3.02 7.31 7.02 695 7.59 1.9×1024 27 增加,当加入 NaOH时,溶解 3.11 692 6.83 670 7.40 6.8×102 2.0 度最小、碱度最 682 6.68 7.18 3.4×102 1.4 683 675 21.×102 1.4 弱的Lu将最先以 20×102 Lu(OH田)3的形式 功场 1.4×102 沉淀出来,而溶 5.0×10” 解度最大,碱度 676 6.50 6.59 1.3×102” a8 3.45 最强的La将最后 640 6.21 6.53 3.3×102 w 06 3.50 630 618 6.50 29×104 05 以La(OD3沉淀 Lu+ 3.54 630 6.18 6.46 25×104 05 析出
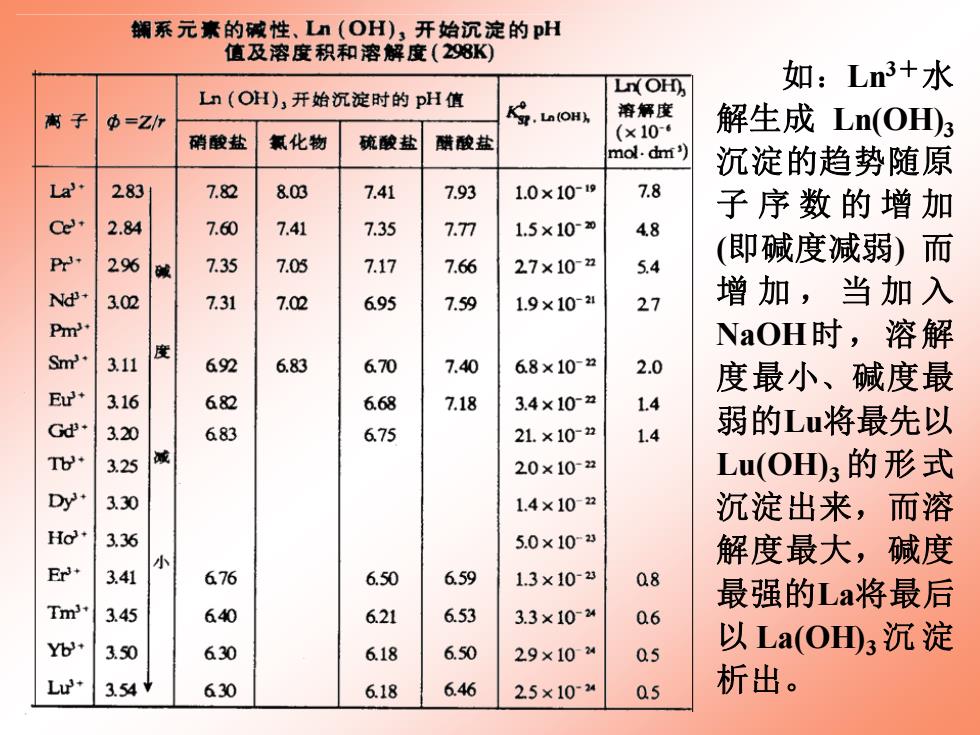
如:Ln3+水 解生成 Ln(OH)3 沉淀的趋势随原 子 序 数 的 增 加 (即碱度减弱) 而 增 加 , 当加入 NaOH时,溶解 度最小、碱度最 弱的Lu将最先以 Lu(OH)3 的形式 沉淀出来,而溶 解度最大,碱度 最强的La将最后 以 La(OH)3 沉 淀 析出

又如:L3+离子生成配合物的稳定性多是随离 子半径的减小,即碱度减弱而增大的。例如在H一 型阳离子交换树脂上使L3+离子溶液流下,这时将 发生L3+离子与H+离子的交换而被吸附在阳离子 交换柱上。然后,用螯合剂(如EDTA)在适当的pH 值和流速下淋洗,此时,半径较小、碱度较弱、能 形成较稳定配合物的重镧系离子将从交换柱上最先 被淋洗出来。假如条件控制得好,各个L3+离子可 以全部被分离开,至少可以被分成几个组。当这个 过程在串联起来的若干个交换柱上进行时(类似于多 次分离),其分离效果就更好
又如:Ln3+离子生成配合物的稳定性多是随离 子半径的减小,即碱度减弱而增大的。例如在H- 型阳离子交换树脂上使Ln3+离子溶液流下,这时将 发生Ln3+离子与H+离子的交换而被吸附在阳离子 交换柱上。然后,用螯合剂(如EDTA)在适当的pH 值和流速下淋洗,此时,半径较小、碱度较弱、能 形成较稳定配合物的重镧系离子将从交换柱上最先 被淋洗出来。假如条件控制得好, 各个Ln3+离子可 以全部被分离开,至少可以被分成几个组。当这个 过程在串联起来的若干个交换柱上进行时(类似于多 次分离),其分离效果就更好