二)离子键和共价键 离子键:原子间通过电子转移产生正负离子,两者相互 吸引形成的化学键。 Na C Na Cl 共价键:成键的两个原子各提供一个电子,通过共用一 对电子相互结合的化学键。共用两对电子形成 双键. HH HH H C.CC.CH CHaCH2CH2CH3 HH HH 或CH3CH22CH3 易斯构造式 短线(或网绪)构造式 构造简式
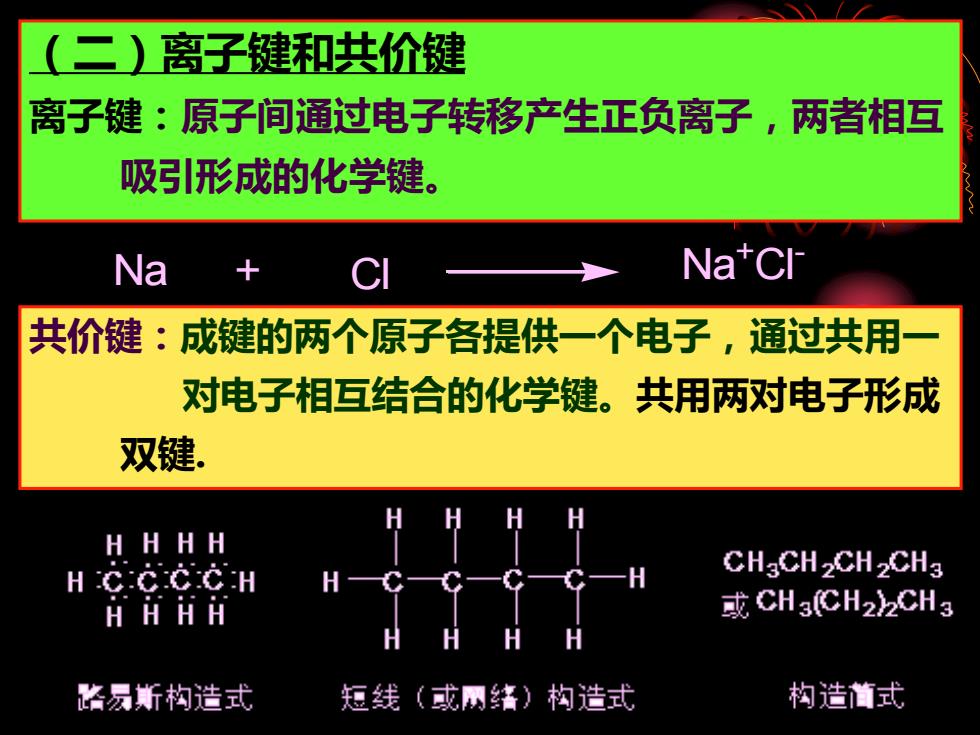
(二)离子键和共价键 离子键:原子间通过电子转移产生正负离子,两者相互 吸引形成的化学键。 Na + Cl Na +Cl - Na + Cl Na + Cl - 共价键:成键的两个原子各提供一个电子,通过共用一 对电子相互结合的化学键。共用两对电子形成 双键

配位键:是一种特殊的共价键。特点是形成共价键的 一对电子是由一个原子提供的。 NH3 +H :N:H (三)现代共价键理论 1.原子轨道和电子云:原子轨道用电子波函数φ表 示反映电子的运动状态。电子云形象化地描述电子在 核外出现的几率密度。 1s轨道 1s电子云
配位键:是一种特殊的共价键。特点是形成共价键的 一对电子是由一个原子提供的。 :N:H + NH3 + H + 1s电子云 (三)现代共价键理论 1.原子轨道和电子云:原子轨道用电子波函数φ表 示反映电子的运动状态。电子云形象化地描述电子在 核外出现的几率密度。 1s轨道
2.价键法:1)共价键的成键条件:形成共价键的电子 必须自旋方向相反 2)共价键的饱和性:元素原子的共价数等 于该原子的未成对电子数。 3)共价键的方向性:成键的两个原子轨道 必须按照一定的方向重叠,以满足最大 重叠原理。 相互常拢 电子云相互重叠 形成H分子的 共价健(H一日)
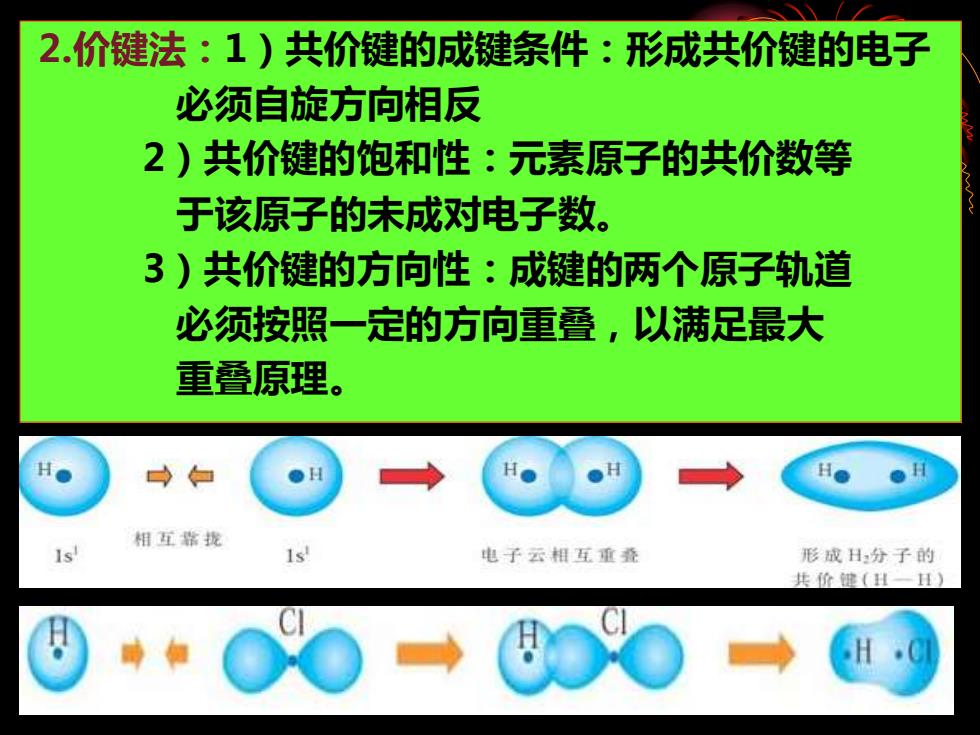
2.价键法:1)共价键的成键条件:形成共价键的电子 必须自旋方向相反 2)共价键的饱和性:元素原子的共价数等 于该原子的未成对电子数。 3)共价键的方向性:成键的两个原子轨道 必须按照一定的方向重叠,以满足最大 重叠原理
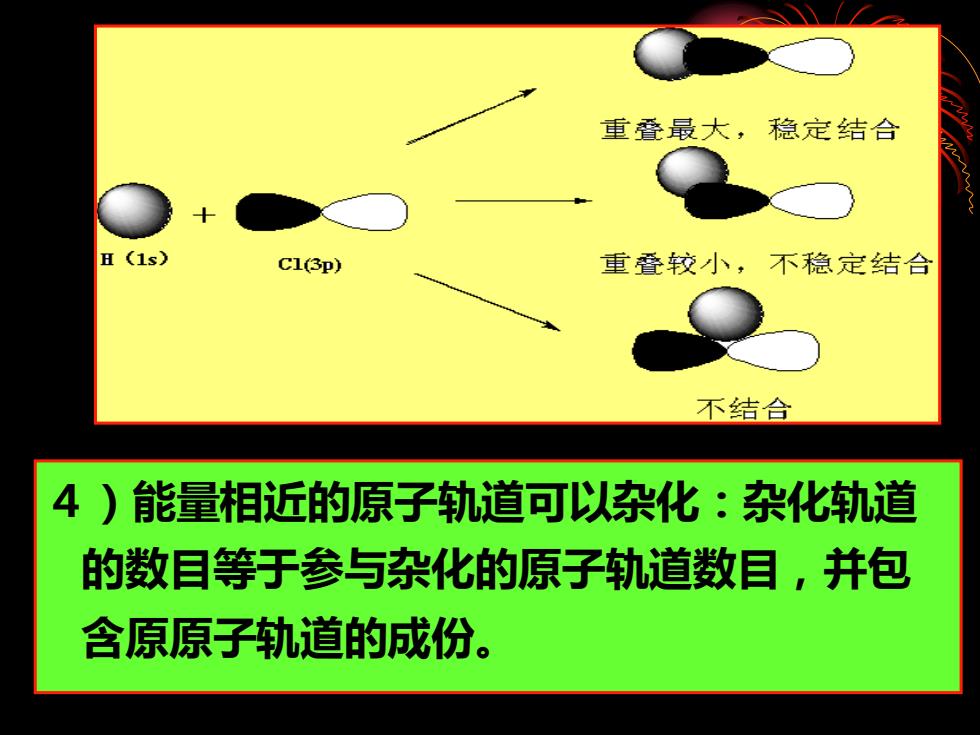
重叠最大,稳定结合 H(1s) C1(3p) 重叠较小,不稳定结合 不结合 4)能量相近的原子轨道可以杂化:杂化轨道 的数目等于参与杂化的原子轨道数目,并包 含原原子轨道的成份
4)能量相近的原子轨道可以杂化:杂化轨道 的数目等于参与杂化的原子轨道数目,并包 含原原子轨道的成份