
剂,直到沉淀完全为止。 如反应需要在一定的酸度下进行,则在加酸或加碱的同时要 充分搅拌,并用搅拌棒蘸少量溶液以pH试纸检查(pH试纸剪成 小块,分放在干的白瓷板或表面皿上),或加酸碱指示剂于试液中, 用来指示溶液的酸碱性。 (2)在点滴板上进行沉淀一般适用于少量试液和试剂在常 温下产生沉淀的鉴定反应。若生成白色沉淀可使用黑色点滴板。 (3)在滤纸上进行沉淀当某种离子与适当试剂作用生成沉 淀时,由于纸的毛细作用,除沉淀外的其它离子均匀扩散至沉淀区 域之外,这样可同时达到分离和鉴定的目的。 6,沉淀的离心沉降和沉淀与溶液的分离 将带有沉淀的离心管放在离心机的管套中,开动离心机,沉淀 微粒受离心力的作用而沉降在离心管的尖端。 图2-11毛细管的使用 图2-12用毛细管吸取少量溶液 离心沉降后可用毛细管(或滴管)将离心液吸出。方法如下。 先用手指捏毛细管上端的橡皮乳头,排出其中的空气,将离心管倾 斜,把毛细管尖端伸入离心液液面下,但不可触及沉淀,然后慢慢 放松橡皮乳头,则溶液被吸入毛细管(图2-11)。将毛细管从溶 液中取出,把溶液移入另一清洁的离心管中。如有必要可重复上
。将毛细管从溶 图 剂,直到沉淀完全为止。 试纸检查( 如反应需要在一定的酸度下进行,则在加酸或加碱的同时要 充分搅拌,并用搅拌棒蘸少量溶液以 试纸剪成 小块,分放在干的白瓷板或表面皿上),或加酸碱指示剂于试液中, 用来指示溶液的酸碱性。 )在点滴板上进行沉淀 一般适用于少量试液和试剂在常 温下产生沉淀的鉴定反应。若生成白色沉淀可使用黑色点滴板。 )在滤纸上进行沉淀 当某种离子与适当试剂作用生成沉 淀时,由于纸的毛细作用,除沉淀外的其它离子均匀扩散至沉淀区 域之外,这样可同时达到分离和鉴定的目的。 沉淀的离心沉降和沉淀与溶液的分离 将带有沉淀的离心管放在离心机的管套中,开动离心机,沉淀 微粒受离心力的作用而沉降在离心管的尖端。 图 用毛细管吸取少量溶液 离心沉降后可用毛细管(或滴管)将离心液吸出。方法如下。 先用手指捏毛细管上端的橡皮乳头,排出其中的空气,将离心管倾 斜,把毛细管尖端伸入离心液液面下,但不可触及沉淀,然后慢慢 放松橡皮乳头,则溶液被吸入毛细管(图 液中取出,把溶液移入另一清洁的离心管中。如有必要可重复上 毛细管的使用

述操作。沉淀表面上少量的溶液用去掉橡皮乳头的毛细吸管更为 合适(图2-12),方法是:将离心管倾斜,把毛细吸管的尖端小心 地浸入溶液(此时毛细吸管上部应靠在离心管口),借毛细作用使 液体进入毛细管中,注意毛细管尖端与沉淀表面的距离不应小于 1mm当液体沿毛细吸管停止上升时,将其从离心管中取出,溶液 可并入同一离心管中。用这种方法可将沉淀与溶液完全分离。 7,沉淀的洗涤 沉淀与溶液分离后必须仔细洗涤,否则可能被溶液中别的离 子玷污,而使分析结果不正确。 洗涤沉淀的方法是:用滴管加数滴洗涤液,用搅拌棒充分搅拌 后,离心沉降,用滴管或毛细吸管吸出洗涤液,每次尽可能把洗涤 液完全吸尽。一般情况下洗涤2~3次即可。第一次洗涤液并入 离心液中,第二、三次洗涤液可弃去。必要时应检验是否洗净。方 法是:将一滴洗涤液放在点滴板上,加入适当试剂,检查应分离出 去的离子是否还存在,如产生正反应,说明未洗净:如产生负反应 则洗涤已完成。 8.沉淀的转移和溶解 沉淀如需分成几份,可在洗净的沉淀上加几滴蒸馏水,将滴管 伸入溶液,挤压橡皮乳头,借挤出的空气搅动沉淀,使之悬浮于溶 液中,然后放松橡皮乳头,浑浊液则进入滴管,便可将其转移到另 外的容器中。 如欲溶解沉淀,可在不断搅拌下,慢慢滴加适当试剂。溶解沉 淀一般都在分离和洗涤后立即进行,因经长时间放置的或已干的 沉淀较难溶解。 9.纸上点滴分析 (1)应先将试剂或试液滴在点滴板上,然后用去掉橡皮乳头 的毛细吸管在点滴板上取用。切不可将毛细吸管直接插入试剂瓶 中吸取试剂。毛细吸管用后应洗净,并用滤纸吸干。 (2)取用试液或试剂时,先将毛细吸管尖端浸入所需溶液中
次即可。第一次洗涤液并入 合 适( 图 述操作。沉淀表面上少量的溶液用去掉橡皮乳头的毛细吸管更为 ,方法是:将离心管倾斜,把毛细吸管的尖端小心 地浸入溶液(此时毛细吸管上部应靠在离心管口),借毛细作用使 液体进入毛细管中,注意毛细管尖端与沉淀表面的距离不应小于 ,当液体沿毛细吸管停止上升时,将其从离心管中取出,溶液 可并入同一离心管中。用这种方法可将沉淀与溶液完全分离。 沉淀的洗涤 沉淀与溶液分离后必须仔细洗涤,否则可能被溶液中别的离 子玷污,而使分析结果不正确。 洗涤沉淀的方法是:用滴管加数滴洗涤液,用搅拌棒充分搅拌 后,离心沉降,用滴管或毛细吸管吸出洗涤液,每次尽可能把洗涤 液完全吸尽。一般情况下洗涤 离心液中,第二、三次洗涤液可弃去。必要时应检验是否洗净。方 法是:将一滴洗涤液放在点滴板上,加入适当试剂,检查应分离出 去的离子是否还存在,如产生正反应,说明未洗净;如产生负反应, 则洗涤已完成。 沉淀的转移和溶解 沉淀如需分成几份,可在洗净的沉淀上加几滴蒸馏水,将滴管 伸入溶液,挤压橡皮乳头,借挤出的空气搅动沉淀,使之悬浮于溶 液中,然后放松橡皮乳头,浑浊液则进入滴管,便可将其转移到另 外的容器中。 如欲溶解沉淀,可在不断搅拌下,慢慢滴加适当试剂。溶解沉 淀一般都在分离和洗涤后立即进行,因经长时间放置的或已干的 沉淀较难溶解。 纸上点滴分析 应先将试剂或试液滴在点滴板上,然后用去掉橡皮乳头 的毛细吸管在点滴板上取用。切不可将毛细吸管直接插入试剂瓶 中吸取试剂。毛细吸管用后应洗净,并用滤纸吸干。 取用试液或试剂时,先将毛细吸管尖端浸入所需溶液中

1~2mm处,然后将毛细吸管取出,垂直持毛细吸管,使管尖与滤 纸接触,轻轻压在滤纸上,如图2-13。纸上的潮湿斑点直径扩大 成5~10mm时,再将毛细吸管迅速拿开,在所生成的潮湿斑点中 心,依照同样规则,用吸有适当试剂的毛细吸管与其接触。溶液绝 对不得滴在滤纸上。滤纸应先做空白试验。 (3)斑点力求圆形,这样可保 证试液或试剂均匀分布和“点滴图 像”准确、清晰。 (4)加试剂时必须按照一定 的顺序,否则可能得出错误的结 论。 (5)滤纸不要直接放在实验 台上或书本上进行操作,最好悬空 图2-13点滴反应方法 操作,即用拇指和食指水平拿着滤 1.毛细管2.反应纸3.湿斑 纸两侧,或将滤纸放在清洁干燥的 坩埚口上进行操作。 10.焰色反应 将镍铬丝或铂丝做成环状。用浓HC!溶液湿润金属环,在煤 气灯氧化焰中灼烧,如此反复处理几次,直到火焰不染色,此时表 示金属丝已清洁。然后再蘸取试液在氧化焰中灼烧,观察火焰的 颜色。 试验完毕后应将金属丝洗净。 注意不能将铂丝放在还原焰中灼烧,以免生成碳化铂,使铂丝 脆断。 11.气体分析 (1)气室反应气室是两块小表面皿合在一起构成的(图2- 14)。先将试纸(石蕊试纸或pH试纸)或浸过所需试剂的滤纸,润 湿后贴在上表面皿凹面上,然后再在下表面皿中放试液和试剂,立 即将贴好试纸的表面皿盖上,在水浴上加热,待反应发生后,观察
处,然后将毛细吸管取出,垂直持毛细吸管,使管尖与滤 纸接触,轻轻压在滤纸上,如图 。纸上的潮湿斑点直径扩大 成 时,再将毛细吸管迅速拿开,在所生成的潮湿斑点中 反应纸 湿斑 心,依照同样规则,用吸有适当试剂的毛细吸管与其接触。溶液绝 对不得滴在滤纸上。 滤纸应先做空白试验。 斑点力求圆形,这样可保 证试液或试剂均匀分布和“点滴图 像”准确、清晰。 加试剂时必须按照一定 的顺序,否则可能得出错误的结 论。 图 点滴反应方法 毛 细管 滤纸不要直接放在实验 台上或书本上进行操作,最好悬空 操作,即用拇指和食指水平拿着滤 纸两侧,或将滤纸放在清洁干燥的 坩埚口上进行操作。 焰色反应 将镍铬丝或铂丝做成环状。用浓 溶液湿润金属环,在煤 气灯氧化焰中灼烧,如此反复处理几次,直到火焰不染色,此时表 示金属丝已清洁。然后再蘸取试液在氧化焰中灼烧,观察火焰的 颜色。 试验完毕后应将金属丝洗净。 注意不能将铂丝放在还原焰中灼烧,以免生成碳化铂,使铂丝 脆断。 气体分析 试纸)或浸过所需试剂的滤纸,润 气室反应 气室是两块小表面皿合在一起构成的(图 。先将试纸(石蕊试纸或 湿后贴在上表面皿凹面上,然后再在下表面皿中放试液和试剂,立 即将贴好试纸的表面皿盖上,在水浴上加热,待反应发生后,观察
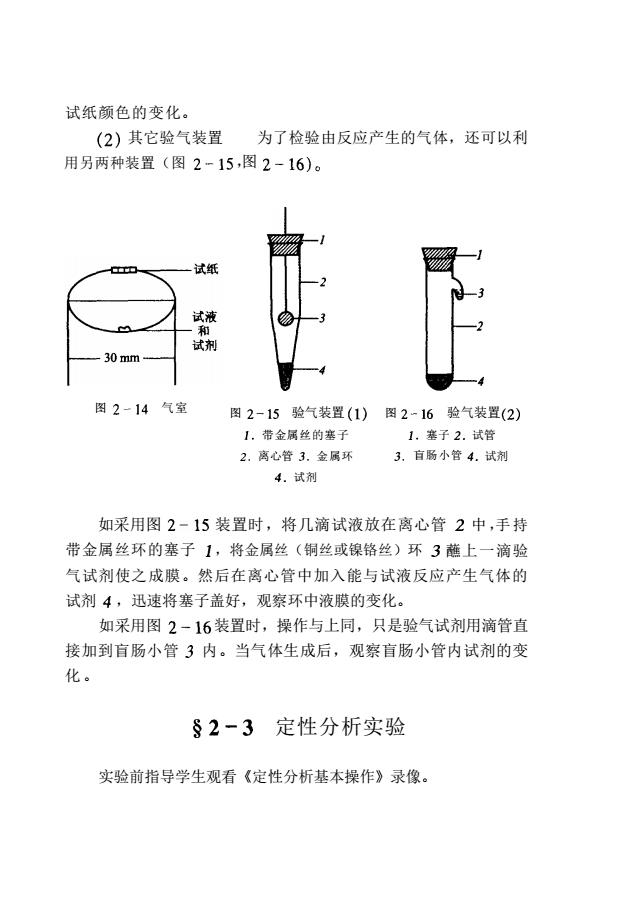
试纸颜色的变化。 (2)其它验气装置为了检验由反应产生的气体,还可以利 用另两种装置(图2-15,图2-16)。 图2-14气室 图2-15验气装置(1)图2-16验气装置(2 1.带金属丝的塞子 1.塞子2.试管 2.离心管3.金属环 3.盲肠小管4.试剂 4.试剂 如采用图2-15装置时,将几滴试液放在离心管2中,手持 带金属丝环的塞子1,将金属丝(铜丝或镍铬丝)环3蘸上一滴验 气试剂使之成膜。然后在离心管中加入能与试液反应产生气体的 试剂4,迅速将塞子盖好,观察环中液膜的变化。 如采用图2-16装置时,操作与上同,只是验气试剂用滴管直 接加到盲肠小管3内。当气体生成后,观察盲肠小管内试剂的变 化。 §2-3定性分析实验 实验前指导学生观看《定性分析基本操作》录像
内。当气体生成后,观察盲肠小管内试剂的变 装置时,操作与上同,只是验气试剂用滴管直 图 气室 图 验气装置 图 验气装置 带金属丝的塞子 塞子 试管 离心管 金属环 盲肠小管 试剂 试剂 如采用图 装置时,将几滴试液放在离心管 中,手持 带金属丝环的塞子 ,将金属丝(铜丝或镍铬丝)环 蘸上一滴验 试纸颜色的变化。 用另两种装置(图 其它验气装置 为了检验由反应产生的气体,还可以利 ,图 气试剂使之成膜。然后在离心管中加入能与试液反应产生气体的 试剂 ,迅速将塞子盖好,观察环中液膜的变化。 如采用图 接加到盲肠小管 化 。 实验前指导学生观看《定性分析基本操作》录像。 定性分析实验

实验2-1阳离子第I组Ag*,Hg+的分析 一、本组离子的分析方法 本组离子的组试剂为稀HCI溶液。 常见阳离子中只有Ag.Hg和Pb2+的氯化物难溶于水。 而PbC2溶解度较大,可溶于热水,而AgC1,Hg2C2则不溶。为 此,可将PbC2加热溶解,并将其分到阳离子第Ⅱ组,否则Pb2+跨 两组,使得Pb2+的检出困难。 Ag*Cl=AgCl Hg?*+2Cl-=Hg2Cl2 Pb2++2C1—PbC2↓ PbCkPb2 +2CI- Hg2Cl2可溶于HNO3与HCI的混合酸中,生成稳定的 HgC,在此条件下,AgCl不溶。可采用此法将Ag*和Hg·分 离。其反应如下: 3Hg2Ci2 +18CI+2NO+8H*-6HgCl+2NO+4H2O AgCI易溶于氨水,形成Ag(NH3).Hg2C2与NH3反应形成 难溶于水的氨基化合物并析出Hg,借此也可将两者分离: AgCI+2NH3-Ag(NH3)+Cl Hg2Cl2 +2NH3-Hg2 NH2Cl+NH Cl Hg2 NH2CI-HgNH2 CI+Hg 但如有大量Hg*存在时,则Ag可能被生成的Hg还原为金属银 而留在沉淀中: 2AgCI+2Hg 2NH,-2Ag+Hg2 NH2 CI+NH.CI
而留在沉淀中: 但如有大量 存在时,则 可能被生成的 还原为金属银 难溶于水的氨基化合物并析出 ,借此也可将两者分离: 易溶于氨水,形成 , 与 反应形成 离。其反应如下: ,在此条件下, 不溶。可采用此法将 和 分 可 溶 于 与 的 混 合 酸 中 , 生 成 稳 定 的 两组,使得 的检出困难。 此,可将 加热溶解,并将其分到阳离子第 组 ,否 则 跨 而 溶解度较大,可溶于热水,而 则不溶。为 常见阳离子中只有 , 和 的氯化物难溶于水。 本组离子的组试剂为稀 溶液。 一、本组离子的分析方法 实验 阳离子第 组 的分析